Clear Sky Science · it
Migliorare le prestazioni dei fotosensori Magnets
Plasmare le cellule con fasci di luce
Immaginate di poter accendere e spegnere geni con un fascio di luce con la stessa semplicità di un interruttore. Questo studio mostra come i ricercatori abbiano migliorato una famiglia popolare di “interruttori” proteici sensibili alla luce, chiamati fotosensori Magnets, rendendoli più precisi e potenti nel rispondere alla luce blu. Questi interruttori perfezionati potrebbero aiutare a controllare il comportamento cellulare usando meno luce, causando meno danni e offrendo maggiore flessibilità in batteri e persino in cellule di mammifero.
Perché la luce è una manopola di controllo potente
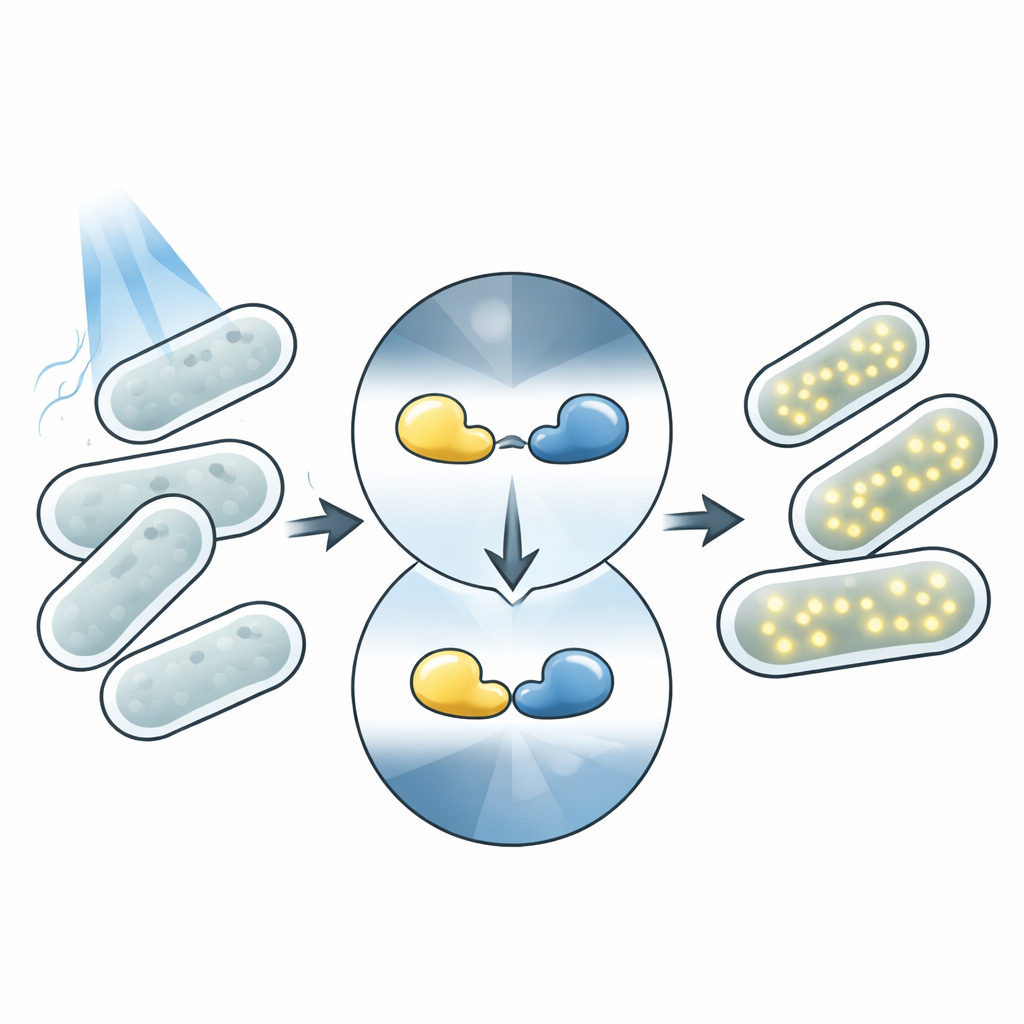
La luce è un telecomando ideale per la biologia. A differenza di additivi chimici, la luce può essere applicata istantaneamente, rimossa altrettanto rapidamente e focalizzata su regioni molto piccole senza toccare le cellule. Molti organismi contengono naturalmente proteine che cambiano forma quando assorbono luce, innescando effetti a valle. L’optogenetica moderna riutilizza queste proteine come componenti controllabili: una “testa” sensibile alla luce viene fusa a un modulo “d’azione”, come un enzima o un interruttore genico. Quando la luce colpisce, il sensore cambia conformazione e attiva la funzione collegata. I fotosensori Magnets sono una coppia di tali proteine che si uniscono sotto luce blu e si separano al buio, rendendoli uno strumento di riferimento per costruire sistemi controllati dalla luce.
Come funziona l’interruttore Magnet nelle cellule
In questo lavoro, il gruppo si concentra su un sistema sensibile alla luce blu chiamato Opto-T7RNAP. Qui, la coppia Magnets è fusa a due metà di un enzima ripartito, la RNA polimerasi T7, che guida l’espressione di un gene bersaglio. Nel buio le metà restano separate e il gene è per lo più silente. Sotto luce blu, i domini Magnets si legano tra loro, avvicinando le metà dell’enzima così che il gene si attivi e produca una proteina fluorescente rossa facilmente misurabile. Questa configurazione collega strettamente la sequenza del DNA di ciascuna proteina sensibile alla luce a un segnale visibile, permettendo ai ricercatori di valutare le prestazioni di migliaia di varianti semplicemente misurando quanto brillano le cellule.
Cambiamento casuale e selezione accurata
Piuttosto che indovinare quali singoli amminoacidi modificare, gli autori hanno usato la mutagenesi casuale per introdurre cambiamenti in tutto ogni proteina Magnet e poi hanno lasciato che i dati rivelassero quali versioni funzionassero meglio. Hanno creato grandi librerie di varianti mutate di nMag e pMag e le hanno introdotte in batteri contenenti Opto-T7RNAP e il gene reporter fluorescente. Utilizzando lo smistamento cellulare basato sulla fluorescenza (FACS), hanno eseguito una selezione in più fasi: prima arricchendo le cellule che brillavano intensamente sotto luce blu tenue, poi scartando quelle che brillavano troppo al buio e infine isolando cloni individuali per test dettagliati. Il livello di fluorescenza di ciascuna variante è stato seguito sia cellula per cellula mediante citometria a flusso sia in colture in massa nel tempo con spettrofotometria automatizzata.
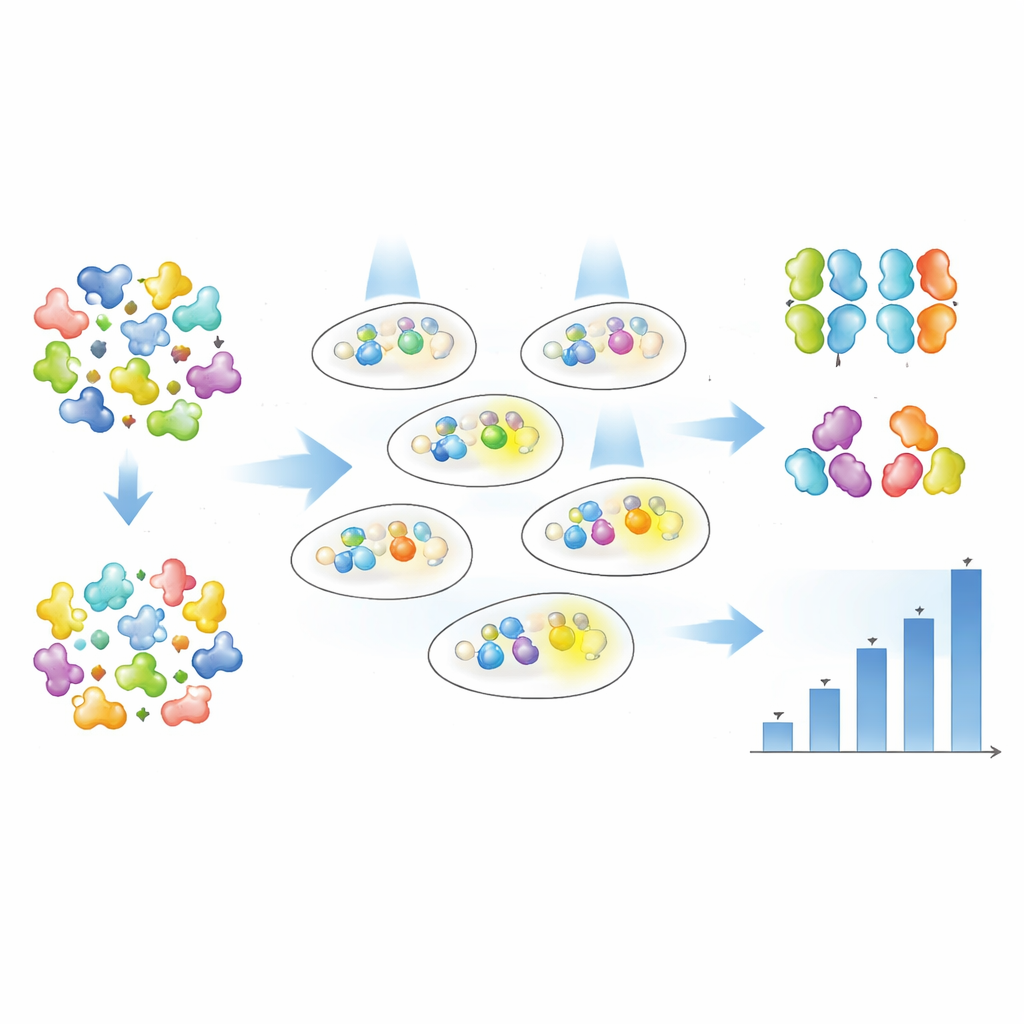
Aggiustare finemente sensibilità e intensità
Dalla sola prima tornata di screening, il team ha trovato 19 varianti distinte di Magnet con un ricco insieme di comportamenti. Alcuni mutanti hanno reso il sistema molto più sensibile alla luce, cioè lo stesso output genico poteva essere raggiunto con intensità luminosa molto più bassa. Altri hanno aumentato principalmente quanto forte il gene veniva attivato a piena illuminazione, e alcuni hanno fatto entrambe le cose. Importante, gli autori hanno dimostrato che “quanta luce è necessaria” (sensibilità) e “quanto output genico si ottiene” (attivazione) possono essere sintonizzati in modo in gran parte indipendente. In alcune varianti, l’attivazione a metà massima si raggiungeva con circa metà della luce, mentre l’output massimo restava simile; in altre, l’output massimo aumentava di più volte mantenendo sensibilità pressoché invariata. Confrontando molte varianti a diverse temperature, hanno inoltre identificato versioni che mantengono un’attività più forte in condizioni simili a quelle corporee e che mostrano comportamento robusto durante la crescita della popolazione cellulare.
Nuovi mattoni per la biologia controllata dalla luce
Per un non specialista, il messaggio principale è che questi scienziati hanno trasformato un singolo interruttore della luce in un intero pannello dimmer. Invece di un sensore fisso per la luce blu, ora offrono un menu di varianti Magnet che richiedono più o meno luce, producono risposte geniche più forti o più lievi, o funzionano bene a diverse temperature. Poiché i Magnets sono già ampiamente usati nella biologia sintetica e sono stati adattati a cellule di mammifero, queste versioni migliorate possono essere inserite in molti progetti esistenti. In termini pratici, ciò significa che esperimenti che necessitano di illuminazione delicata e prolungata possono usare varianti altamente sensibili, mentre applicazioni che devono evitare attivazioni accidentali dalla luce ambiente possono usare varianti meno sensibili. Il lavoro amplia così la cassetta degli attrezzi per scolpire con precisione il comportamento cellulare con la luce nella ricerca e nelle biotecnologie.
Citazione: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Parole chiave: optogenetica, espressione genica controllata dalla luce, ingegneria delle proteine, proteine fotosensoriali, biologia sintetica