Clear Sky Science · zh
尤因肉瘤原发肿瘤与转移灶的蛋白组学图谱
这项儿童癌症研究的重要性
尤因肉瘤是一种罕见但侵袭性的骨癌,主要发生在儿童和青少年身上。对于家庭和医生而言存在一个令人不安的难题:一些肿瘤对化疗反应良好、患者预后良好,而另一些在相同治疗下却复发或转移。这项研究罕见地深入分析了来自74位年轻患者的170个肿瘤样本中的实际蛋白质,探讨是什么因素让某些肿瘤更容易治疗,以及机体自身的免疫细胞如何塑造疾病进程。
从蛋白水平解读肿瘤
以往对尤因肉瘤的大多数研究集中在DNA和RNA上,这些信息告诉我们癌细胞可能会做什么。蛋白质则揭示癌症实际在做什么。研究者使用先进的质谱技术,在每个肿瘤样本中测量了超过1万种蛋白,样本来自不同阶段的患者:新诊断、化疗后、复发期间以及已转移到肺或骨的病灶。通过精细分离肿瘤区域并筛选高癌细胞含量的样本,他们创建了迄今为止该疾病最详尽的蛋白图谱之一。该图谱使他们能够比较肿瘤随时间的变化,以及这些变化如何与治疗反应和生存相关联。
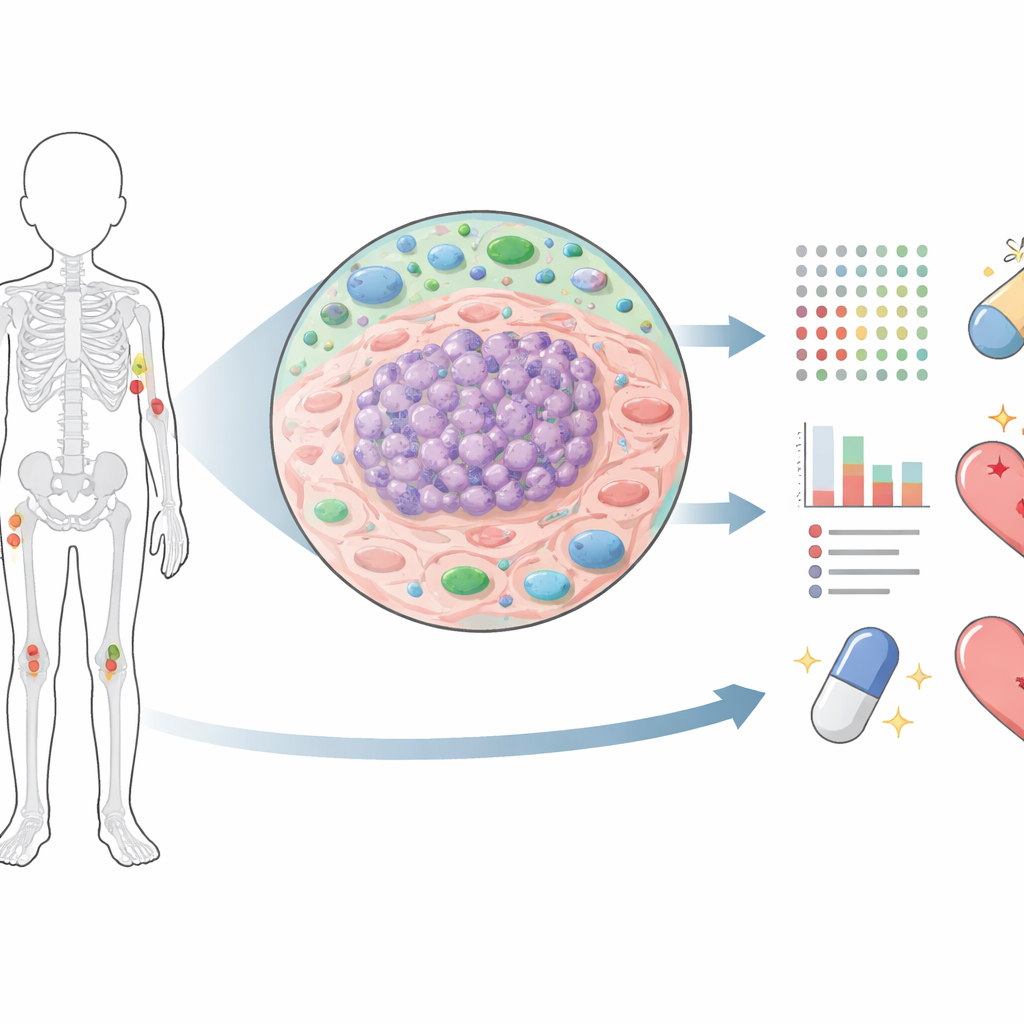
治疗如何重塑癌症
当团队将原发肿瘤与化疗后取样比较时,观察到蛋白组景观发生了广泛变化。参与细胞分裂、DNA修复和构建新细胞器的蛋白在治疗后显著下降,这与化疗抑制快速增殖细胞相一致。但在随后复发或进展的肿瘤中,许多相同的蛋白又再次升高,表明幸存细胞重新激活了生长和修复程序。与此同时,化疗后肿瘤显示出更高水平的免疫相关蛋白和缺氧应激标志,暗示化疗留下的是一个处于应激、炎症但具适应性的肿瘤残余,而非一个干净的清除。
铁、细胞死亡与耐药
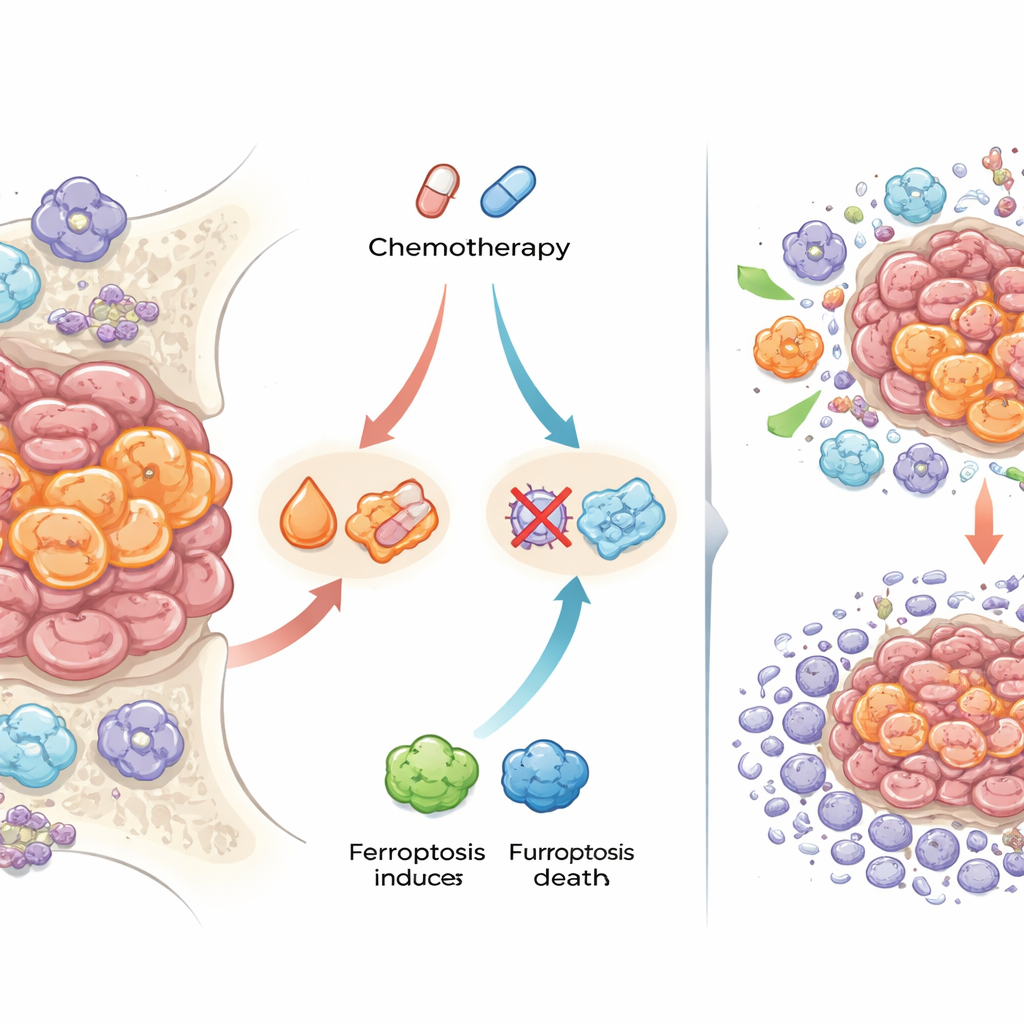
最引人注目的发现之一涉及铁代谢相关蛋白和一种依赖铁驱动的细胞膜损伤的特殊细胞死亡形式——铁死亡。化疗后,许多肿瘤中的癌细胞表现出更高水平的铁蛋白(用于储存铁)和转铁蛋白受体(用于摄取铁),并染色显示游离铁沉积。它们还表达已知可阻断铁死亡并减少氧化损伤的蛋白。为检验这一现象是否与治疗有关,研究者使用在体外培养并对标准药物产生耐药性的尤因肉瘤三维“球体”模型。当他们将化疗与诱导铁死亡的化合物联合使用时,耐药球体变得更为敏感,所需药物剂量降低就能杀死细胞。这提示一些尤因肉瘤细胞可能正是通过缓冲铁并避免铁死亡而在化疗后幸存。
对肿瘤有利或有害的免疫细胞
由于肿瘤不会孤立生长,团队还考察了肿瘤微环境中免疫细胞与结局的关系。仅基于蛋白模式对原发肿瘤进行分组后,他们发现了三类主要亚型,具有不同的生存率。一类高风险组显示大量细胞周期和泛素相关蛋白以及核心蛋白酶体活性低,同时伴有中性粒细胞和可抑制免疫攻击的“检查点”分子相关的蛋白特征。另一类预后较好的组则具有更高水平参与将肿瘤片段呈递到细胞表面的蛋白,这是激活T细胞的关键步骤。多重免疫荧光成像证实,预后较差的肿瘤更富含中性粒细胞,而预后较好的肿瘤含有更多巨噬细胞、T细胞和HLA阳性的抗原呈递细胞。简单来说,“中性粒细胞主导”的肿瘤倾向于表现更差,而含有更多活跃适应性免疫细胞的肿瘤则倾向于表现更好。
这对未来治疗的意义
综上所述,这项工作表明尤因肉瘤不仅仅是单一基因的错误;它是由癌细胞、铁代谢和免疫成分组成的复杂生态系统,在治疗压力下发生变化。对于患者和临床医生来说,这些发现指向两个有希望的方向。其一,促使癌细胞发生铁死亡的药物可能增强现有化疗的疗效,尤其是在耐药疾病中。其二,基于蛋白的中性粒细胞、巨噬细胞、T细胞和抗原呈递标志物可能有助于识别哪些患者可能从免疫为基础的疗法或组合策略中受益。尽管仍需更多验证,这一蛋白组图谱为将尤因肉瘤隐蔽的生物学转化为更精确、潜在更有效的儿童患者治疗方案提供了路线图。
引用: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
关键词: 尤因肉瘤, 蛋白质组学, 铁死亡, 肿瘤微环境, 儿童癌症