Clear Sky Science · he
נוף הפרוטאומים של גידולי אפינג הראשוניים והגרורות
מדוע מחקר זה על סרטן ילדים חשוב
סרקומת איבינג היא סרטן עצם נדיר אך תוקפני שפוגע בעיקר בילדים ובמתבגרים. משפחות ורופאים ניצבים בפני חידה מדאיגה: חלק מהגידולים מגיבים היטב לכימותרפיה והחולים מסתדרים, בעוד אחרים חוזרים או מתפשטים אף על פי שקיבלו את אותן הטיפולים. המחקר הזה מבצע מבט עמוק ובלתי רגיל לחלבונים עצמם ב‑170 גידולים של 74 מטופלים צעירים, ושואל מה עושה גידול אחד שקל יותר לטפל בו מאשר אחר וכיצד תאי המערכת החיסונית של הגוף מעצבים את המחלה.
מבט לתוך הגידול ברמת החלבון
רוב העבודה הקודמת על סרקומת איבינג התמקדה ב‑DNA וב‑RNA, שמספרים מה הסרטן עלול לעשות. חלבונים מגלים מה הסרטן עושה בפועל. החוקרים השתמשו בספקטרומטריית מסה מתקדמת כדי למדוד יותר מ‑10,000 חלבונים בכל מדגם גידול, שנלקחו ממטופלים בשלבים שונים: אבחנה ראשונית, אחרי כימותרפיה, בזמן הישנות, ובגרורות שהתפשטו לריאות או לעצמות. על ידי חיתוך מוקפד של אזורי הגידול וסינון לפי תכולת תאי סרטן גבוהה, יצרו את אחד המפות החלבוניות המפורטות ביותר למחלה זו עד כה. מפה זו אפשרה להם להשוות כיצד הגידולים משתנים לאורך זמן וכיצד שינויים אלה קשורים לתגובה לטיפול ולהישרדות.
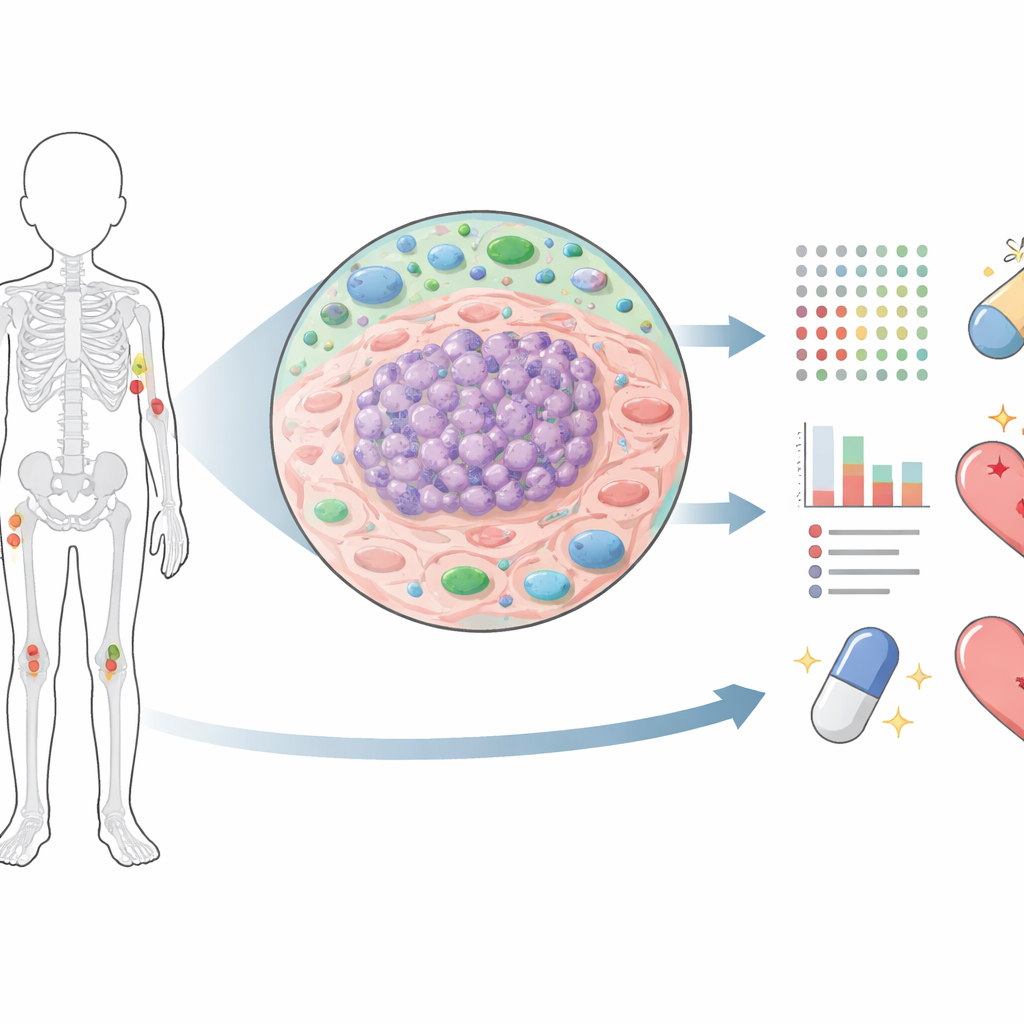
כיצד הטיפול מעצב מחדש את הסרטן
כשקיבלה הקבוצה השוואה בין גידולים ראשוניים למדגמים שנלקחו אחרי כימותרפיה, נצפו שינויים נרחבים בנוף החלבוני. חלבונים המעורבים בחלוקת תאים, בתיקון DNA ובבנייה של מכונות תאיות חדשות ירדו באופן חד אחרי הטיפול, תואם להשפעת הכימותרפיה על תאים הצומחים במהירות. אך בגידולים שחזרו או התקדמו מאוחר יותר, רבים מאותם חלבונים עלו שוב, מה שמרמז שתאים ששרדו הפעילו מחדש תוכניות צמיחה ותיקון. במקביל, בגידולים אחרי הטיפול נרשמו רמות גבוהות יותר של חלבונים קשורים למערכת החיסון וסמנים של מתח מחוסר חמצן, מרמזים שהכימותרפיה משאירה שייר גידולי מדוכדך ומודלק אך גמיש, ולא מצב נקי לחלוטין.
ברזל, מוות תאי ובעמידות לתרופות
אחת הממצאים הבולטים עסקה בחלבוני טיפול בברזל ובצורה מיוחדת של מוות תאי שנקראת פרורוטוזיס (ferroptosis), שתלויה בנזק שמונע על ידי ברזל לממברנות התאים. אחרי כימותרפיה, תאי סרטן ברבים מהגידולים נשאו רמות גבוהות יותר של פריטין (שמאחסן ברזל) ושל רצפטור הטרנספרין (שנכנס ברזל לתא), ונצבעו בצורה שמצביעה על משקעים של ברזל חופשי. הם גם ביטאו חלבונים הידועים כבולמי פרורוטוזיס ומפחיתי נזק חמצוני. כדי לבדוק האם הדבר רלוונטי לטיפול, החוקרים השתמשו בספירואידים תלת‑ממדיים של תאי סרקומת איבינג שעוררו עמידות לתרופות סטנדרטיות. כאשר שילבו כימותרפיה עם תרכובות שמפעילות פרורוטוזיס, הספירואידים העמידים הפכו לרגישים יותר ונדרשו מינונים נמוכים יותר של התרופה כדי להרוגם. ממצאים אלה מצביעים על כך שחלק מתאי סרקומת איבינג עשויים לשרוד כימותרפיה בדיוק משום שהם מאגדים ברזל ומנעים מוות פרורוטוטי.
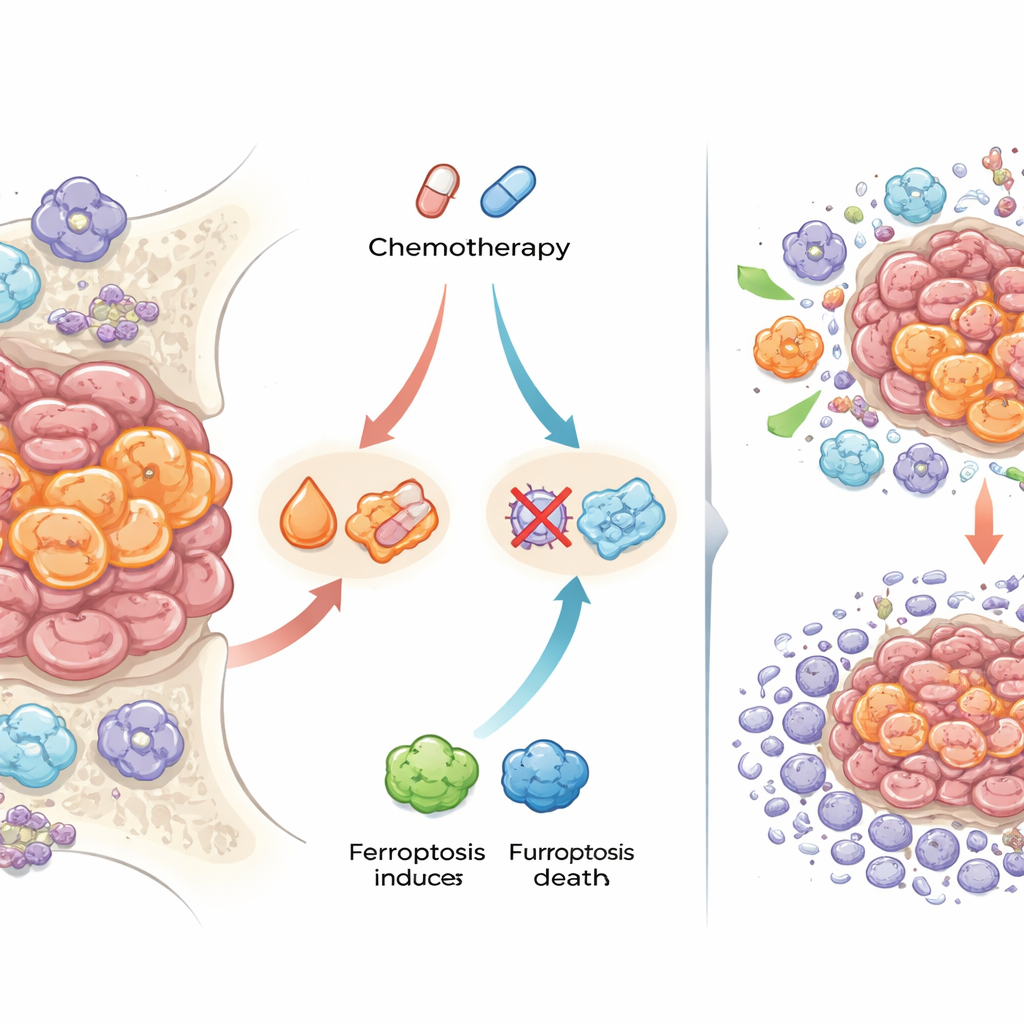
תאי חיסון שעוזרים או מזיקים
מכיוון שגידולים אינם גדלים בבידוד, הצוות בדק גם כיצד תאי החיסון בתוך מיקרו‑הסביבה של הגידול קשורים לתוצאה. על ידי קיבוץ גידולים ראשוניים בהתבסס אך ורק על דפוסי החלבונים שלהם, הם גילו שלוש תת‑כיתות עיקריות עם שיעורי הישרדות שונים. קבוצה בסיכון גבוה הציגה שפע חלבונים הקשורים במחזור התא ובאוביקוויטין ופעילות נמוכה של פרוטאזום מרכזי, יחד עם חתימות של נויטרופילים ומולקולות "צ'ק‑פוינט" שיכולות לדכא מתקפה חיסונית. קבוצה אחרת, עם תוצאות טובות יותר, הציגה רמות גבוהות יותר של חלבונים המעורבים בהצגת קטעי גידול על פני התא, צעד מרכזי בהפעלת תאי T. הדמיה אימונופלורסצנטית מרובה אישרה כי גידולים בקבוצות גרועות היו עשירים יותר בנויטרופילים, בעוד שאלה בקבוצות טובות יותר הכילו יותר מקרופאגים, תאי T ותאים מציגי‑אנטיגן בעלי HLA. בפשטות, גידולים "עשירים בנויטרופילים" נטו להתנהג פחות טוב, בעוד גידולים עם יותר תאי חיסון אדפטיביים מעורבים נטו להתנהג טוב יותר.
מתי פירוש הדבר לטיפול בעתיד
לסיכום, העבודה הזו מראה שסרקומת איבינג היא יותר מטעות גנטית בודדת; היא מערכת אקולוגית מורכבת של תאי סרטן, מטבוליזם ברזל ושחקני חיסון שמשתנה תחת לחץ הטיפול. עבור מטופלים ורופאים, הממצאים מצביעים על שתי רעיונות מבטיחים. ראשית, תרופות שמדחפות תאים סרטניים לכיוון פרורוטוזיס עשויות להגביר את השפעת הכימותרפיה הקיימת, במיוחד במחלות עמידות. שנית, סמנים חלבוניים של נויטרופילים, מקרופאגים, תאי T והצגת אנטיגן יכולים לעזור לזהות אילו מטופלים עשויים להרוויח מטיפולים מבוססי חיסון או מאסטרטגיות שילוב. למרות שדרושה אימות נוסף, האטלס הפרוטאומי הזה מציע מפת דרכים להפיכת הביולוגיה המוסתרת של סרקומת איבינג לטיפולים מדויקים וייתכן שגם יעילים יותר עבור מטופלים צעירים.
ציטוט: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
מילות מפתח: סרקומת איבינג, פרוטאומיקה, פרורוטוזיס (ferroptosis), מיקרו‑סביבת הגידול, סרטן בילדות