Clear Sky Science · tr
Ewing sarkomu primer tümörleri ve metastazlarının proteomik haritası
Bu çocukluk çağı kanseri çalışması neden önemli
Ewing sarkomu, çoğunlukla çocukları ve ergenleri etkileyen nadir ama agresif bir kemik kanseridir. Aileler ve hekimler için zorlayıcı bir bilmece vardır: bazı tümörler kemoterapiye iyi yanıt verir ve hastalar iyi bir seyir izlerken, aynı tedavilere rağmen diğerleri nüks eder veya yayılır. Bu çalışma, 74 genç hastadan alınan 170 tümör içindeki gerçek proteinlere alışılmadık derecede derin bir bakış atıyor; bir tümörü diğerinden daha kolay tedavi edilebilir kılan nedir ve vücudun kendi bağışıklık hücreleri hastalığı nasıl şekillendirir sorularını araştırıyor.
Tümörlerin protein düzeyinde incelenmesi
Ewing sarkomu üzerine önceki çalışmaların çoğu, kanserin neler yapabileceğini gösteren DNA ve RNA üzerine odaklandı. Proteinler ise kanserin gerçekte neler yaptığını ortaya koyar. Araştırmacılar, ileri kütle spektrometresi kullanarak her bir tümör örneğinde 10.000’den fazla proteini ölçtüler; örnekler farklı evrelerden alındı: yeni tanı konmuş, kemoterapi sonrası, nüks sırasında ve akciğer veya kemiklere yayılmış metastazlarda. Tümör bölgelerini dikkatle ayırıp yüksek kanser hücresi içeriği için filtreleyerek, bu hastalığın şimdiye kadarki en ayrıntılı protein haritalarından birini oluşturdular. Bu harita, tümörlerin zaman içinde nasıl değiştiğini ve bu değişimlerin tedavi yanıtı ile sağkalım ile nasıl ilişkili olduğunu karşılaştırmaya izin verdi.
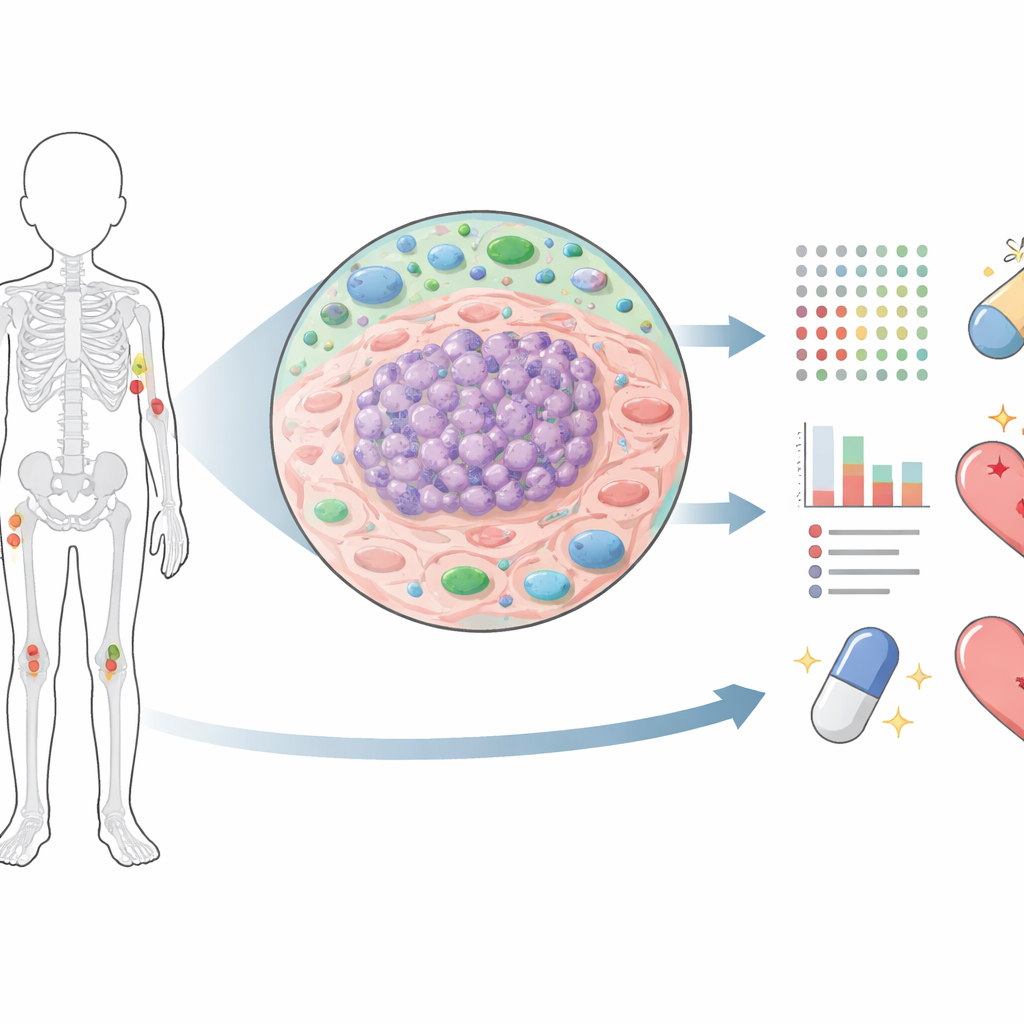
Tedavinin kanseri nasıl yeniden şekillendirdiği
Araştırma ekibi primer tümörleri kemoterapi sonrası alınan örneklerle karşılaştırdığında, protein manzarasında geniş çaplı değişimler gözlendi. Hücre bölünmesi, DNA onarımı ve yeni hücresel yapıların inşasında rol oynayan proteinler tedavi sonrası keskin bir şekilde azaldı; bu, kemoterapinin hızlı bölünen hücreleri geri ittiğiyle uyumlu. Ancak daha sonra nüks eden veya ilerleyen tümörlerde bu aynı proteinlerin birçoğu tekrar yükseldi; bu da hayatta kalan hücrelerin büyüme ve onarım programlarını yeniden aktive ettiğini düşündürüyor. Aynı zamanda, tedavi sonrası tümörlerde bağışıklıkla ilişkili proteinlerin ve düşük oksijen stresinin belirteçlerinin daha yüksek seviyelerde olması, kemoterapinin temiz bir sıfır bırakmaktansa stresli, iltihaplı ama uyum sağlayabilen bir tümör kalıntısı bıraktığını ima ediyor.
Demir, hücre ölümü ve ilaç direnci
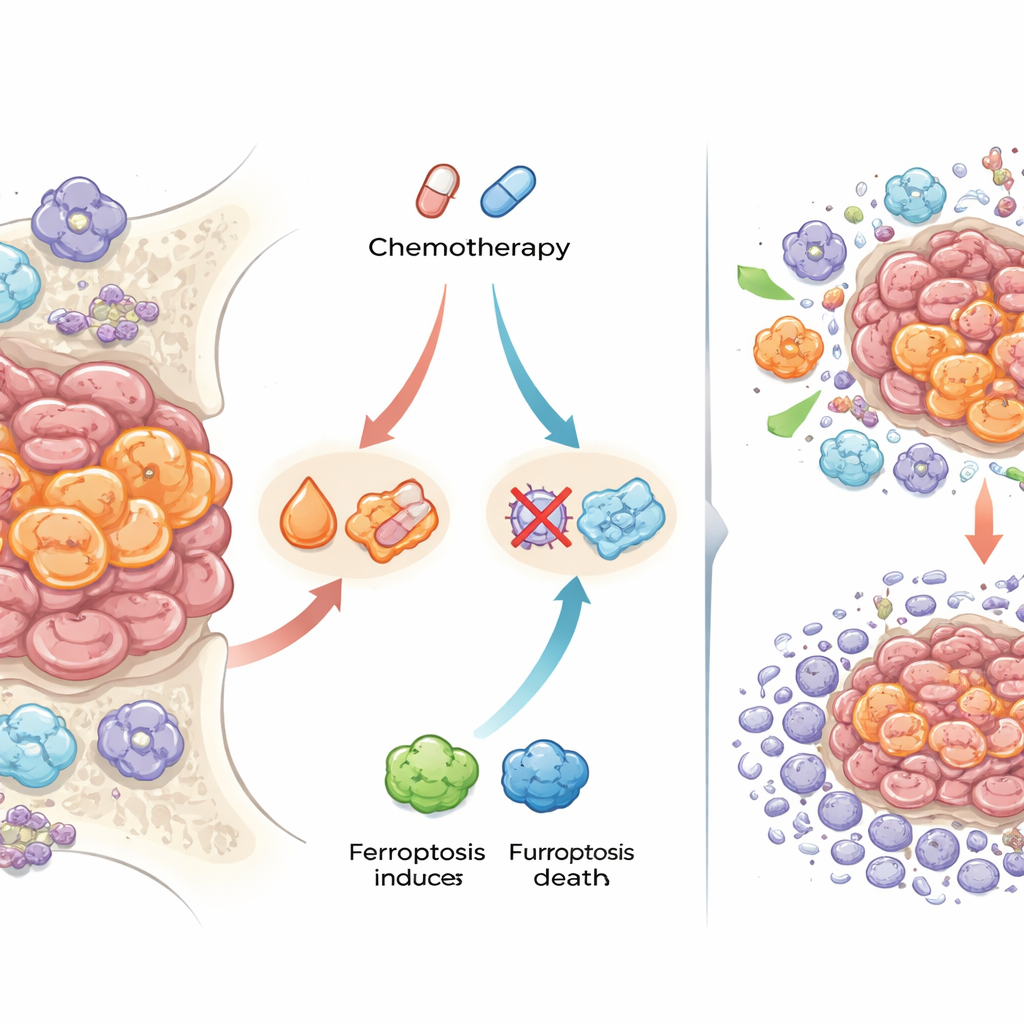
En çarpıcı bulgulardan biri demir taşımaya yönelik proteinler ve ferroptoz adı verilen özel bir hücre ölümü biçimiyle ilgiliydi; bu süreç hücre zarlarına demire bağlı zarar verilmesine dayanır. Kemoterapi sonrası, birçok tümörde kanser hücreleri daha yüksek düzeyde ferritin (demiri depolar) ve transferrin reseptörü (demiri hücre içine alır) taşıdı ve serbest demir birikimleri için pozitif boyama gösterdi. Ayrıca ferroptozu engellediği ve oksidatif hasarı azalttığı bilinen proteinleri de ifade ettiler. Bunun tedavi açısından önemli olup olmadığını test etmek için araştırmacılar, standart ilaçlara dirençli hale getirilmiş Ewing sarkomu hücrelerinden oluşan laboratuvar ortamında yetiştirilen 3B “sferoid” modeller kullandılar. Kemoterapiyi ferroptozu tetikleyen bileşiklerle birleştirdiklerinde, dirençli sferoidler daha hassas hale geldi ve öldürülmek için daha düşük ilaç dozlarına ihtiyaç duydu. Bu, bazı Ewing sarkomu hücrelerinin kemoterapiden tam olarak kurtulmasının nedeni olarak demiri tamponlayıp ferroptotik ölümü önlemeleri olabileceğini düşündürüyor.
Yarar sağlayan ya da zarar veren bağışıklık hücreleri
Tümörler izole büyümediği için ekip, tümör ortamındaki bağışıklık hücrelerinin sonuçla nasıl ilişkili olduğunu da inceledi. Primer tümörleri yalnızca protein desenlerine göre gruplayarak, farklı sağkalım oranlarına sahip üç ana alt sınıf keşfettiler. Yüksek riskli bir grup, birçok hücre döngüsü ve ubiquitin ilişkili protein ile çekirdek proteazom aktivitesinin düşük olması ve nötrofiller ile bağışıklık saldırısını zayıflatabilen “checkpoint” moleküllerinin protein imzalarını gösteriyordu. Daha iyi seyirli bir diğer grup ise tümör parçacıklarını hücre yüzeyinde sunmaya aracılık eden protein düzeylerinin daha yüksek olmasıyla öne çıkıyordu; bu, T hücrelerini etkinleştirmede kilit bir adımdır. Çoklu immünofloresans görüntüleme, kötü sonuçlu gruplardaki tümörlerin nötrofillerce daha zengin, daha iyi sonuçlu gruplardakilerin ise daha fazla makrofaj, T hücresi ve HLA-pozitif antijen sunan hücre içerdiğini doğruladı. Basitçe söylemek gerekirse, “nötrofil ağırlıklı” tümörler genellikle daha kötü seyir gösterirken, daha aktif adaptif bağışıklık hücrelerine sahip tümörler daha iyi seyretme eğilimindeydi.
Gelecekteki tedaviler için ne anlama geliyor
Bir araya getirildiğinde, bu çalışma Ewing sarkomunun tek bir gen hatasından ibaret olmadığını; tedavi baskısı altında değişen, kanser hücreleri, demir metabolizması ve bağışıklık oyuncularından oluşan karmaşık bir ekosistem olduğunu gösteriyor. Hastalar ve klinisyenler için bulgular iki vaat eden fikre işaret ediyor. Birincisi, kanser hücrelerini ferroptoz yönüne iten ilaçlar, özellikle dirençli hastalıkta mevcut kemoterapinin etkinliğini artırabilir. İkincisi, nötrofiller, makrofajlar, T hücreleri ve antijen sunumunun protein temelli belirteçleri, hangi hastaların bağışıklık temelli tedavilerden veya kombinasyon stratejilerinden yararlanabileceğini belirlemede yardımcı olabilir. Daha fazla doğrulamaya ihtiyaç olsa da, bu proteomik atlas Ewing sarkomunun gizli biyolojisini daha kesin ve muhtemelen daha başarılı tedavilere dönüştürmek için bir yol haritası sunuyor.
Atıf: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Anahtar kelimeler: Ewing sarkomu, proteomik, ferroptoz, tümör mikroçevresi, pediatrik kanser