Clear Sky Science · pt
Panorama proteômico de tumores primários e metástases de sarcoma de Ewing
Por que este estudo sobre câncer infantil importa
O sarcoma de Ewing é um câncer ósseo raro, porém agressivo, que atinge principalmente crianças e adolescentes. Famílias e médicos enfrentam um enigma preocupante: alguns tumores respondem bem à quimioterapia e os pacientes evoluem bem, enquanto outros retornam ou se disseminam apesar dos mesmos tratamentos. Este estudo faz uma investigação incomum e profunda das proteínas presentes em 170 tumores de 74 pacientes jovens, perguntando o que torna um tumor mais fácil de tratar do que outro e como as próprias células imunes do corpo moldam a doença.
Olhando dentro dos tumores ao nível das proteínas
A maior parte dos trabalhos anteriores sobre sarcoma de Ewing concentrou-se em DNA e RNA, que nos dizem o que o câncer poderia fazer. As proteínas revelam o que o câncer está realmente fazendo. Os pesquisadores usaram espectrometria de massa avançada para medir mais de 10.000 proteínas em cada amostra tumoral, coletadas de pacientes em diferentes estágios: diagnóstico inicial, após quimioterapia, durante recidiva e em metástases que se espalharam para pulmões ou ossos. Ao dissecar cuidadosamente as regiões tumorais e filtrar por alto conteúdo de células cancerígenas, eles criaram um dos mapas proteômicos mais detalhados dessa doença até hoje. Esse mapa permitiu comparar como os tumores mudam ao longo do tempo e como essas mudanças se relacionam com a resposta ao tratamento e a sobrevida.
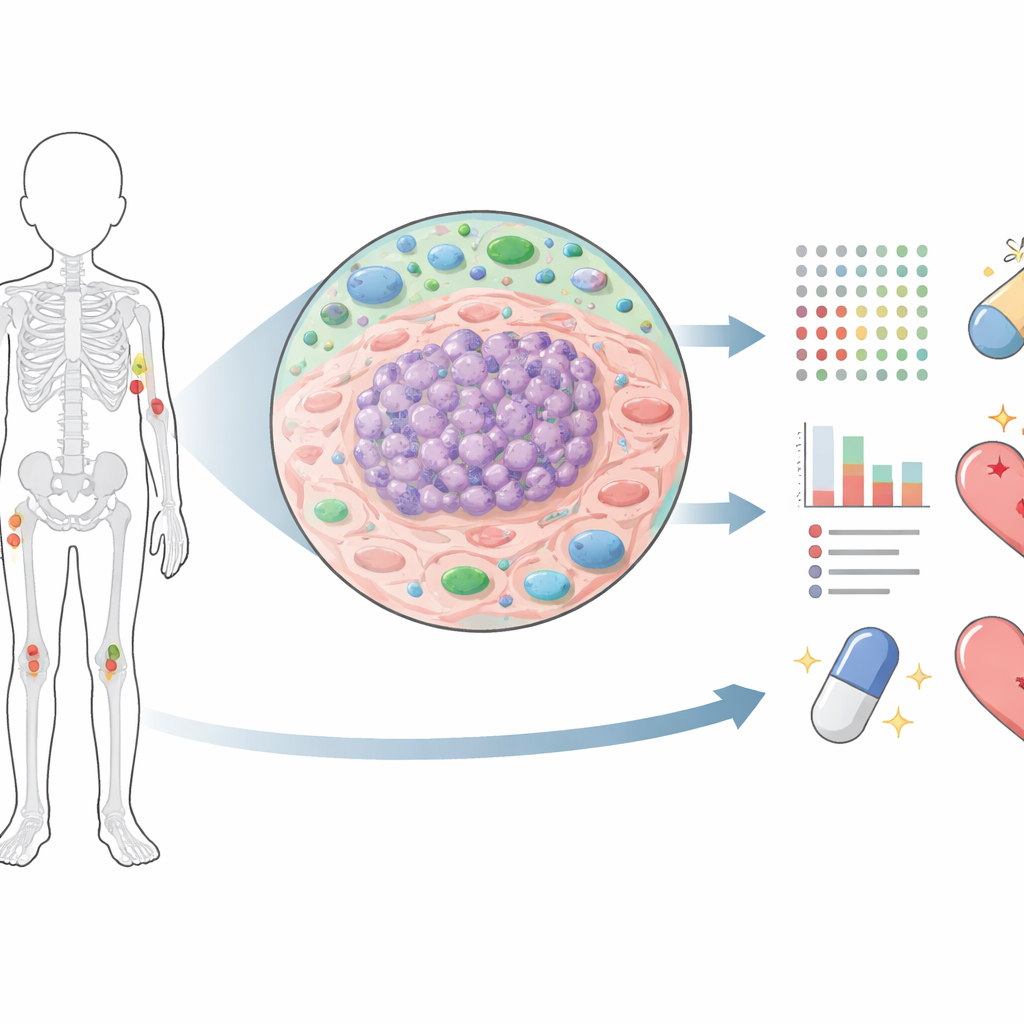
Como o tratamento remodela o câncer
Quando a equipe comparou tumores primários com amostras colhidas após a quimioterapia, observaram mudanças profundas no panorama proteico. Proteínas envolvidas na divisão celular, reparo de DNA e construção de nova maquinaria celular caíram acentuadamente após o tratamento, consistente com a quimioterapia reprimindo células de crescimento rápido. Mas em tumores que depois recidivaram ou progrediram, muitas dessas mesmas proteínas voltaram a subir, sugerindo que as células sobreviventes reativaram programas de crescimento e reparo. Ao mesmo tempo, tumores pós-tratamento mostraram níveis mais altos de proteínas relacionadas à resposta imune e marcadores de estresse por baixa oxigenação, indicando que a quimioterapia pode deixar um remanescente tumoral estressado, inflamado e ainda adaptável, em vez de um ambiente limpo.
Ferro, morte celular e resistência a medicamentos
Uma das descobertas mais marcantes envolveu proteínas que lidam com ferro e uma forma especial de morte celular chamada ferroptose, que depende de danos ao membrana celular mediados por ferro. Após a quimioterapia, células cancerígenas em muitos tumores apresentaram níveis mais altos de ferritina (que armazena ferro) e receptor de transferrina (que importa ferro), e reagiram positivamente para depósitos de ferro livre. Elas também expressaram proteínas conhecidas por bloquear a ferroptose e reduzir danos oxidativos. Para testar se isso tinha impacto no tratamento, os pesquisadores usaram “esferoides” 3D de células de sarcoma de Ewing cultivadas em laboratório e tornadas resistentes a fármacos padrão. Quando combinaram quimioterapia com compostos que induzem ferroptose, os esferoides resistentes tornaram-se mais sensíveis, precisando de doses menores do medicamento para serem eliminados. Isso sugere que algumas células de sarcoma de Ewing podem sobreviver à quimioterapia precisamente porque tamponam o ferro e evitam a morte ferroptótica.
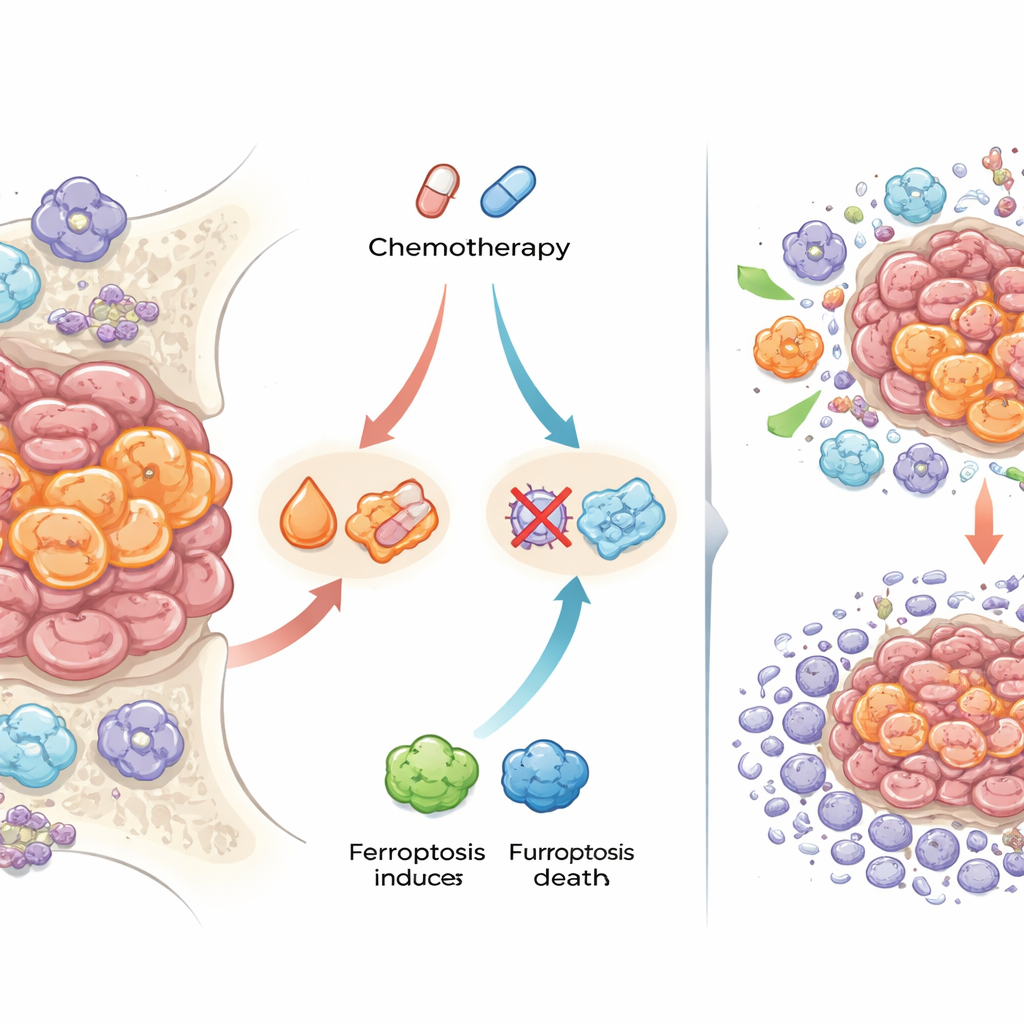
Células imunes que ajudam ou atrapalham
Como os tumores não crescem isoladamente, a equipe também examinou como as células imunes no microambiente tumoral se relacionam com o desfecho. Ao agrupar tumores primários apenas com base em seus padrões proteicos, descobriram três subclasses principais com diferentes taxas de sobrevida. Um grupo de alto risco mostrou muitas proteínas relacionadas ao ciclo celular e à ubiquitinação e baixa atividade do proteassoma central, junto com assinaturas proteicas de neutrófilos e moléculas de “checkpoint” que podem reduzir o ataque imune. Outro grupo, com melhor prognóstico, apresentava níveis mais altos de proteínas envolvidas na apresentação de fragmentos tumorais na superfície celular, um passo crucial para ativar células T. Imagens por imunofluorescência multiplex confirmaram que tumores de grupos de pior prognóstico eram mais ricos em neutrófilos, enquanto aqueles de melhor prognóstico continham mais macrófagos, células T e células apresentadoras de antígeno HLA-positivas. Em termos simples, tumores “ricos em neutrófilos” tendiam a se comportar pior, enquanto tumores com mais células adaptativas engajadas tendiam a se comportar melhor.
O que isso significa para tratamentos futuros
Em conjunto, este trabalho mostra que o sarcoma de Ewing é mais do que um único erro genético; é um ecossistema complexo de células cancerígenas, metabolismo do ferro e atores imunológicos que muda sob a pressão da terapia. Para pacientes e clínicos, as descobertas apontam duas ideias promissoras. Primeiro, fármacos que direcionem as células cancerígenas à ferroptose podem potencializar os efeitos da quimioterapia existente, especialmente em doenças resistentes. Segundo, marcadores proteicos de neutrófilos, macrófagos, células T e apresentação de antígenos poderiam ajudar a identificar quais pacientes podem se beneficiar de terapias baseadas no sistema imune ou de estratégias combinadas. Embora sejam necessárias mais validações, este atlas proteômico oferece um roteiro para transformar a biologia oculta do sarcoma de Ewing em tratamentos mais precisos e, potencialmente, mais eficazes para pacientes jovens.
Citação: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Palavras-chave: Sarcoma de Ewing, proteômica, ferroptose, microambiente tumoral, câncer pediátrico