Clear Sky Science · ru
Протеомный ландшафт первичных опухолей и метастазов саркомы Юинга
Почему это исследование детского рака важно
Саркома Юинга — редкая, но агрессивная опухоль кости, которая в основном поражает детей и подростков. Семьи и врачи сталкиваются с тревожной загадкой: одни опухоли хорошо реагируют на химиотерапию, и пациенты идут на поправку, а другие рецидивируют или метастазируют, несмотря на те же схемы лечения. Это исследование даёт необычно глубокое представление о белках внутри 170 опухолей от 74 юных пациентов, пытаясь выяснить, почему одну опухоль легче лечить, чем другую, и как собственные иммунные клетки организма формируют течение болезни.
Взгляд внутрь опухоли на уровне белков
Большая часть предыдущих работ по саркоме Юинга была сосредоточена на ДНК и РНК, которые показывают, что опухоль может делать. Белки же раскрывают, что опухоль действительно делает. Исследователи использовали продвинутую масс-спектрометрию, чтобы измерить более 10 000 белков в каждой пробе опухоли, взятой у пациентов на разных этапах: при первичной диагностике, после химиотерапии, при рецидиве и в метастазах, распространившихся в лёгкие или кости. Тщательно выделяя регион опухоли и отбирая участки с высоким содержанием раковых клеток, они создали одну из самых детализированных карт белкового состава этого заболевания на сегодняшний день. Эта карта позволила сравнивать, как опухоли меняются со временем и как эти изменения связаны с ответом на лечение и выживаемостью.
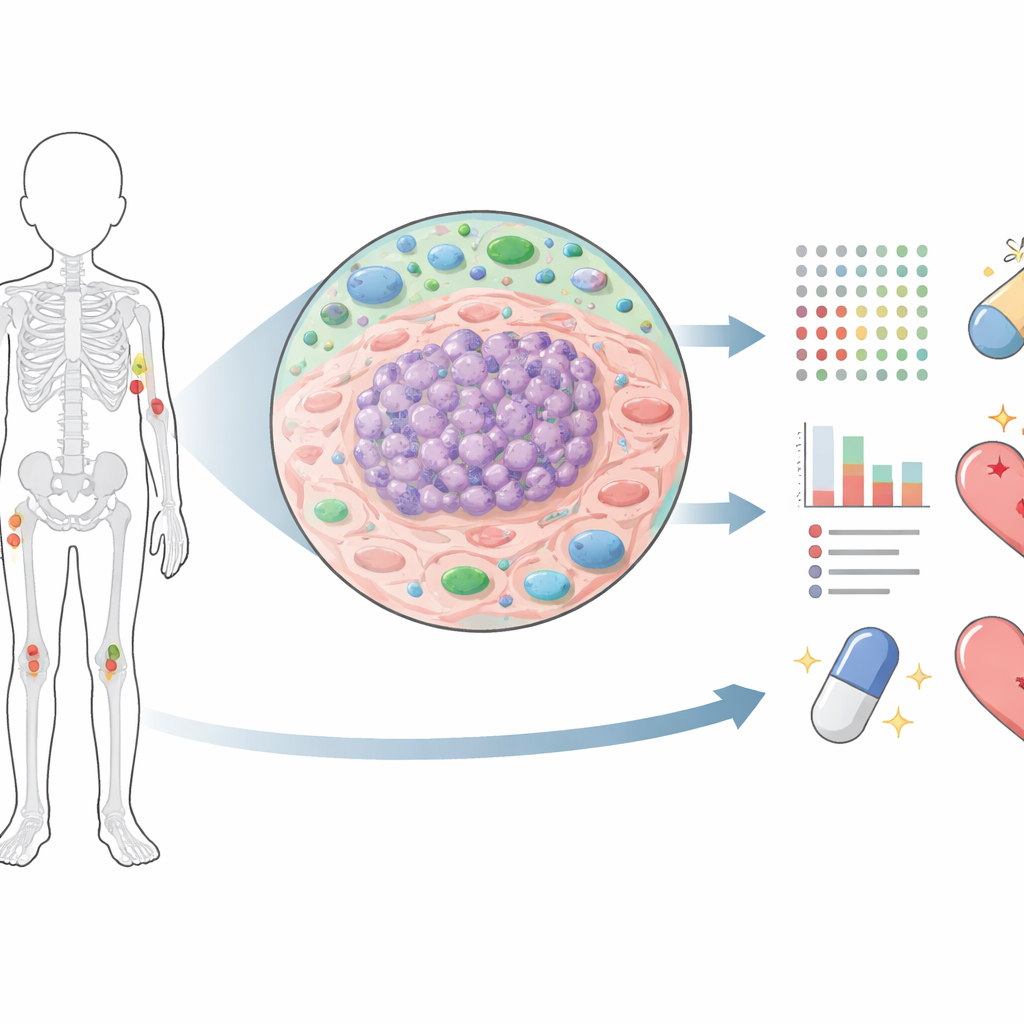
Как лечение перестраивает опухоль
При сравнении первичных опухолей с образцами, взятыми после химиотерапии, команда обнаружила масштабные сдвиги в белковом ландшафте. Белки, вовлечённые в деление клетки, репарацию ДНК и создание новых клеточных структур, резко снижались после лечения, что согласуется с подавлением быстрорастущих клеток химиотерапией. Но в опухолях, которые позже дали рецидив или прогрессировали, многие из этих же белков вновь повышались, что указывает на то, что пережившие клетки реактивировали программы роста и ремонта. Одновременно посттерапевтические опухоли демонстрировали более высокие уровни иммунных белков и маркеров гипоксии, намекая на то, что химиотерапия оставляет после себя стрессовую, воспалённую, но адаптивную остаточную ткань опухоли, а не «чистую доску».
Железо, гибель клеток и лекарственная устойчивость
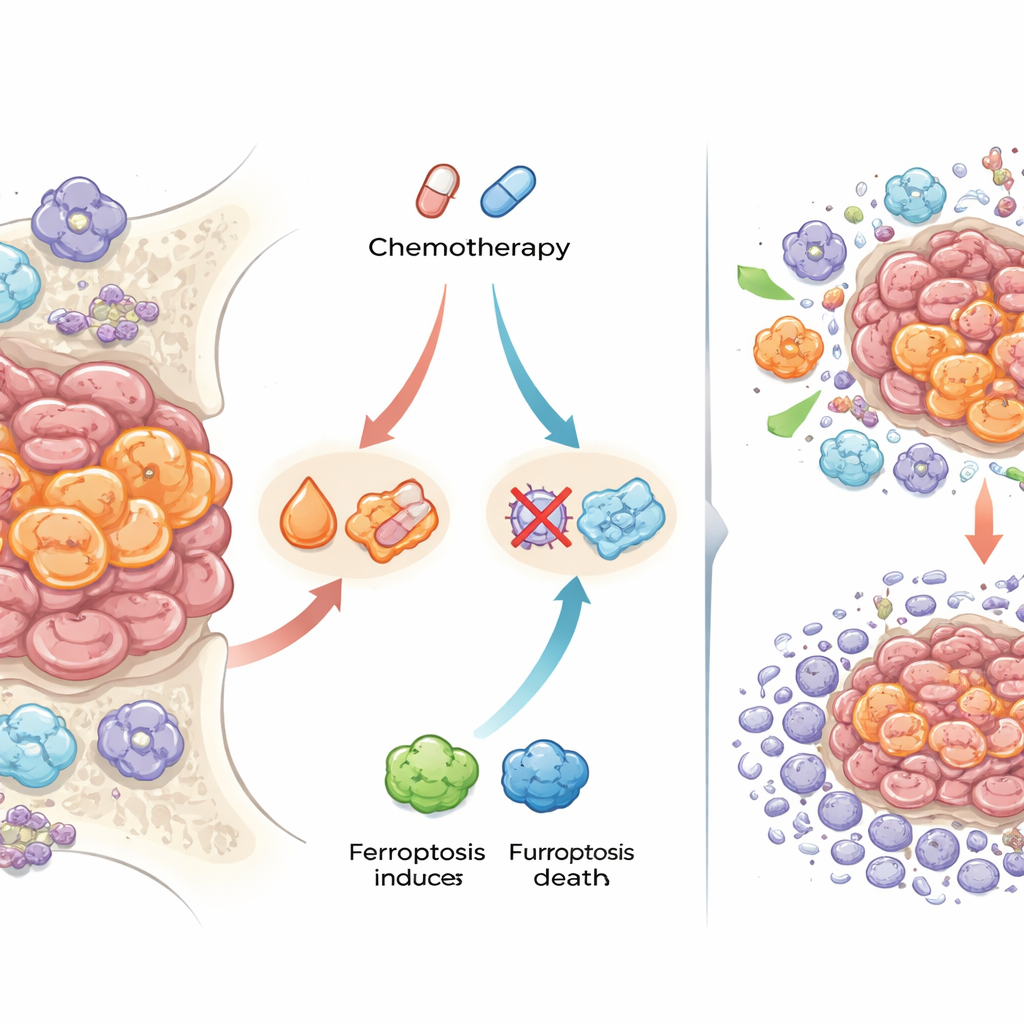
Одно из самых заметных наблюдений касалось белков, работающих с железом, и особой формы клеточной гибели — ферроптоза, зависящей от железосодержащего повреждения мембран. После химиотерапии в многих опухолях раковые клетки содержали повышенные уровни ферритина (белка, который запасает железо) и рецептора трансферрина (ввозящего железо), а также окрашивались на наличие свободных депонированных ионов железа. Они также экспрессировали белки, известные тем, что блокируют ферроптоз и снижают оксидативное повреждение. Чтобы проверить значение этого наблюдения для лечения, исследователи использовали лабораторно выращенные 3D «сфероиды» клеток саркомы Юинга, выведенные устойчивыми к стандартным препаратам. При сочетании химиотерапии с соединениями, запускающими ферроптоз, устойчивые сфероиды становились более чувствительными и требовали меньших доз препарата для гибели. Это указывает на то, что некоторые клетки саркомы Юинга могут выживать после химиотерапии именно потому, что буферизуют железо и избегают ферроптотической гибели.
Иммунные клетки, которые помогают или вредят
Поскольку опухоли не растут в изоляции, команда также изучила, как иммунные клетки в микроокружении опухоли соотносятся с исходом. Группируя первичные опухоли только по их белковым паттернам, они выделили три основные подпопуляции с разной выживаемостью. Одна группа высокого риска характеризовалась множеством белков, связанных с клеточным циклом и убиквитиновой системой, а также пониженной активностью основного протеасома, вместе с белковыми сигнатурами нейтрофилов и «чекпоинтных» молекул, которые могут подавлять иммунную атаку. Другая, с более благоприятным прогнозом, имела более высокие уровни белков, участвующих в презентации фрагментов опухолей на поверхности клетки — ключевом шаге для активации Т-клеток. Мультиплексная иммунофлюоресцентная визуализация подтвердила, что опухоли в группах с плохим прогнозом богаче нейтрофилами, тогда как в группах с лучшим прогнозом встречалось больше макрофагов, Т-клеток и HLA-позитивных антигенпредставляющих клеток. Проще говоря, «нейтрофильно насыщенные» опухоли обычно вели себя хуже, тогда как опухоли с более активными адаптивными иммунными клетками вели себя лучше.
Что это значит для будущего лечения
В совокупности эта работа показывает, что саркома Юинга — это не просто единичная генетическая ошибка; это сложная экосистема раковых клеток, обмена железом и иммунных участников, которая изменяется под давлением терапии. Для пациентов и клиницистов результаты указывают на две многообещающие идеи. Во-первых, препараты, направленные на сдвиг раковых клеток в сторону ферроптоза, могут усилить эффекты существующей химиотерапии, особенно при устойчивой болезни. Во-вторых, белковые маркеры нейтрофилов, макрофагов, Т-клеток и презентации антигенов могли бы помочь выявлять пациентов, которые выиграют от иммунотерапии или комбинированных стратегий. Хотя требуется дальнейшая валидация, этот протеомный атлас предлагает карту для превращения скрытой биологии саркомы Юинга в более точные и, возможно, более успешные методы лечения для молодых пациентов.
Цитирование: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Ключевые слова: саркома Юинга, протеомика, ферроптоз, микроокружение опухоли, детский рак