Clear Sky Science · nl
Proteomische kaart van primaire tumoren en metastasen bij Ewing-sarcoom
Waarom deze studie naar kinderonkologie ertoe doet
Ewing-sarcoom is een zeldzame maar agressieve botkanker die vooral kinderen en tieners treft. Familieleden en artsen staan voor een lastig raadsel: sommige tumoren reageren goed op chemotherapie en patiënten herstellen, terwijl andere tumoren terugkeren of uitzaaien ondanks dezelfde behandelingen. Deze studie kijkt uitzonderlijk diep naar de daadwerkelijke eiwitten in 170 tumoren van 74 jonge patiënten en onderzoekt wat een tumor gemakkelijker behandelbaar maakt dan een andere en hoe de eigen immuuncellen van het lichaam de ziekte vormen.
In tumoren kijken op eiwitniveau
Het merendeel van eerder onderzoek naar Ewing-sarcoom richtte zich op DNA en RNA, die aangeven wat de kanker zou kunnen doen. Eiwitten tonen wat de kanker daadwerkelijk doet. De onderzoekers gebruikten geavanceerde massaspectrometrie om meer dan 10.000 eiwitten in elk tumormonster te meten, genomen bij patiënten in verschillende stadia: bij de diagnose, na chemotherapie, tijdens terugval en in metastasen die naar longen of botten waren uitgezaaid. Door tumorregio’s zorgvuldig te disseceren en te filteren op een hoog aandeel kankercellen, creëerden ze een van de meest gedetailleerde eiwitkaarten van deze ziekte tot nu toe. Deze kaart stelde hen in staat te vergelijken hoe tumoren in de loop van de tijd veranderen en hoe die veranderingen samenhangen met behandelrespons en overleving.
Hoe behandeling de kanker hervormt
Toen het team primaire tumoren vergeleek met monsters na chemotherapie, zagen ze ingrijpende verschuivingen in het eiwitlandschap. Eiwitten die betrokken zijn bij celdeling, DNA-herstel en het aanmaken van nieuw cellulair materiaal daalden sterk na behandeling, wat consistent is met chemotherapie die snel delende cellen onderdrukt. Maar in tumoren die later terugkeerden of vooruitgingen, stegen veel van diezelfde eiwitten weer, wat suggereert dat overlevende cellen groeivoorzieningen en herstelprogramma’s opnieuw activeerden. Tegelijkertijd vertoonden post-behandelings tumoren hogere niveaus van immuun-gerelateerde eiwitten en merkers van zuurstofgebrek, wat erop wijst dat chemotherapie een gestrest, ontstoken maar aanpasbaar tumorrestant achterlaat in plaats van een schone lei.
IJzer, celdood en medicijnresistentie
Een van de meest opvallende bevindingen betrof eiwitten die met ijzer omgaan en een bijzondere vorm van celdood genaamd ferroptose, die afhankelijk is van ijzer-gedreven schade aan celmembranen. Na chemotherapie hadden kankercellen in veel tumoren hogere niveaus van ferritine (het opslag-eiwit voor ijzer) en transferrinereceptor (die ijzer opneemt), en kleurden ze positief voor vrije ijzerafzettingen. Ze brachten ook eiwitten tot expressie die bekendstaan om ferroptose te blokkeren en oxidatieve schade te verminderen. Om te testen of dit relevant was voor de behandeling, gebruikten de onderzoekers in het laboratorium gekweekte 3D ‘spheroïden’ van Ewing-sarcoomcellen die resistent waren gemaakt tegen standaardmedicijnen. Wanneer ze chemotherapie combineerden met verbindingen die ferroptose opwekken, werden de resistente spheroïden gevoeliger en waren lagere doses medicijn nodig om ze te doden. Dit suggereert dat sommige Ewing-sarcoomcellen chemotherapie kunnen overleven doordat ze ijzer bufferen en ferroptotische celdood vermijden.
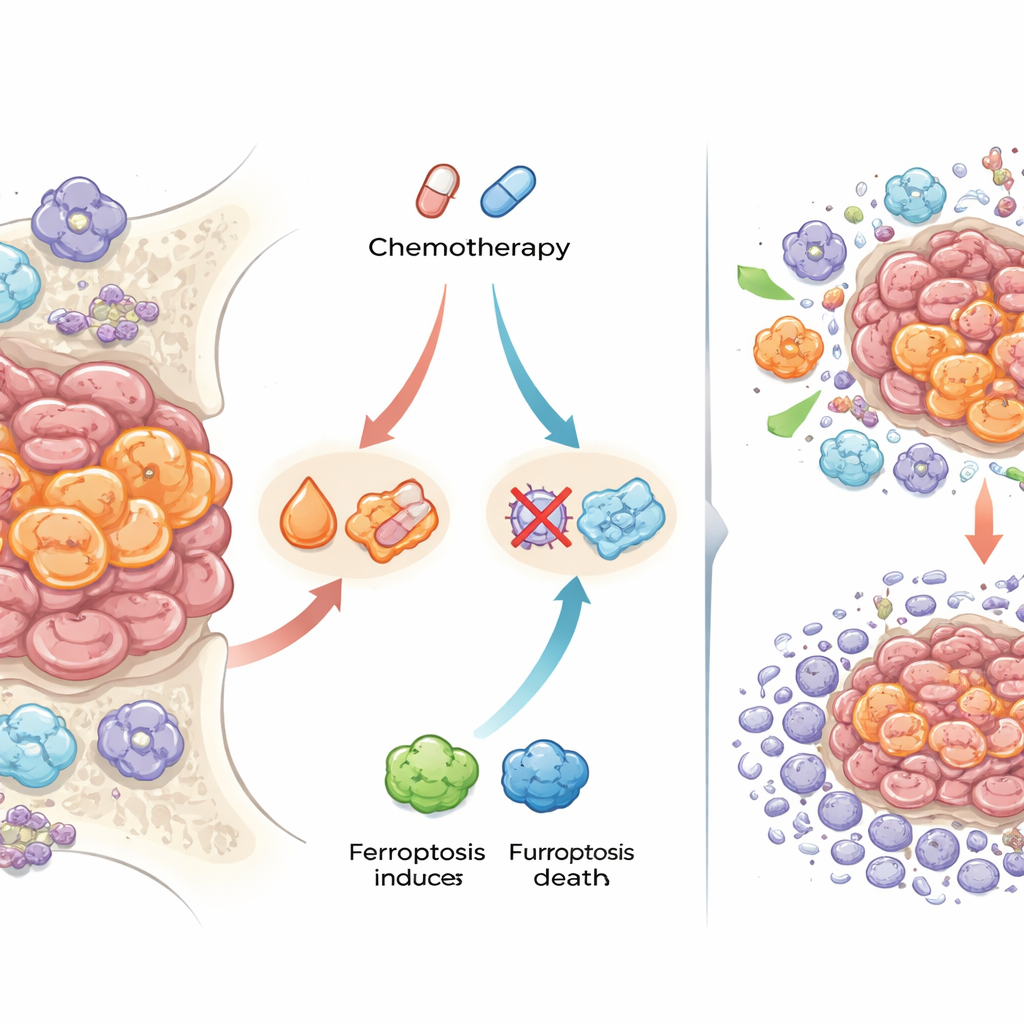
Immuuncellen die helpen of schaden
Aangezien tumoren niet in isolatie groeien, onderzocht het team ook hoe immuuncellen binnen de tumoromgeving samenhangen met uitkomst. Door primaire tumoren alleen te groeperen op basis van hun eiwitpatronen ontdekten ze drie hoofdsubklassen met verschillende overlevingskansen. Eén hoogrisicogroep toonde veel eiwitten gerelateerd aan celcyclus en ubiquitinering en lage activiteit van het kernproteasoom, samen met eiwitsignaturen van neutrofielen en ‘checkpoint’-moleculen die immuunaanvallen kunnen dempen. Een andere, gunstiger groep had hogere niveaus van eiwitten die betrokken zijn bij het presenteren van tumorfragmenten op het celoppervlak, een cruciale stap voor activatie van T-cellen. Multiplex immunofluorescentie-imaging bevestigde dat tumoren in de slechte-uitkomstgroepen rijker waren aan neutrofielen, terwijl die in de betere-uitkomstgroepen meer macrofagen, T-cellen en HLA-positieve antigeenpresenterende cellen bevatten. Simpel gezegd: ‘neutrofiel-rijke’ tumoren gedroegen zich meestal slechter, terwijl tumoren met meer betrokken adaptieve immuuncellen geneigd waren het beter te doen.
Wat dit betekent voor toekomstige behandeling
Samengevoegd laat dit werk zien dat Ewing-sarcoom meer is dan een enkele genetische fout; het is een complex ecosysteem van kankercellen, ijzermetabolisme en immuuncomponenten dat verschuift onder de druk van therapie. Voor patiënten en clinici wijzen de bevindingen op twee veelbelovende ideeën. Ten eerste zouden middelen die kankercellen naar ferroptose duwen de effecten van bestaande chemotherapie kunnen versterken, vooral bij resistent ziekteverloop. Ten tweede zouden eiwitgebaseerde merkers van neutrofielen, macrofagen, T-cellen en antigeenpresentatie kunnen helpen bepalen welke patiënten baat hebben bij immuun- gebaseerde therapieën of combinatiestrategieën. Hoewel meer bevestiging nodig is, biedt deze proteomische atlas een routekaart om de verborgen biologie van Ewing-sarcoom te vertalen naar meer gerichte en mogelijk succesvollere behandelingen voor jonge patiënten.
Bronvermelding: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Trefwoorden: Ewing-sarcoom, proteomica, ferroptose, tumormicro-omgeving, pediatrische kanker