Clear Sky Science · it
Paesaggio proteomico dei tumori primari e delle metastasi del sarcoma di Ewing
Perché questo studio sul cancro infantile è importante
Il sarcoma di Ewing è un tumore osseo raro ma aggressivo che colpisce prevalentemente bambini e adolescenti. Famiglie e medici affrontano un rompicapo inquietante: alcuni tumori rispondono bene alla chemioterapia e i pazienti guariscono, mentre altri recidivano o si diffondono nonostante gli stessi trattamenti. Questo studio offre un’analisi particolarmente approfondita delle proteine presenti in 170 campioni tumorali provenienti da 74 giovani pazienti, cercando di capire cosa rende un tumore più facile da trattare rispetto a un altro e come le cellule immunitarie dell’organismo influenzino la malattia.
Esaminare i tumori a livello proteico
La maggior parte dei lavori precedenti sul sarcoma di Ewing si è concentrata su DNA e RNA, che indicano cosa il cancro potrebbe fare. Le proteine invece rivelano cosa il cancro sta effettivamente facendo. I ricercatori hanno usato spettrometria di massa avanzata per misurare oltre 10.000 proteine in ciascun campione tumorale, prelevato da pazienti in diverse fasi: alla diagnosi, dopo la chemioterapia, durante la recidiva e nelle metastasi polmonari o ossee. Dissecando con cura le regioni tumorali e selezionando campioni con alto contenuto di cellule tumorali, hanno creato una delle mappe proteiche più dettagliate di questa malattia fino ad oggi. Questa mappa ha permesso di confrontare come i tumori cambiano nel tempo e come tali cambiamenti si relazionano alla risposta terapeutica e alla sopravvivenza.
Come il trattamento rimodella il cancro
Confrontando i tumori primari con i campioni prelevati dopo la chemioterapia, il team ha osservato grandi cambiamenti nel paesaggio proteico. Le proteine coinvolte nella divisione cellulare, nella riparazione del DNA e nell’allestimento di nuovi apparati cellulari sono diminuite bruscamente dopo il trattamento, coerentemente con l’effetto della chemioterapia sulle cellule a rapida proliferazione. Tuttavia, nei tumori che successivamente recidivavano o progredivano, molte di queste stesse proteine sono aumentate di nuovo, suggerendo che le cellule sopravvissute riattivano programmi di crescita e riparazione. Allo stesso tempo, i tumori post-trattamento mostravano livelli più elevati di proteine correlate all’immunità e marcatori di stress ipossico, indicando che la chemioterapia lascia dietro di sé un residuo tumorale stressato, infiammato ma adattabile, più che una pulizia completa.
Ferro, morte cellulare e resistenza ai farmaci
Uno dei risultati più rilevanti riguarda le proteine che modulano il ferro e una forma di morte cellulare chiamata ferroptosi, che dipende dal danno al comparto lipidico mediato dal ferro. Dopo la chemioterapia, molte cellule tumorali presentavano livelli più alti di ferritina (che immagazzina il ferro) e del recettore per la transferrina (che importa il ferro), e mostravano depositi di ferro libero alla colorazione. Espressi erano anche fattori noti per bloccare la ferroptosi e ridurre il danno ossidativo. Per verificare se questo fosse rilevante per il trattamento, i ricercatori hanno usato sfere 3D di cellule di sarcoma di Ewing coltivate in laboratorio e rese resistenti ai farmaci standard. Combinando la chemioterapia con composti che inducono la ferroptosi, le sfere resistenti sono diventate più sensibili, richiedendo dosi minori di farmaco per essere uccise. Ciò suggerisce che alcune cellule del sarcoma di Ewing possono sopravvivere alla chemioterapia proprio perché tamponano il ferro ed evitano la morte ferroptotica.
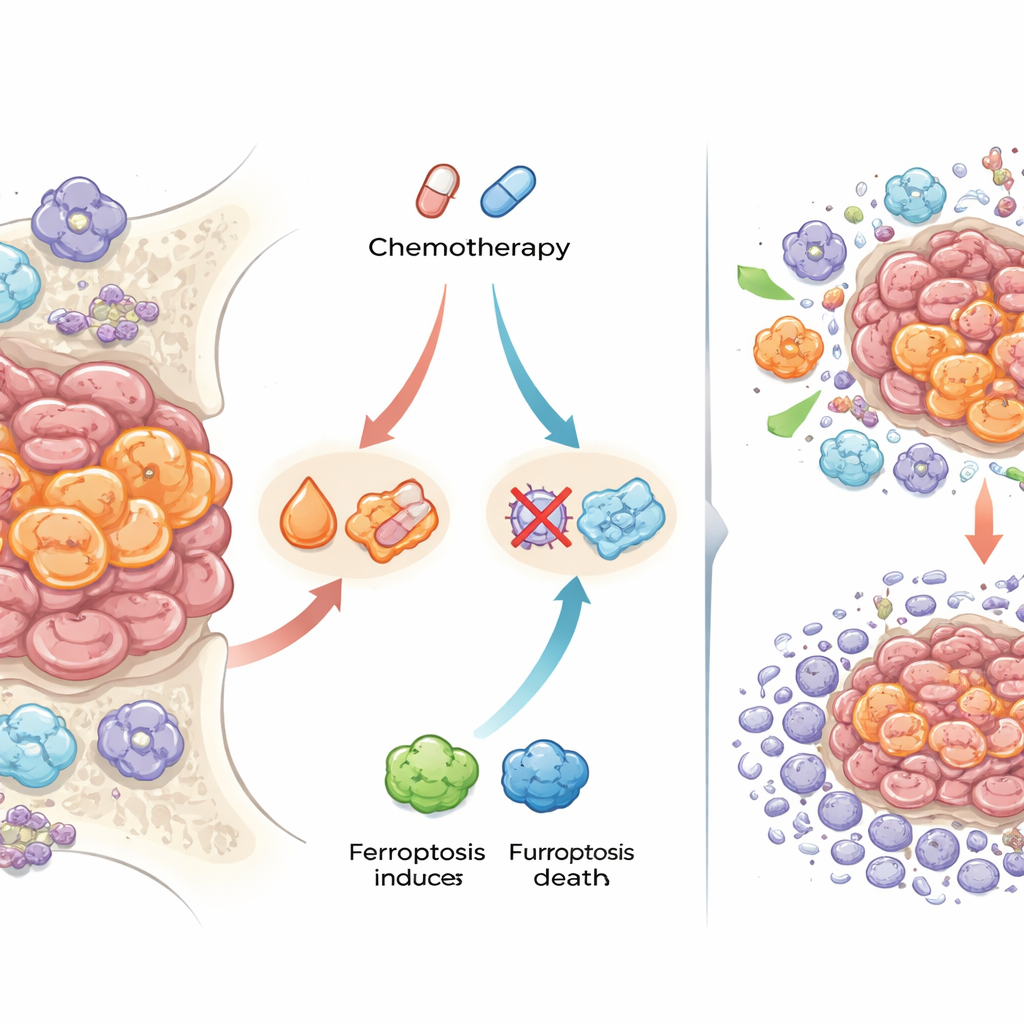
Cellule immunitarie che aiutano o danneggiano
Poiché i tumori non crescono in isolamento, il team ha esaminato anche come le cellule immunitarie presenti nel microambiente tumorale si correlino all’esito. Raggruppando i tumori primari basandosi solo sui loro modelli proteici, hanno identificato tre sottoclassi principali con differenti tassi di sopravvivenza. Un gruppo ad alto rischio mostrava molte proteine legate al ciclo cellulare e all’ubiquitina e una bassa attività del proteasoma core, insieme a firme proteiche di neutrofili e molecole checkpoint che possono attenuare l’attacco immunitario. Un altro gruppo, con prognosi migliore, presentava livelli più elevati di proteine coinvolte nella presentazione di frammenti tumorali sulla superficie cellulare, passo chiave per l’attivazione delle cellule T. L’imaging immunofluorescente multiplex ha confermato che i tumori dei gruppi con esito peggiore erano più ricchi di neutrofili, mentre quelli con esito migliore contenevano più macrofagi, cellule T e cellule presentanti antigene HLA-positive. In termini semplici, i tumori “ricchi di neutrofili” tendevano ad avere un comportamento clinico peggiore, mentre quelli con una maggiore presenza di cellule adattative impegnate tendevano ad avere un comportamento migliore.
Cosa significa per i trattamenti futuri
Complessivamente, questo lavoro dimostra che il sarcoma di Ewing non è solo un singolo errore genetico; è un ecosistema complesso di cellule tumorali, metabolismo del ferro e componenti immunitarie che si rimodella sotto la pressione della terapia. Per pazienti e clinici, i risultati indicano due idee promettenti. Primo, farmaci che spingono le cellule tumorali verso la ferroptosi potrebbero potenziare l’effetto della chemioterapia esistente, specialmente nelle malattie resistenti. Secondo, marcatori proteici di neutrofili, macrofagi, linfociti T e presentazione antigene potrebbero aiutare a identificare quali pazienti potrebbero beneficiare di terapie immunitarie o di strategie combinate. Pur necessitando di ulteriori validazioni, questa mappa proteomica offre una guida per trasformare la biologia nascosta del sarcoma di Ewing in terapie più precise e potenzialmente più efficaci per i pazienti giovani.
Citazione: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Parole chiave: Sarcoma di Ewing, proteomica, ferroptosi, microambiente tumorale, cancro pediatrico