Clear Sky Science · es
Panorama proteómico de los tumores primarios y las metástasis del sarcoma de Ewing
Por qué importa este estudio sobre un cáncer infantil
El sarcoma de Ewing es un cáncer óseo poco frecuente pero agresivo que afecta principalmente a niños y adolescentes. Familias y médicos se enfrentan a un rompecabezas preocupado: algunos tumores responden bien a la quimioterapia y los pacientes evolucionan favorablemente, mientras que otros reaparecen o hacen metástasis pese a recibir los mismos tratamientos. Este estudio realiza un examen inusualmente profundo de las proteínas reales dentro de 170 tumores procedentes de 74 pacientes jóvenes, preguntando qué hace que un tumor sea más fácil de tratar que otro y cómo las propias células inmunitarias del organismo moldean la enfermedad.
Mirando dentro de los tumores a nivel proteico
La mayor parte de los trabajos previos sobre el sarcoma de Ewing se ha centrado en el ADN y el ARN, que nos dicen qué podría hacer el cáncer. Las proteínas revelan qué está haciendo realmente. Los investigadores emplearon espectrometría de masas avanzada para medir más de 10.000 proteínas en cada muestra tumoral, tomadas de pacientes en diferentes estadios: recién diagnosticados, tras la quimioterapia, durante la recaída y en metástasis que se habían diseminado a pulmón o hueso. Al diseccionar cuidadosamente las regiones tumorales y filtrar por alto contenido de células cancerosas, crearon uno de los mapas proteómicos más detallados de esta enfermedad hasta la fecha. Este mapa les permitió comparar cómo cambian los tumores con el tiempo y cómo esos cambios se relacionan con la respuesta al tratamiento y la supervivencia.
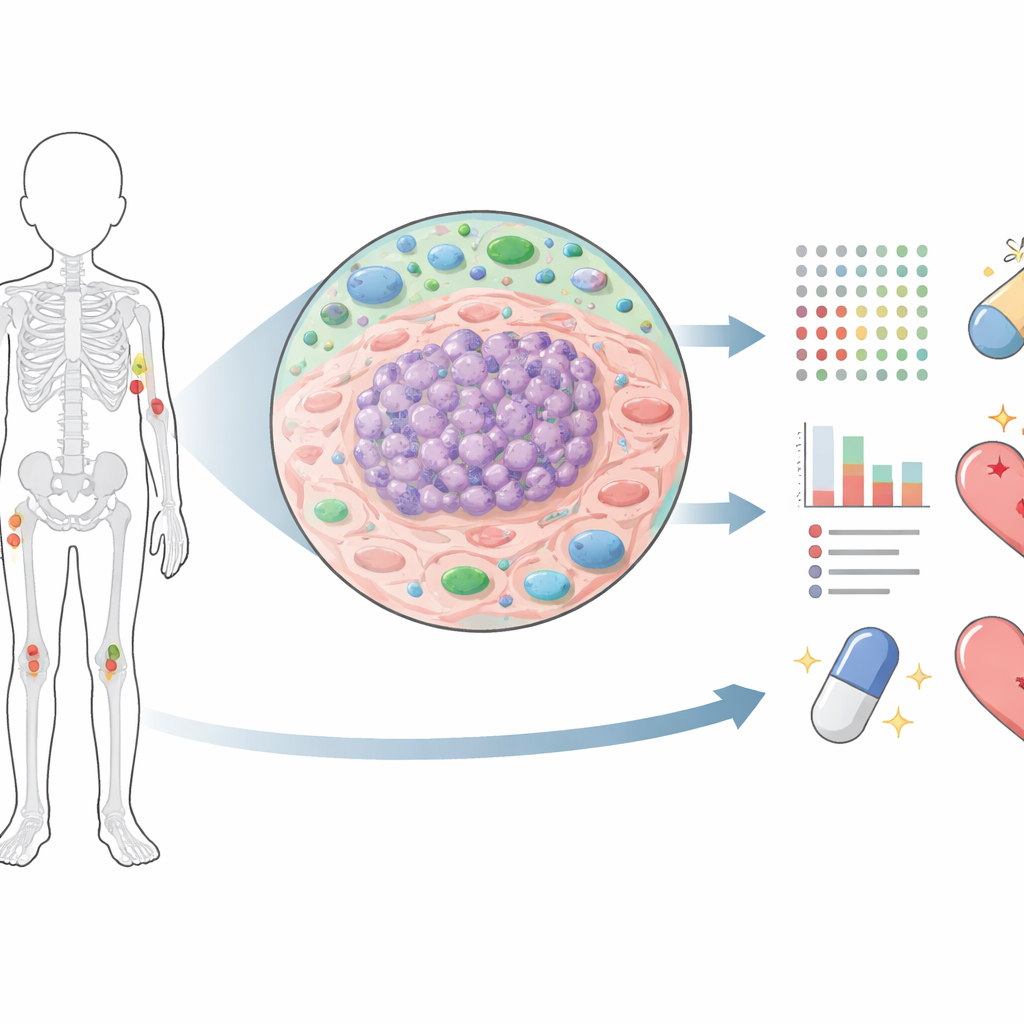
Cómo el tratamiento remodela el cáncer
Al comparar los tumores primarios con muestras tomadas tras la quimioterapia, el equipo observó cambios drásticos en el paisaje proteico. Las proteínas implicadas en la división celular, la reparación del ADN y la construcción de nueva maquinaria celular disminuyeron notablemente después del tratamiento, coherente con que la quimioterapia reduce las células de rápido crecimiento. Pero en los tumores que luego recidivaron o progresaron, muchas de esas mismas proteínas volvieron a elevarse, lo que sugiere que las células supervivientes reactivaron programas de crecimiento y reparación. Al mismo tiempo, los tumores posratamiento mostraron niveles más altos de proteínas relacionadas con la inmunidad y marcadores de estrés por hipoxia, lo que insinúa que la quimioterapia deja un remanente tumoral estresado, inflamado y aún adaptable en lugar de una limpieza total.
Hierro, muerte celular y resistencia a fármacos
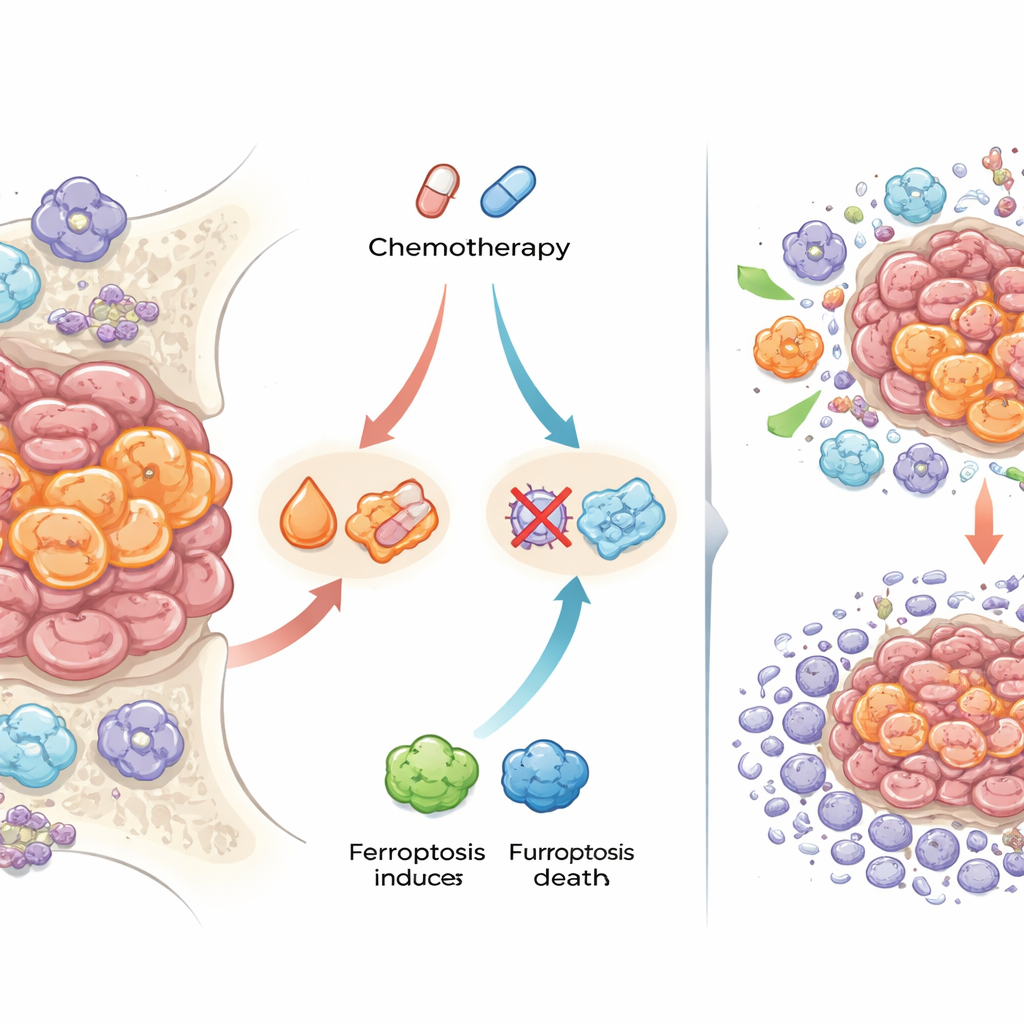
Uno de los hallazgos más llamativos implicó proteínas del manejo del hierro y una forma especial de muerte celular llamada ferroptosis, que depende del daño a las membranas celulares impulsado por el hierro. Tras la quimioterapia, las células cancerosas en muchos tumores presentaron niveles más altos de ferritina (que almacena hierro) y del receptor de transferrina (que importa hierro), y tiñeron positivamente por depósitos de hierro libre. También expresaron proteínas conocidas por bloquear la ferroptosis y reducir el daño oxidativo. Para comprobar si esto tenía trascendencia para el tratamiento, los investigadores usaron esferoides 3D de células de sarcoma de Ewing cultivadas en laboratorio que se habían hecho resistentes a fármacos estándar. Cuando combinaron la quimioterapia con compuestos que inducen ferroptosis, los esferoides resistentes se volvieron más sensibles, precisando dosis más bajas de fármaco para ser eliminados. Esto sugiere que algunas células del sarcoma de Ewing pueden sobrevivir a la quimioterapia precisamente porque regulan el hierro y evitan la muerte por ferroptosis.
Células inmunitarias que ayudan o perjudican
Puesto que los tumores no crecen en aislamiento, el equipo también examinó cómo las células inmunitarias dentro del microambiente tumoral se relacionan con el resultado. Al agrupar los tumores primarios únicamente según sus patrones proteicos, descubrieron tres grandes subclases con tasas de supervivencia diferentes. Un grupo de alto riesgo mostró muchas proteínas relacionadas con el ciclo celular y la ubiquitinación y baja actividad del proteasoma central, junto con firmas proteicas de neutrófilos y moléculas de 'checkpoint' que pueden atenuar el ataque inmune. Otro grupo, con mejor pronóstico, presentó mayores niveles de proteínas implicadas en la presentación de fragmentos tumorales en la superficie celular, un paso clave para activar a las células T. La imagen por inmunofluorescencia multiplex confirmó que los tumores de los grupos de peor pronóstico eran más ricos en neutrófilos, mientras que los de mejor pronóstico contenían más macrófagos, células T y células presentadoras de antígeno positivas para HLA. En términos sencillos, los tumores 'ricos en neutrófilos' tendieron a comportarse peor, mientras que los tumores con más células inmunitarias adaptativas activas tendieron a comportarse mejor.
Qué significa esto para tratamientos futuros
En conjunto, este trabajo muestra que el sarcoma de Ewing es más que un único error genético; es un ecosistema complejo de células cancerosas, metabolismo del hierro y actores inmunitarios que cambia bajo la presión de la terapia. Para pacientes y clínicos, los hallazgos apuntan a dos ideas prometedoras. Primero, fármacos que empujen a las células cancerosas hacia la ferroptosis podrían potenciar los efectos de la quimioterapia existente, especialmente en enfermedades resistentes. Segundo, marcadores basados en proteínas de neutrófilos, macrófagos, células T y presentación de antígeno podrían ayudar a identificar qué pacientes podrían beneficiarse de terapias basadas en el sistema inmune o de estrategias combinadas. Aunque se necesita más validación, este atlas proteómico ofrece una hoja de ruta para convertir la biología oculta del sarcoma de Ewing en tratamientos más precisos y, potencialmente, más eficaces para pacientes jóvenes.
Cita: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Palabras clave: Sarcoma de Ewing, proteómica, ferroptosis, microambiente tumoral, cáncer pediátrico