Clear Sky Science · de
Proteomische Landschaft von Ewing‑Sarkom Primärtumoren und Metastasen
Warum diese Studie zu Kinderkrebs wichtig ist
Das Ewing‑Sarkom ist ein seltener, aber aggressiver Knochentumor, der vor allem Kinder und Jugendliche trifft. Familien und Ärzte stehen vor einem beunruhigenden Rätsel: Manche Tumoren sprechen gut auf Chemotherapie an und die Patienten erholen sich, während andere trotz gleicher Behandlung wiederkehren oder metastasieren. Diese Studie wirft einen ungewöhnlich tiefen Blick auf die tatsächlichen Proteine in 170 Tumoren von 74 jungen Patientinnen und Patienten und fragt, was einen Tumor leichter behandelbar macht als einen anderen und wie körpereigene Immunzellen die Krankheit formen.
Blick in Tumoren auf Proteinebene
Die meisten früheren Arbeiten am Ewing‑Sarkom konzentrierten sich auf DNA und RNA, die zeigen, was der Krebs tun könnte. Proteine offenbaren, was der Krebs tatsächlich tut. Die Forschenden nutzten hochentwickelte Massenspektrometrie, um in jeder Tumorprobe mehr als 10.000 Proteine zu messen, entnommen von Patientinnen und Patienten in unterschiedlichen Stadien: bei Erstdiagnose, nach Chemotherapie, bei Rückfall und in Metastasen in Lunge oder Knochen. Durch sorgfältige Präparation der Tumorregionen und Filterung nach hohem Anteil an Krebszellen schufen sie eine der bisher detailliertesten Proteinkarten dieser Erkrankung. Diese Karte ermöglichte Vergleiche, wie Tumoren sich im Verlauf verändern und wie diese Veränderungen mit Therapierespons und Überleben zusammenhängen.
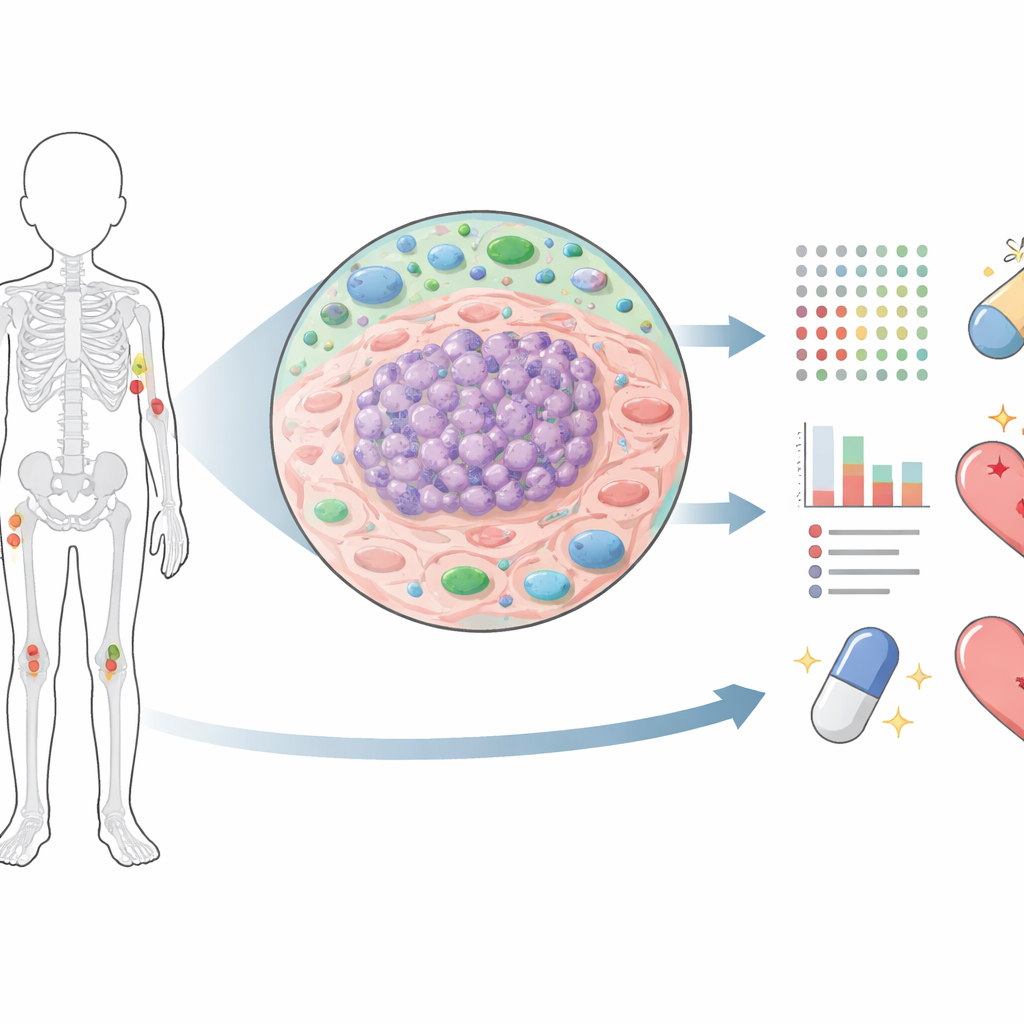
Wie Behandlung den Krebs umgestaltet
Beim Vergleich von Primärtumoren mit Proben nach Chemotherapie beobachtete das Team weitreichende Verschiebungen im Proteom. Proteine, die an Zellteilung, DNA‑Reparatur und Aufbau neuer zellulärer Maschinerie beteiligt sind, nahmen nach der Behandlung stark ab, was mit der Wirkung der Chemotherapie auf schnell teilende Zellen übereinstimmt. In Tumoren, die später rückfällig wurden oder fortschritten, stiegen viele dieser Proteine jedoch wieder an, was darauf hindeutet, dass überlebende Zellen Wachstums‑ und Reparaturprogramme reaktivieren. Gleichzeitig zeigten posttherapeutische Tumoren erhöhte Mengen an immunbezogenen Proteinen und Markern für Sauerstoffmangelstress, was darauf hindeutet, dass die Chemotherapie eher ein gestresstes, entzündetes und anpassungsfähiges Tumorrestgewebe hinterlässt als eine saubere Fläche.
Eisen, Zellsterben und Medikamentenresistenz
Eines der auffälligsten Ergebnisse betraf Eisen‑handhabende Proteine und eine besondere Form des Zelltods namens Ferroptose, die von eisengetriebener Schädigung der Zellmembran abhängt. Nach der Chemotherapie wiesen Krebszellen in vielen Tumoren höhere Spiegel von Ferritin (Eisenspeicherung) und Transferrinrezeptor (Eisenaufnahme) auf und zeigten positive Färbungen für freie Eisenablagerungen. Sie exprimierten außerdem Proteine, die bekannt sind dafür, Ferroptose zu blockieren und oxidative Schäden zu vermindern. Um die Bedeutung dafür für die Therapie zu prüfen, verwendeten die Forschenden im Labor gezüchtete 3D‑„Sphäroide“ von Ewing‑Sarkomzellen, die gegen Standardmedikamente resistent gemacht worden waren. Kombinierten sie Chemotherapie mit Verbindungen, die Ferroptose auslösen, wurden die resistenten Sphäroide wieder empfindlicher und benötigten niedrigere Wirkstoffdosen, um abgetötet zu werden. Das deutet darauf hin, dass einige Ewing‑Sarkomzellen Chemotherapie überleben, weil sie Eisen puffern und so ferroptotischen Zelltod vermeiden.
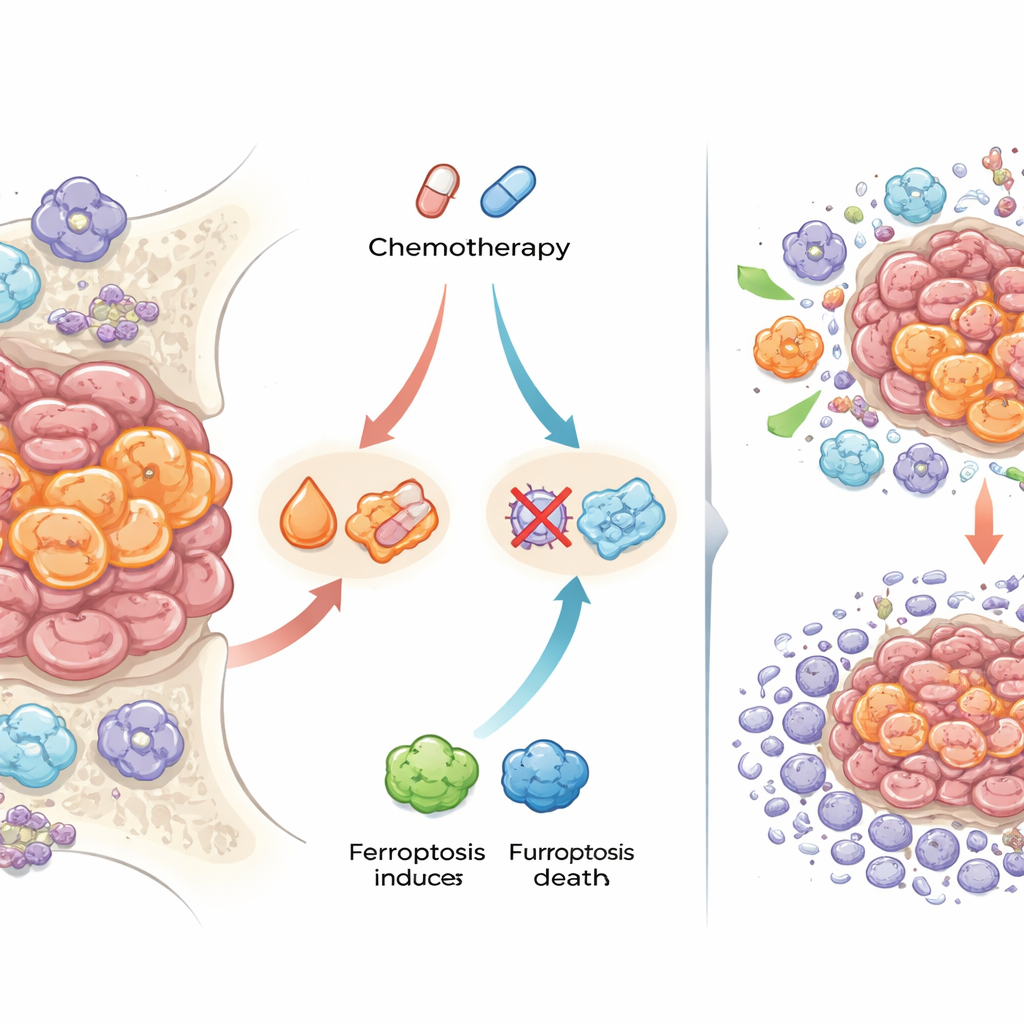
Immunzellen, die nützen oder schaden
Da Tumoren nicht isoliert wachsen, untersuchte das Team auch, wie Immunzellen in der Tumormikroumgebung mit dem Ergebnis zusammenhängen. Durch die Gruppierung von Primärtumoren allein anhand ihrer Proteom‑Muster entdeckten sie drei Hauptunterklassen mit unterschiedlichen Überlebensraten. Eine Hochrisikogruppe zeigte viele Zellzyklus‑ und Ubiquitin‑assoziierte Proteine und geringe Aktivität des Kernproteasoms, zusammen mit Proteinmustern von Neutrophilen und „Checkpoint“‑Molekülen, die Immunangriffe dämpfen können. Eine besserergebnis Gruppe wies höhere Spiegel von Proteinen auf, die an der Präsentation von Tumorfragmenten auf der Zelloberfläche beteiligt sind, ein entscheidender Schritt zur Aktivierung von T‑Zellen. Multiplex‑Immunfluoreszenz‑Bildgebung bestätigte, dass Tumoren mit schlechtem Ausgang reich an Neutrophilen waren, während Tumoren mit besserem Ausgang mehr Makrophagen, T‑Zellen und HLA‑positive antigenpräsentierende Zellen enthielten. Einfach gesagt: „Neutrophilenreiche“ Tumoren zeigten tendenziell ein schlechteres Verhalten, während Tumoren mit stärker eingebundenen adaptiven Immunzellen tendenziell besser verliefen.
Was das für künftige Behandlungen bedeutet
Zusammengefasst zeigt diese Arbeit, dass das Ewing‑Sarkom mehr ist als ein einzelner Genfehler; es ist ein komplexes Ökosystem aus Krebszellen, Eisenstoffwechsel und Immunakteuren, das sich unter Therapiedruck verschiebt. Für Patienten und Klinikpersonal weisen die Ergebnisse auf zwei vielversprechende Ansätze hin. Erstens könnten Wirkstoffe, die Krebszellen in Richtung Ferroptose treiben, die Wirkung bestehender Chemotherapien verbessern, insbesondere bei resistenten Erkrankungen. Zweitens könnten proteinbasierte Marker für Neutrophile, Makrophagen, T‑Zellen und Antigenpräsentation helfen, diejenigen Patientinnen und Patienten zu identifizieren, die von Immuntherapien oder Kombinationstherapien profitieren könnten. Zwar sind weitere Validierungen nötig, doch bietet dieser proteomische Atlas eine Landkarte, um die verborgene Biologie des Ewing‑Sarkoms in präzisere und möglicherweise erfolgreichere Behandlungsstrategien für junge Patientinnen und Patienten zu übersetzen.
Zitation: Gordon, S., Mohan, V., Shukrun, R. et al. Proteomic landscape of Ewing sarcoma primary tumors and metastases. Nat Commun 17, 3802 (2026). https://doi.org/10.1038/s41467-026-70449-5
Schlüsselwörter: Ewing‑Sarkom, Proteomik, Ferroptose, Tumormikroumgebung, Pädiatrischer Krebs