Clear Sky Science · zh
BRD4募集到ASXL1基因组靶点依赖BRD4的额外端域
这项研究为何重要
癌症常常劫持细胞的基因开关,在不该开启的时候启动生长程序。两个这样的关键基因调控因子,ASXL1和BRD4,在血液癌和脑瘤中经常发生改变或过度活跃。本研究以分子水平揭示了这两种蛋白在DNA上的物理连接方式、促癌形式的ASXL1如何增强该连接,以及为何这种蛋白伙伴关系可能成为新型抗癌疗法的有吸引力的靶点。 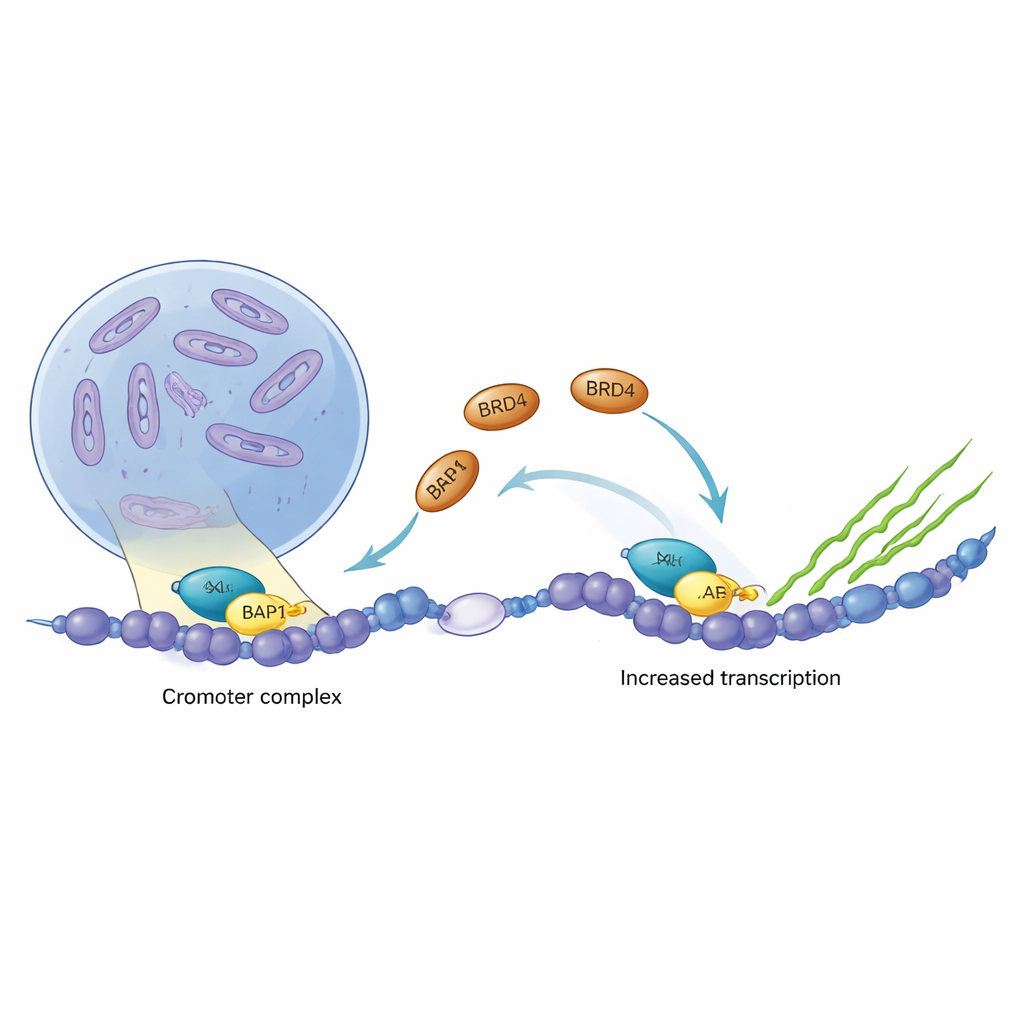
位于基因控制核心的伙伴关系
ASXL1是一个蛋白团队的一员,负责微调DNA的紧密程度,帮助决定哪些基因沉默、哪些被激活。相比之下,BRD4充当转录的强力点火开关,转录是将基因读成RNA的过程。通过分析若干肿瘤类型的癌症数据,作者发现ASXL1和BRD4的表达往往同向变化,并且BRD4经常占据驱动ASXL1自身表达的DNA区域。这种紧密的相关性暗示两者可能直接协作以增强癌细胞中特定的基因程式。
拉近分子握手的细节
为了解ASXL1与BRD4如何连接,团队使用了高分辨率结构学工具和生化检测。他们证明ASXL1中的一小段序列恰好嵌入BRD4所谓的额外端(ET)区域的一个凹槽中,形成紧密复合体。核磁共振实验显示,ASXL1贡献了一段短的伸展链与BRD4的一部分配对,同时疏水和带电侧链像拉链齿一样咬合。仅改变一到两个关键的ASXL1或BRD4残基,就足以在很大程度上破坏结合,证明该相互作用高度特异且具有明确的结构基础。有趣的是,ASXL1的近缘同源物ASXL2和ASXL3也使用类似的短基序与同一ET凹槽结合,提示存在保守的识别代码。
与癌症相关的截断如何重塑复合体
许多患有髓系血液癌的患者携带截短的ASXL1,截断大致位于蛋白质中段。作者聚焦于两种常见变体,终止于591和645位点。两者都缩短了蛋白但保留了BRD4结合区。当这些变体导入人类细胞时,它们能像正常蛋白一样有效地拉下BRD4,除非改变了单个关键接触残基。全基因组结合图谱显示,BRD4在ASXL1存在的启动子处强烈富集,当ASXL1–BRD4接触被破坏时,这种富集会下降。令人惊讶的是,稍长的截断(止于645)在将BRD4招募到某些基因启动子方面比更短的截断更有效,表明丢失ASXL1的某些部分反而可能悖论性地形成更强的、助长癌症的桥接作用。
激活基因的三方枢纽
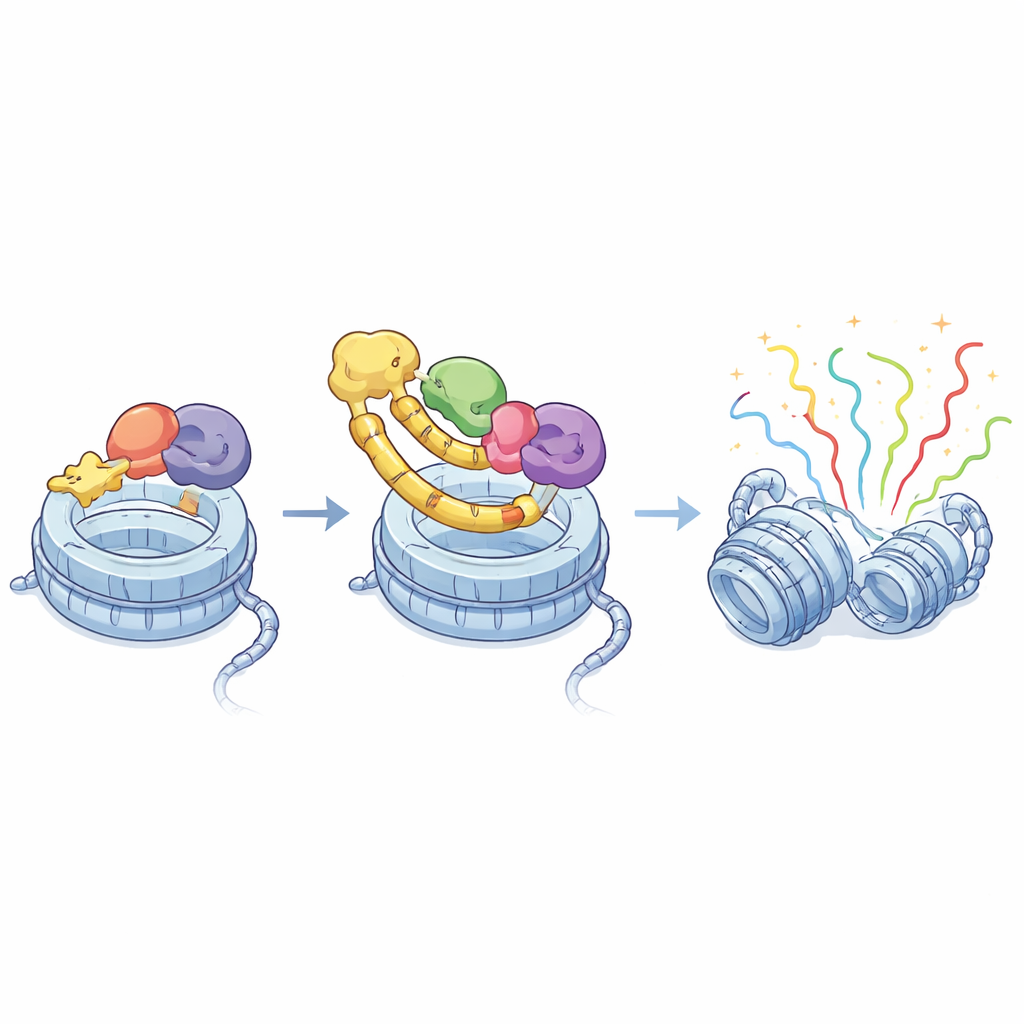
从分子洞见到治疗构想
通过结合结构生物学、基因组定位和癌症基因组学,这项研究表明BRD4的ET区域物理上钩住ASXL1中的一段短基序,这种“分子握手”对于指导BRD4到ASXL1调控的基因至关重要。与癌症相关的ASXL1截断不仅保留了这次握手,且在某些情况下增强了BRD4的募集并增加了系挂MLL3/4的能力,从而放大了基因激活。由于这些相互作用依赖于BRD4上的一个明确表面和ASXL1上的一小段序列,它们为设计可选择性破坏ASXL1–BRD4连接的小分子提供了清晰蓝图,可能在抑制驱动癌症的基因程式的同时保留BRD4的其他功能。
引用: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
关键词: 表观遗传调控, BRD4, ASXL1, 染色质复合体, 癌症转录