Clear Sky Science · nl
Rekrutering van BRD4 naar de ASXL1-genomische doelen hangt af van het extra-terminale domein van BRD4
Waarom deze studie ertoe doet
Kanker kapert vaak de gen-schakelaars van de cel en zet groeiprogramma’s aan wanneer ze uit zouden moeten staan. Twee zulke sleutelregulatoren van genen, ASXL1 en BRD4, zijn veelvuldig veranderd of overactief bij bloedkankers en hersentumoren. Deze studie onthult, tot op moleculair niveau, hoe deze twee eiwitten fysiek op het DNA met elkaar verbinden, hoe kankerveroorzakende vormen van ASXL1 die verbinding versterken, en waarom dit partnerschap een aantrekkelijk doel kan zijn voor nieuwe kankertherapieën. 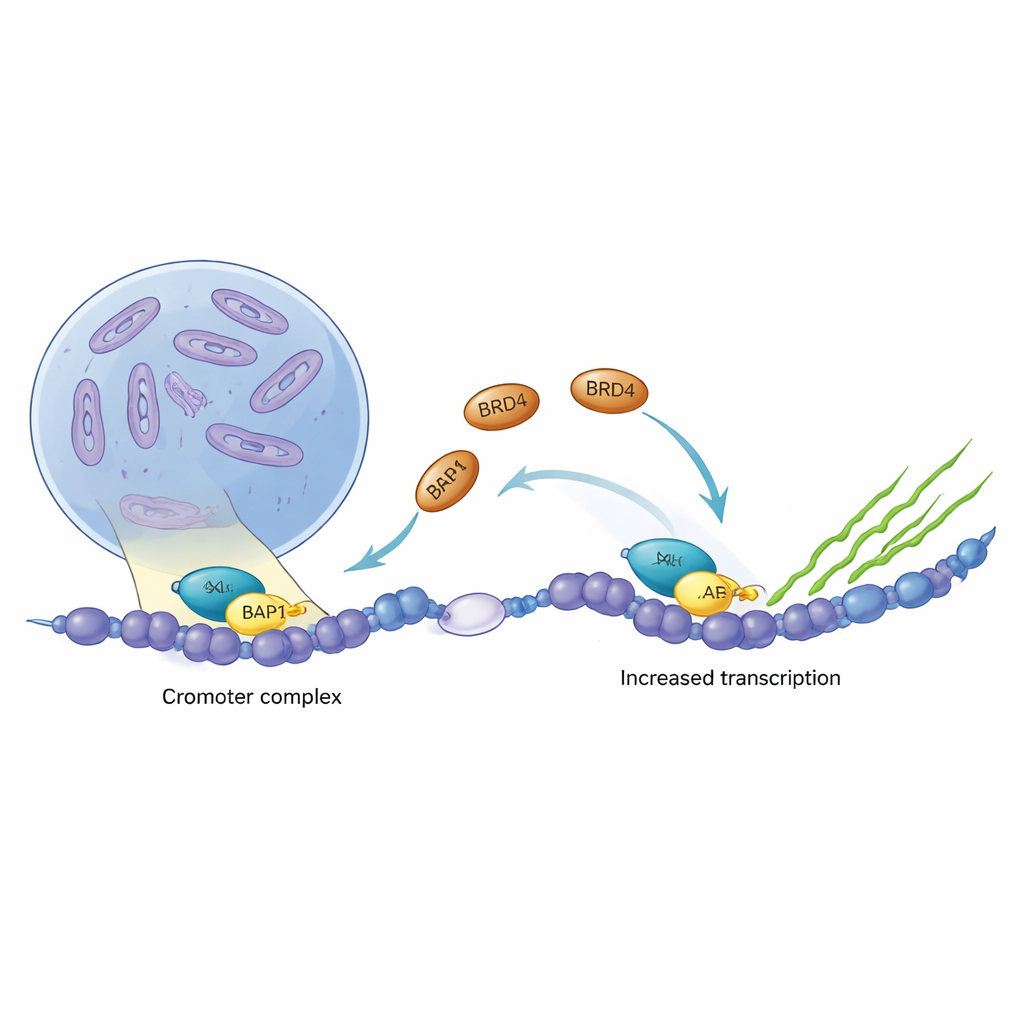
Een partnerschap in het hart van genregulatie
ASXL1 maakt deel uit van een eiwitcomplex dat nauwkeurig regelt hoe strak DNA is opgerold en daarmee helpt bepalen welke genen stil zijn en welke actief. BRD4 fungeert daarentegen als een krachtige ontstekingsschakelaar voor transcriptie, het proces dat genen omzet in RNA. Door kankergegevens van meerdere tumortypes te analyseren, vonden de auteurs dat ASXL1 en BRD4 de neiging hebben om samen te stijgen en te dalen, en dat BRD4 vaak aanwezig is op de DNA-regio die de eigen productie van ASXL1 aanstuurt. Deze sterke correlatie wees erop dat de twee eiwitten mogelijk rechtstreeks samenwerken om specifieke genprogramma’s in kankercellen te versterken.
Inzoomen op de moleculaire handdruk
Om te begrijpen hoe ASXL1 en BRD4 verbinden, gebruikte het team hoogresolutie-structurele technieken en biochemische tests. Ze lieten zien dat een korte reeks binnen ASXL1 precies in een groef past in het zogeheten extra-terminale (ET) gebied van BRD4, waarbij een strak complex ontstaat. Nucleaire magnetische resonantie-experimenten toonden aan dat ASXL1 een korte, uitgestrekte streng bijdraagt die paart met een deel van BRD4, terwijl hydrofobe en geladen zijketens in elkaar grijpen als tanden van een ritssluiting. Het muteren van slechts één of twee van deze sleutelresidu’s in ASXL1 of BRD4 was genoeg om de binding grotendeels te laten verdwijnen, waarmee bewezen wordt dat de interactie zeer specifiek en structureel goed gedefinieerd is. Intrigerend genoeg gebruiken ASXL1’s nauwe verwanten, ASXL2 en ASXL3, vergelijkbare korte motieven om aan dezelfde ET-groef te binden, wat wijst op een geconserveerde herkenningscode.
Hoe kanker-geassocieerde truncaties het complex hervormen
Veel patiënten met myeloïde bloedkankers dragen verkorte versies van ASXL1 die ongeveer halverwege het eiwit eindigen. De auteurs richtten zich op twee veelvoorkomende vormen die stoppen op positie 591 en 645. Beide verkorten het eiwit maar behouden de BRD4-bindende regio. Wanneer deze varianten in humane cellen werden geïntroduceerd, trokken ze BRD4 even effectief aan als het normale eiwit, tenzij een enkel kritisch contactresidu was gewijzigd. Genoomwijde bindingskaarten toonden aan dat BRD4 sterk verrijkt is bij promotoren waar ASXL1 aanwezig is, en dat deze verrijking afneemt wanneer het ASXL1–BRD4-contact wordt verstoord. Verrassend genoeg was de iets langere truncatie (eindigend bij 645) beter in staat BRD4 naar bepaalde genpromotoren te brengen dan de kortere variant, wat aangeeft dat het verliezen van sommige delen van ASXL1 paradoxaal genoeg een sterker, kankerbevorderend bruggetje naar BRD4 kan creëren.
Een drieledige hub voor genactivatie
Van moleculair inzicht naar behandelideeën
Door structurele biologie, genoomkaarten en kankergenomica te combineren, toont de studie aan dat het ET-gebied van BRD4 zich fysiek vastgrijpt aan een kort motief in ASXL1 en dat deze “moleculaire handdruk” essentieel is om BRD4 naar door ASXL1 gecontroleerde genen te leiden. Kanker-geassocieerde ASXL1-truncaties behouden deze handdruk niet alleen, maar versterken in sommige gevallen de rekrutering van BRD4 en voegen het vermogen toe om MLL3/4 vast te maken, waardoor genactivatie wordt versterkt. Omdat deze interacties afhangen van een goed afgebakend oppervlak op BRD4 en een korte reeks in ASXL1, bieden ze een duidelijk stappenplan voor het ontwerpen van kleine moleculen die mogelijk selectief de ASXL1–BRD4-verbinding kunnen verstoren, en zo kankerveroorzakende genprogramma’s kunnen dempen terwijl andere BRD4-functies gespaard blijven.
Bronvermelding: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Trefwoorden: epigenetische regulatie, BRD4, ASXL1, chromatinecomplexen, kankertranscriptie