Clear Sky Science · pt
Recrutamento de BRD4 aos alvos genômicos de ASXL1 depende do domínio extra‑terminal de BRD4
Por que este estudo é importante
O câncer frequentemente sequestra os interruptores genéticos da célula, ligando programas de crescimento quando deveriam permanecer desligados. Dois reguladores de genes importantes, ASXL1 e BRD4, são frequentemente alterados ou hiperativos em cânceres hematológicos e tumores cerebrais. Este estudo revela, em detalhe molecular, como essas duas proteínas se conectam fisicamente no DNA, como formas de ASXL1 associadas ao câncer fortalecem essa conexão e por que essa parceria pode ser um alvo atraente para novas terapias contra o câncer. 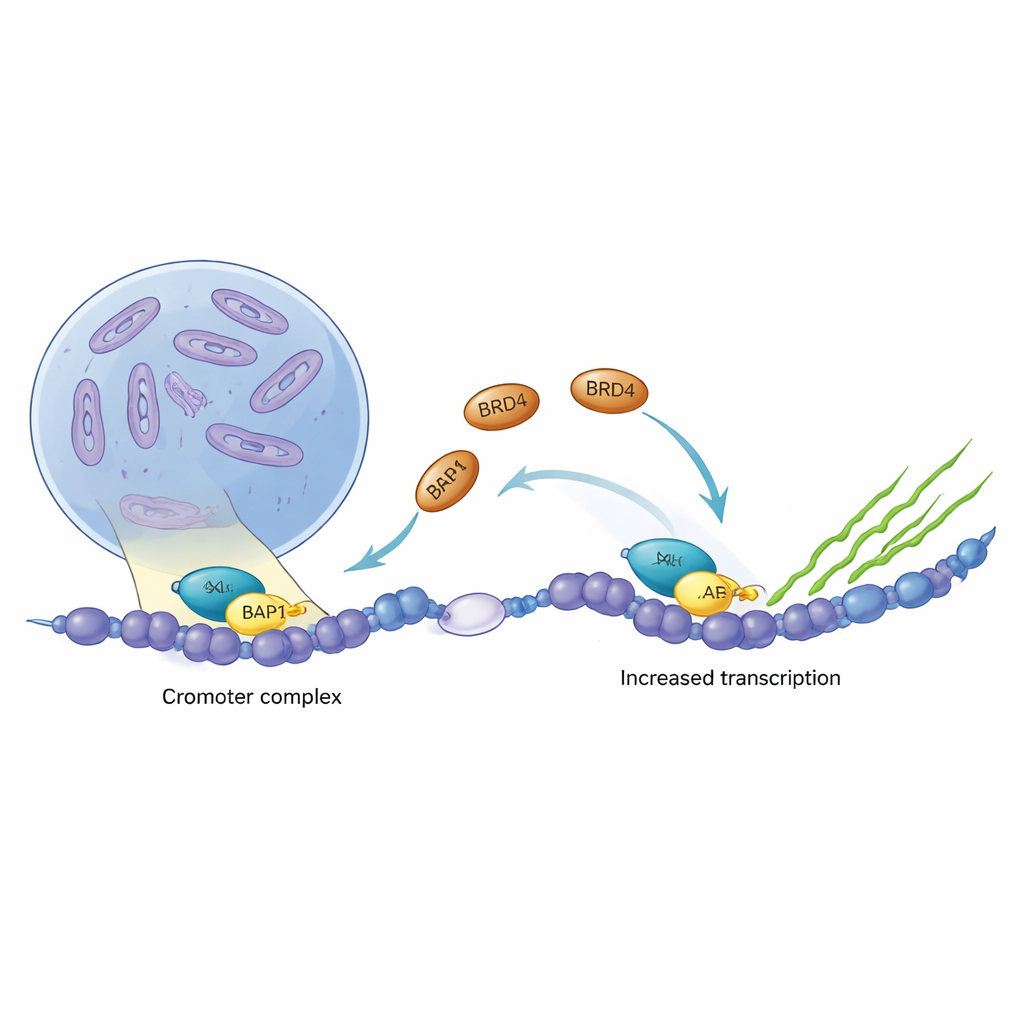
Uma parceria no centro do controle gênico
ASXL1 faz parte de um conjunto de proteínas que ajustam finamente o grau de empacotamento do DNA, ajudando a decidir quais genes ficam silenciados e quais ficam ativos. BRD4, em contraste, atua como um potente interruptor de ignição para a transcrição, o processo que lê genes em RNA. Ao analisar dados de câncer de vários tipos tumorais, os autores descobriram que ASXL1 e BRD4 tendem a subir e descer juntos, e que BRD4 frequentemente ocupa a região de DNA que dirige a própria produção de ASXL1. Essa correlação estreita sugeriu que as duas proteínas podem colaborar diretamente para impulsionar programas gênicos específicos em células cancerosas.
Focando no aperto de mão molecular
Para entender como ASXL1 e BRD4 se conectam, a equipe usou ferramentas estruturais de alta resolução e testes bioquímicos. Eles mostraram que um pequeno trecho dentro de ASXL1 se encaixa firmemente em uma ranhura na chamada região extra‑terminal (ET) de BRD4, formando um complexo estável. Experimentos de ressonância magnética nuclear revelaram que ASXL1 contribui com uma curta fita estendida que se emparelha com parte de BRD4, enquanto cadeias laterais hidrofóbicas e carregadas se entrelaçam como dentes de um zíper. A mutação de apenas um ou dois desses resíduos-chave em ASXL1 ou BRD4 foi suficiente para abolir em grande parte a ligação, provando que a interação é altamente específica e estruturalmente bem definida. Curiosamente, parentes próximos de ASXL1, ASXL2 e ASXL3, usam motivos curtos semelhantes para se ligar à mesma ranhura ET, sugerindo um código de reconhecimento conservado.
Como as truncações associadas ao câncer remodelam o complexo
Muitos pacientes com cânceres mieloides apresentam versões truncadas de ASXL1 que terminam aproximadamente na metade da proteína. Os autores concentraram‑se em duas formas comuns que param nas posições 591 e 645. Ambas encurtam a proteína, mas preservam a região de ligação a BRD4. Quando essas variantes foram introduzidas em células humanas, elas capturaram BRD4 com a mesma eficiência da proteína normal, a menos que um único resíduo crítico de contato fosse alterado. Mapas de ligação em todo o genoma mostraram que BRD4 está fortemente enriquecido em promotores onde ASXL1 está presente, e esse enriquecimento cai quando o contato ASXL1–BRD4 é interrompido. Surpreendentemente, a truncaçã o um pouco mais longa (terminando em 645) foi melhor em recrutar BRD4 para certos promotores do que a mais curta, indicando que perder algumas partes de ASXL1 pode paradoxalmente criar uma ponte mais forte e pró‑câncer para BRD4.
Um hub triplo para ativar genes
Do insight molecular a ideias de tratamento
Ao combinar biologia estrutural, mapeamento genômico e genômica do câncer, o estudo mostra que a região ET de BRD4 se prende fisicamente a um motivo curto em ASXL1 e que esse “aperto de mão molecular” é essencial para guiar BRD4 aos genes controlados por ASXL1. Truncaçõ es de ASXL1 associadas ao câncer não apenas preservam esse aperto de mão, mas, em alguns casos, potencializam o recrutamento de BRD4 e adicionam a capacidade de anexar MLL3/4, ampliando a ativação gênica. Como essas interações dependem de uma superfície bem definida em BRD4 e de um curto trecho de ASXL1, elas fornecem um roteiro claro para o desenho de pequenas moléculas que poderiam interromper seletivamente a ligação ASXL1–BRD4, potencialmente atenuando programas gênicos promotores do câncer ao mesmo tempo em que preservam outras funções de BRD4.
Citação: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Palavras-chave: regulação epigenética, BRD4, ASXL1, complexos de cromatina, transcrição no câncer