Clear Sky Science · ru
Привлечение BRD4 к геномным мишеням ASXL1 зависит от вне-концевого домена BRD4
Почему это исследование важно
Рак часто захватывает переключатели генов клетки, включая программы роста в неподходящее время. Два таких ключевых регулятора генов, ASXL1 и BRD4, нередко мутируют или оказываются гиперактивными при злокачественных заболеваниях крови и опухолях мозга. В этом исследовании подробно показано, как эти два белка физически связываются на ДНК, почему онкогенные усечённые формы ASXL1 усиливают это взаимодействие и почему такое партнёрство может быть привлекательной мишенью для новых противораковых терапий. 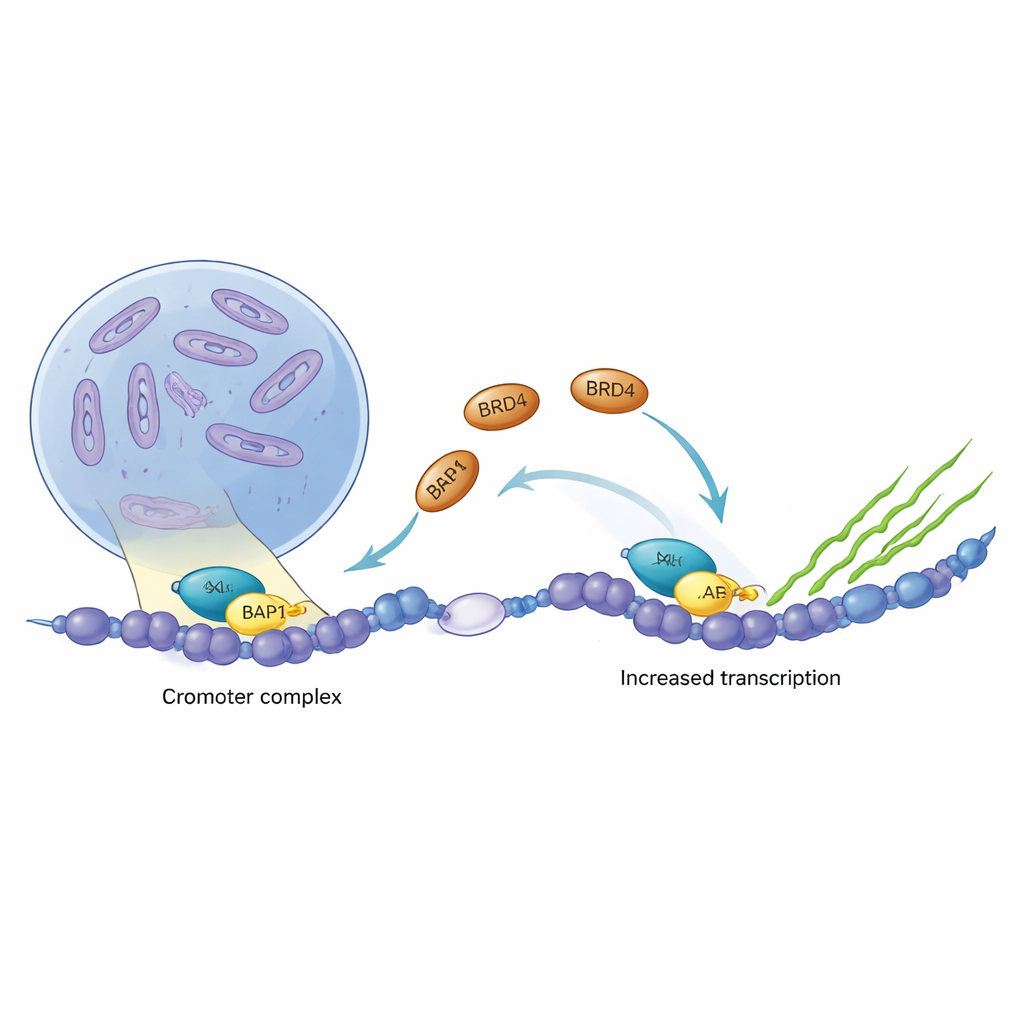
Партнёрство в основе управления генами
ASXL1 входит в белковый ансамбль, который тонко регулирует степень упаковки ДНК, помогая определять, какие гены молчат, а какие активны. BRD4, напротив, действует как мощный «замок зажигания» транскрипции — процесса считывания генов в РНК. Анализ данных о раке в нескольких типах опухолей показал, что уровни ASXL1 и BRD4 часто коррелируют, причём BRD4 часто занимает участки ДНК, управляющие собственной экспрессией ASXL1. Эта тесная корреляция навела на мысль, что два белка могут напрямую сотрудничать, усиливая конкретные генетические программы в раковых клетках.
Приближение к молекулярному рукопожатию
Чтобы понять, как ASXL1 и BRD4 связываются, группа использовала методы высокоразрешающей структурной биологии и биохимические тесты. Они показали, что короткий участок внутри ASXL1 плотно входит в бороздку вне-концевого (ET) домена BRD4, образуя стабильный комплекс. Эксперименты ядерного магнитного резонанса выявили, что ASXL1 даёт короткую вытянутую нить, которая сочетается с частью BRD4, а гидрофобные и заряженные боковые цепи сцепляются подобно зубцам молнии. Замена всего одного–двух ключевых остатков в ASXL1 или BRD4 была достаточна, чтобы почти полностью нарушить связывание, что доказывает высокую специфичность и чёткую структурную детерминанту взаимодействия. Любопытно, что близкие родственники ASXL1 — ASXL2 и ASXL3 — используют похожие короткие мотивы для связывания той же бороздки ET, что указывает на сохранённый код узнавания.
Как онкоприурчённые усечения меняют комплекс
У многих больных миелоидными опухолями крови обнаруживаются усечённые варианты ASXL1, которые обрываются примерно на середине молекулы. Авторы сосредоточились на двух распространённых вариантах, которые прекращаются на позициях 591 и 645. Оба укорачивают белок, но сохраняют область связывания с BRD4. При введении этих вариантов в человеческие клетки они так же эффективно вытягивали BRD4, как и нормальный белок, если только не была изменена одна критическая контактная аминокислота. Геномные карты связывания показали, что BRD4 сильно обогащён на промоторах, где присутствует ASXL1, и это обогащение уменьшается при разрушении контакта ASXL1–BRD4. Удивительно, что чуть более длинный усечённый вариант (с окончанием на 645) был лучше способен привлекать BRD4 к определённым промоторам по сравнению с более коротким — это указывает на то, что утрата некоторых частей ASXL1 порою парадоксально создаёт более прочный, канцерогенно значимый мост к BRD4.
Трёхсторонний узел для активации генов
От молекулярного понимания к идеям терапии
Объединив структурную биологию, картирование в масштабах генома и онкогеномику, исследование показывает, что ET‑регион BRD4 физически захватывает короткий мотив в ASXL1 и что это «молекулярное рукопожатие» необходимо для направления BRD4 к генам, контролируемым ASXL1. Онкологические усечения ASXL1 не только сохраняют это рукопожатие, но в некоторых случаях усиливают привлечение BRD4 и добавляют способность стягивать MLL3/4, усиливая активацию генов. Поскольку эти взаимодействия опираются на чётко определённую поверхность BRD4 и короткий участок ASXL1, они дают ясную основу для разработки малых молекул, которые могли бы избирательно разрушать связь ASXL1–BRD4, потенциально ослабляя онкологические программы генов при сохранении других функций BRD4.
Цитирование: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Ключевые слова: эпигенетическая регуляция, BRD4, ASXL1, хроматиновые комплексы, транскрипция при раке