Clear Sky Science · sv
Rekrytering av BRD4 till ASXL1:s genomiska mål beror på BRD4:s extra-terminala domän
Varför denna studie är viktig
Cancer kapar ofta cellens genreglage och slår på tillväxtprogram som borde vara avstängda. Två sådana centrala genregulatorer, ASXL1 och BRD4, är ofta förändrade eller överaktiva i blodcancer och hjärntumörer. Denna studie avslöjar i molekylär detalj hur dessa två proteiner fysiskt förbinder sig på DNA, hur cancerskapande former av ASXL1 stärker den kopplingen och varför detta partnerskap kan vara ett attraktivt mål för nya cancerterapier. 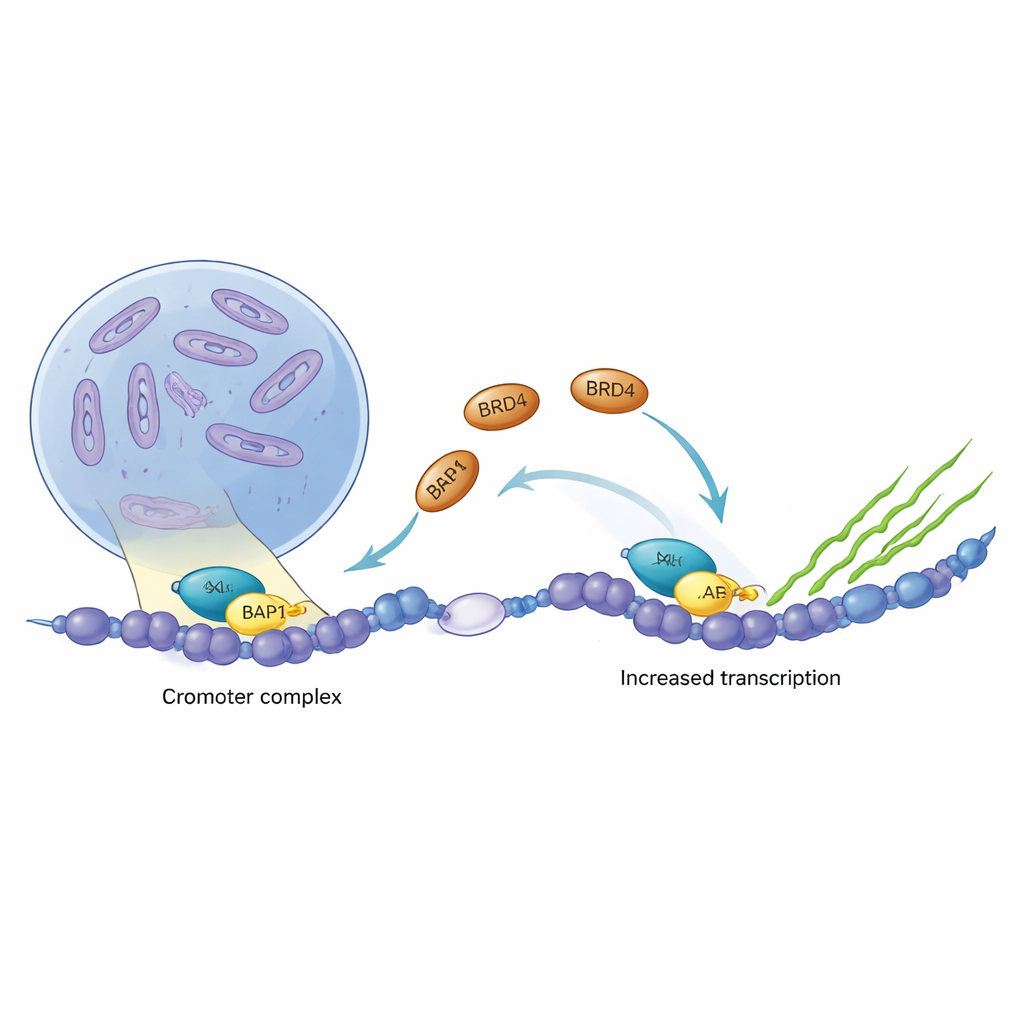
En partnerskap i genregleringens mitt
ASXL1 ingår i ett proteinkomplex som finjusterar hur tätt DNA är packat och hjälper till att avgöra vilka gener som är tysta och vilka som är aktiva. BRD4 fungerar däremot som en kraftfull tändning för transkription, processen som läser av gener till RNA. Genom att analysera cancerdata från flera tumörtyper fann författarna att ASXL1 och BRD4 tenderar att öka och minska tillsammans, och att BRD4 ofta binder till den DNA-region som driver ASXL1:s egen produktion. Denna starka korrelation antydde att de två proteinerna kan samarbeta direkt för att förstärka specifika genprogram i cancerceller.
Närbild av det molekylära handslaget
För att förstå hur ASXL1 och BRD4 kopplar ihop sig använde gruppen högupplösta strukturella metoder och biokemiska tester. De visade att en kort sekvens inom ASXL1 passar tätt i en fåra i BRD4:s så kallade extra-terminala (ET) region och bildar ett stabilt komplex. NMR-experiment visade att ASXL1 bidrar med en kort, utsträckt streng som parar med en del av BRD4, medan hydrofoba och laddade sidokedjor hakar i varandra som tänder i en dragkedja. Att mutera bara en eller två av dessa viktiga ASXL1- eller BRD4-restar var tillräckligt för i stort sett att upphäva bindningen, vilket bevisar att interaktionen är mycket specifik och strukturellt väl definierad. Intressant nog använder ASXL1:s närbesläktade proteiner, ASXL2 och ASXL3, liknande korta motiv för att binda samma ET-fåra, vilket tyder på en bevarad igenkänningskod.
Hur cancerkopplade trunkeringar omformar komplexet
Många patienter med myeloida blodcancer bär på trunkerade versioner av ASXL1 som slutar ungefär halvvägs genom proteinet. Författarna fokuserade på två vanliga varianter som slutar vid position 591 respektive 645. Båda förkortar proteinet men bevarar BRD4-bindande regionen. När dessa varianter introducerades i humana celler drog de ner BRD4 lika effektivt som det normala proteinet, om inte en enda kritisk kontaktrest ändrades. Genomkartläggning av bindningsplatser i hela genomet visade att BRD4 är starkt förhöjt vid promotorer där ASXL1 finns, och denna förhöjning minskar när ASXL1–BRD4-kontakten störs. Överraskande nog var den något längre trunkeringen (slutande vid 645) bättre på att rekrytera BRD4 till vissa genpromotorer än den kortare, vilket tyder på att förlust av vissa delar av ASXL1 paradoxalt nog kan skapa en starkare, cancerdrivande bro till BRD4.
Ett trefaldigt nav för genaktivering
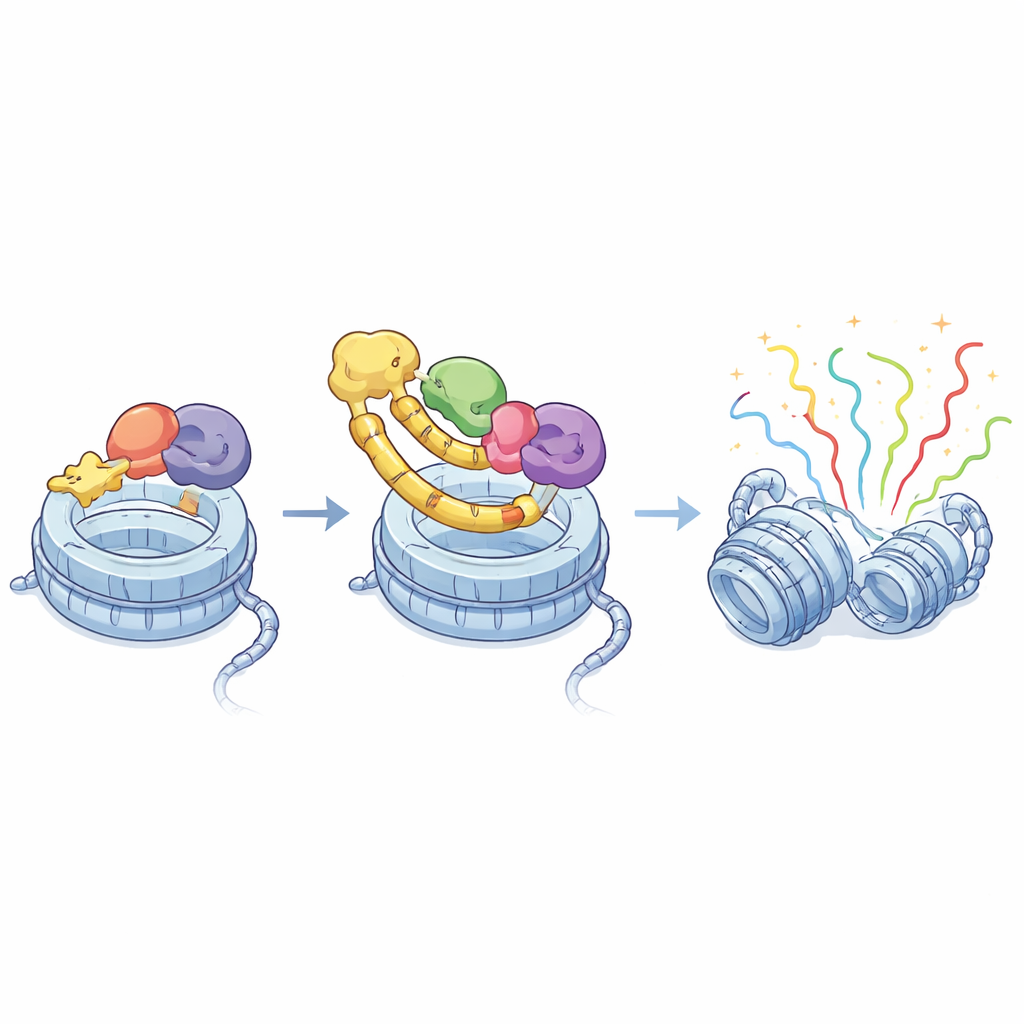
Från molekylär insikt till behandlingsidéer
Genom att kombinera strukturell biologi, genomkartläggning och cancergenomik visar studien att BRD4:s ET-region fysiskt hakar fast vid ett kort motiv i ASXL1 och att detta ”molekylära handslag” är avgörande för att styra BRD4 till ASXL1-kontrollerade gener. Cancerassocierade ASXL1-trunkeringar bevarar inte bara detta handslag utan förstärker i vissa fall BRD4-rekrytering och tillför förmågan att förankra MLL3/4, vilket förstärker genaktivering. Eftersom dessa interaktioner bygger på en väl definierad yta på BRD4 och en kort sekvens i ASXL1 ger de en tydlig ritning för att designa småmolekyler som selektivt skulle kunna störa ASXL1–BRD4-länken, och potentiellt dämpa cancerdrivande genprogram samtidigt som andra BRD4-funktioner sparas.
Citering: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Nyckelord: epigenetisk reglering, BRD4, ASXL1, kromatin-komplex, cancertranskription