Clear Sky Science · ja
BRD4のASXL1ゲノム標的へのリクルートはBRD4のエクストラターミナル領域に依存する
この研究が重要な理由
がんはしばしば細胞の遺伝子スイッチを乗っ取り、本来オフであるべき増殖プログラムをオンにしてしまいます。ASXL1とBRD4はそのような主要な遺伝子調節因子であり、血液がんや脳腫瘍で頻繁に変異や過剰活性化が見られます。本研究は、これら二つのタンパク質がDNA上でどのように物理的に結合するか、がん促進型のASXL1がその結合をどのように強化するか、そしてなぜこの協調が新しいがん治療の有望な標的となり得るかを分子レベルで明らかにします。 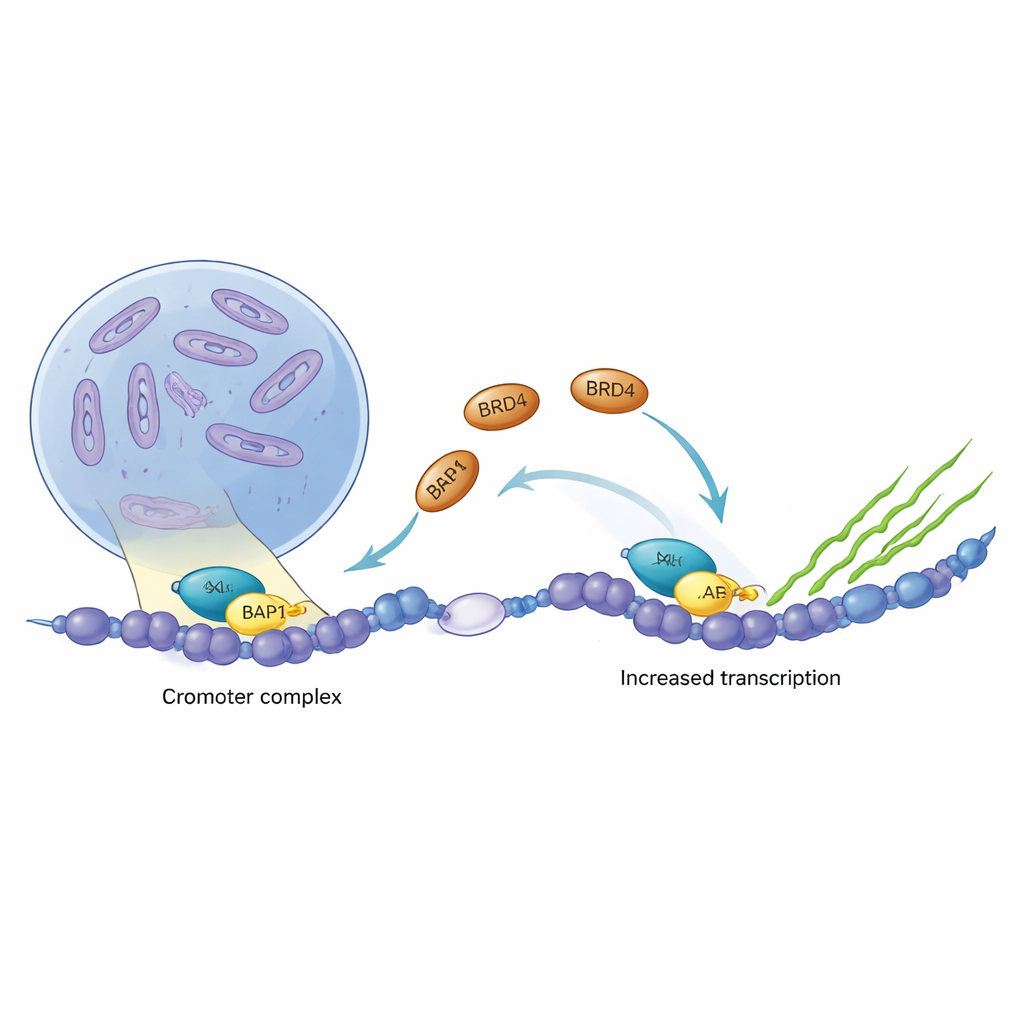
遺伝子制御の中心にある協働
ASXL1はDNAの締まり具合を微調整するタンパク質群の一員で、どの遺伝子を沈黙させどれを活性化するかを決めるのに寄与します。一方BRD4は、遺伝子をRNAへ読み取る転写というプロセスの強力な点火スイッチとして働きます。複数の腫瘍タイプからのがんデータを解析したところ、ASXL1とBRD4は発現が連動する傾向があり、BRD4はしばしばASXL1自身の産生を駆動する領域に占有していました。この強い相関は、両者ががん細胞における特定の遺伝子プログラムを直接的に協働して高めている可能性を示唆しました。
分子レベルの握手を詳細に見る
ASXL1とBRD4がどのように結びつくかを理解するために、研究チームは高解像度の構造解析手法と生化学的試験を用いました。彼らはASXL1の短い配列がBRD4のいわゆるエクストラターミナル(ET)領域の溝にぴったり収まり、緊密な複合体を形成することを示しました。核磁気共鳴(NMR)実験は、ASXL1が短い伸長した鎖を供給してBRD4の一部と対を成し、疎水性や電荷をもつ側鎖がジッパーの歯のようにかみ合うことを明らかにしました。ASXL1またはBRD4のこれら重要な残基を一つか二つ変異させるだけで結合がほとんど失われることから、この相互作用は極めて特異的で構造的に明確に定義されていることが証明されました。興味深いことに、ASXL1の近縁であるASXL2やASXL3も同様の短いモチーフを使って同じET溝に結合するため、保存された認識コードが存在すると示唆されます。
がんに関連した切断が複合体をどう変えるか
多くの骨髄系血液がん患者は、タンパク質の途中でほぼ半分で終わるASXL1の切断型を持っています。著者らは位置591と645で終わる二つの一般的な型に注目しました。どちらもタンパク質を短縮しますが、BRD4結合領域は保持します。これらのバリアントをヒト細胞に導入すると、単一の重要な接触残基が変えられない限り、正常型と同様にBRD4を引き下ろしました。ゲノム全体の結合マップは、BRD4がASXL1が存在するプロモーターに強く濃縮していることを示し、この濃縮はASXL1–BRD4の接触が破壊されると低下します。驚くべきことに、やや長い切断型(645で終わる方)は短い切断型よりも特定の遺伝子プロモーターにBRD4を呼び込む能力が高く、ASXL1の一部を失うことが矛盾的にBRD4とのより強い、がんを助長する橋を作る場合があることを示しています。
遺伝子を活性化する三者ハブ
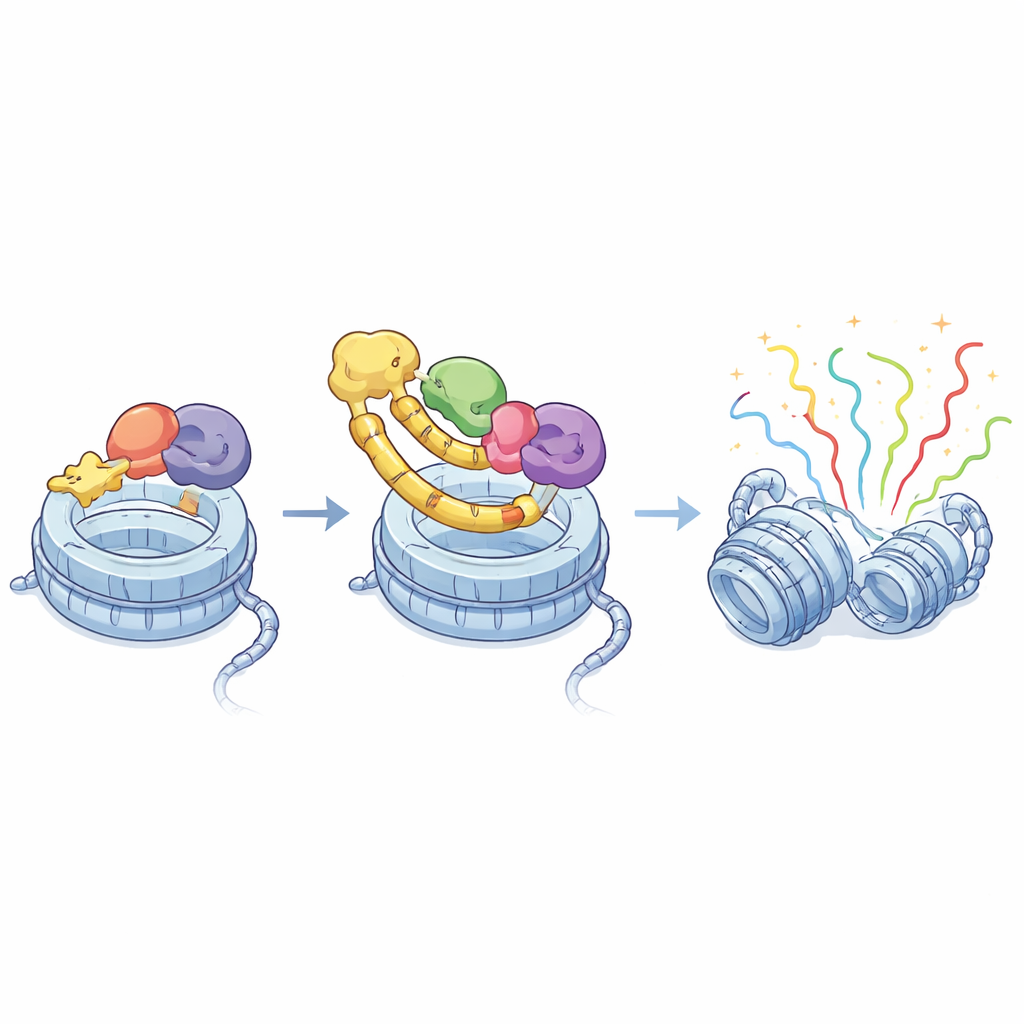
分子洞察から治療アイデアへ
構造生物学、ゲノムマッピング、がんゲノミクスを組み合わせた本研究は、BRD4のET領域がASXL1の短いモチーフに物理的に結合し、この「分子の握手」がBRD4をASXL1が制御する遺伝子へ導く上で不可欠であることを示します。がん関連のASXL1切断型はこの握手を保持するだけでなく、場合によってはBRD4のリクルートを強化し、MLL3/4を繋ぎ止める能力を付加して遺伝子活性化を増幅します。これらの相互作用がBRD4上の明確に定義された表面とASXL1の短い配列に依存しているため、ASXL1–BRD4結合を選択的に妨げる小分子を設計するための明確な設計図を提供し得ます。そうした薬剤は他のBRD4機能を残しつつ、がんを駆動する遺伝子プログラムを弱める可能性があります。
引用: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
キーワード: エピジェネティック制御, BRD4, ASXL1, クロマチン複合体, がんの転写