Clear Sky Science · pl
Rekrutacja BRD4 do celów genomicznych ASXL1 zależy od domeny ekstra‑terminalnej BRD4
Dlaczego to badanie ma znaczenie
Nowotwory często przejmują kontrolę nad przełącznikami genów komórki, uruchamiając programy wzrostu wtedy, gdy powinny być wyłączone. Dwoje takich kluczowych regulatorów genów, ASXL1 i BRD4, jest często zmienionych lub nadaktywnych w nowotworach krwi i guzach mózgu. To badanie ujawnia, na poziomie molekularnym, jak te dwa białka fizycznie łączą się na DNA, w jaki sposób formy ASXL1 sprzyjające nowotworzeniu wzmacniają to połączenie oraz dlaczego ta współpraca może być atrakcyjnym celem dla nowych terapii przeciwnowotworowych. 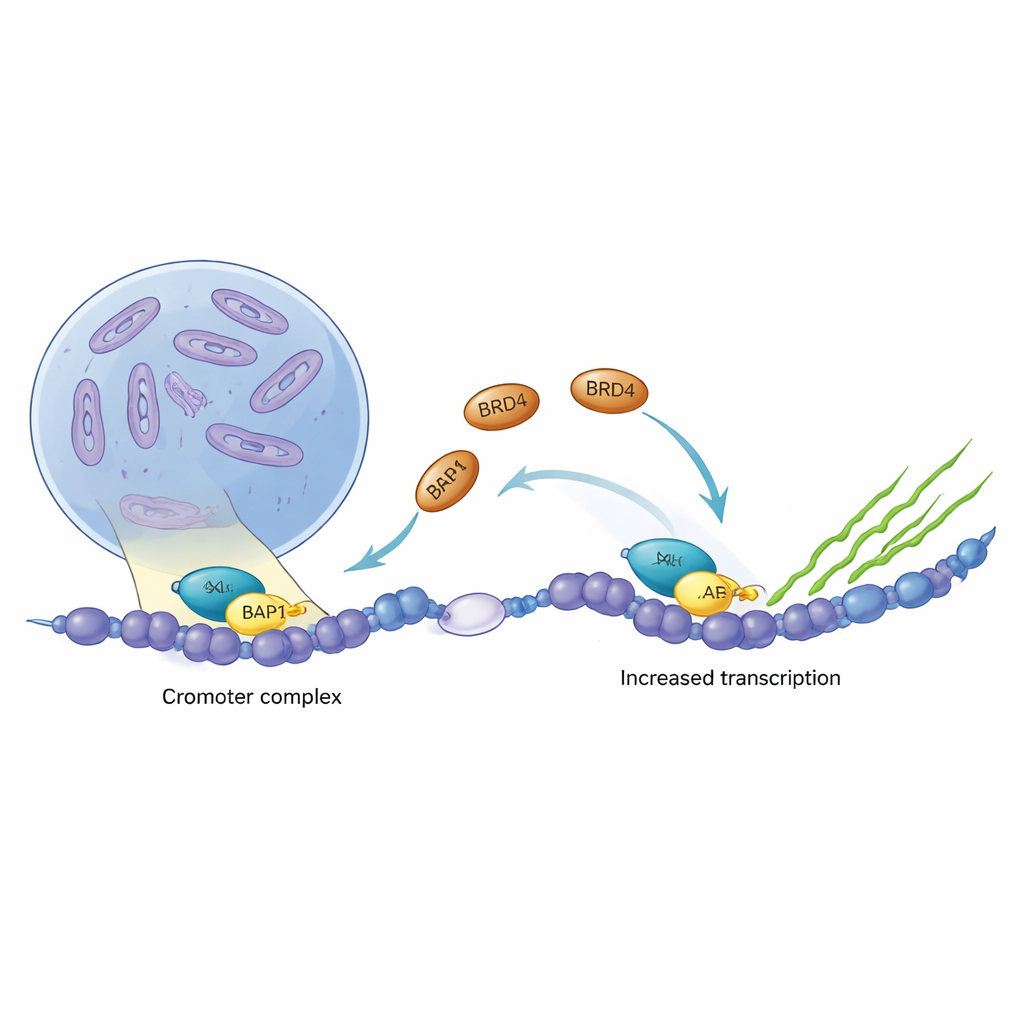
Partnerstwo w centrum kontroli genów
ASXL1 jest częścią zespołu białek, które precyzyjnie regulują, jak ciasno upakowane jest DNA, pomagając decydować, które geny są wyciszone, a które aktywne. Natomiast BRD4 działa jak silny wyłącznik zapłonu transkrypcji, procesu przepisywania genów na RNA. Analiza danych z różnych typów guzów wykazała, że poziomy ASXL1 i BRD4 często rosną i spadają razem, a BRD4 często zajmuje region DNA odpowiadający za własną produkcję ASXL1. Ten silny związek sugerował, że oba białka mogą współpracować bezpośrednio, aby wzmacniać określone programy genowe w komórkach nowotworowych.
Pogłębienie molekularnego uścisku dłoni
Aby zrozumieć, jak ASXL1 i BRD4 się łączą, zespół użył narzędzi strukturalnych o wysokiej rozdzielczości i testów biochemicznych. Wykazali, że krótki fragment ASXL1 idealnie wpasowuje się w rowek w tak zwanej domenie ekstra‑terminalnej (ET) BRD4, tworząc silny kompleks. Eksperymenty z użyciem magnetycznego rezonansu jądrowego ujawniły, że ASXL1 dostarcza krótkiego, wydłużonego pasma, które paruje się z częścią BRD4, podczas gdy hydrofobowe i naładowane łańcuchy boczne zazębiają się jak zęby zamka błyskawicznego. Mutacja zaledwie jednego lub dwóch kluczowych reszt ASXL1 lub BRD4 wystarczyła, by w dużym stopniu zlikwidować wiązanie, dowodząc, że interakcja jest wysoce specyficzna i strukturalnie dobrze określona. Co ciekawe, bliscy krewni ASXL1, ASXL2 i ASXL3, używają podobnych krótkich motywów do wiązania tego samego rowka ET, co sugeruje zachowany kod rozpoznawczy.
Jak mutacje skracające ASXL1 przekształcają kompleks
Wielu pacjentów z nowotworami mieloidalnymi krwi nosi zmutowane, skrócone wersje ASXL1, które kończą się mniej więcej w połowie białka. Autorzy skupili się na dwóch powszechnych formach kończących się na pozycjach 591 i 645. Obie skracają białko, ale zachowują region wiążący BRD4. Gdy te warianty wprowadzono do komórek ludzkich, wyciągały BRD4 równie skutecznie co białko normalne, chyba że zmieniono pojedynczą krytyczną resztę kontaktową. Mapy wiązań w skali genomu wykazały, że BRD4 jest silnie wzbogacony w promotorach, gdzie obecny jest ASXL1, a to wzbogacenie spada, gdy kontakt ASXL1–BRD4 zostanie przerwany. Co zaskakujące, nieco dłuższe skrócenie (kończące się na 645) lepiej przyciągało BRD4 do niektórych promotorów genów niż krótsza wersja, co wskazuje, że utrata niektórych części ASXL1 może paradoksalnie stworzyć silniejsze, sprzyjające nowotworzeniu połączenie z BRD4.
Trójstronny węzeł aktywujący geny
Od wglądu molekularnego do pomysłów terapeutycznych
Łącząc biologię strukturalną, mapowanie genomu i genomikę nowotworową, badanie pokazuje, że domena ET BRD4 fizycznie zakleszcza się na krótkim motywie w ASXL1 i że ten „molekularny uścisk dłoni” jest niezbędny do kierowania BRD4 do genów kontrolowanych przez ASXL1. Mutacje skracające ASXL1 związane z rakiem nie tylko zachowują ten uścisk dłoni, ale w niektórych przypadkach wzmacniają rekrutację BRD4 i dodają zdolność przyciągania MLL3/4, wzmacniając aktywację genów. Ponieważ te interakcje opierają się na dobrze określonej powierzchni BRD4 i krótkim fragmencie ASXL1, stanowią jasny plan do zaprojektowania małych cząsteczek, które mogłyby selektywnie zakłócać połączenie ASXL1–BRD4, potencjalnie osłabiając programy genowe napędzające raka przy zachowaniu innych funkcji BRD4.
Cytowanie: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Słowa kluczowe: regulacja epigenetyczna, BRD4, ASXL1, kompleksy chromatynowe, transkrypcja nowotworowa