Clear Sky Science · de
Die Rekrutierung von BRD4 zu genomischen Zielen von ASXL1 hängt von der extra‑terminalen Domäne von BRD4 ab
Warum diese Studie wichtig ist
Krebs kapert häufig die Gen‑Schalter der Zelle und schaltet Wachstumsprogramme ein, wenn sie eigentlich aus sein sollten. Zwei solche zentralen Genregulatoren, ASXL1 und BRD4, sind bei Blutkrebsarten und Hirntumoren oft verändert oder überaktiv. Diese Studie enthüllt auf molekularer Ebene, wie sich diese beiden Proteine physisch auf der DNA verbinden, warum krebsfördernde Varianten von ASXL1 diese Verbindung verstärken und weshalb diese Partnerschaft ein vielversprechendes Ziel für neue Krebstherapien sein könnte. 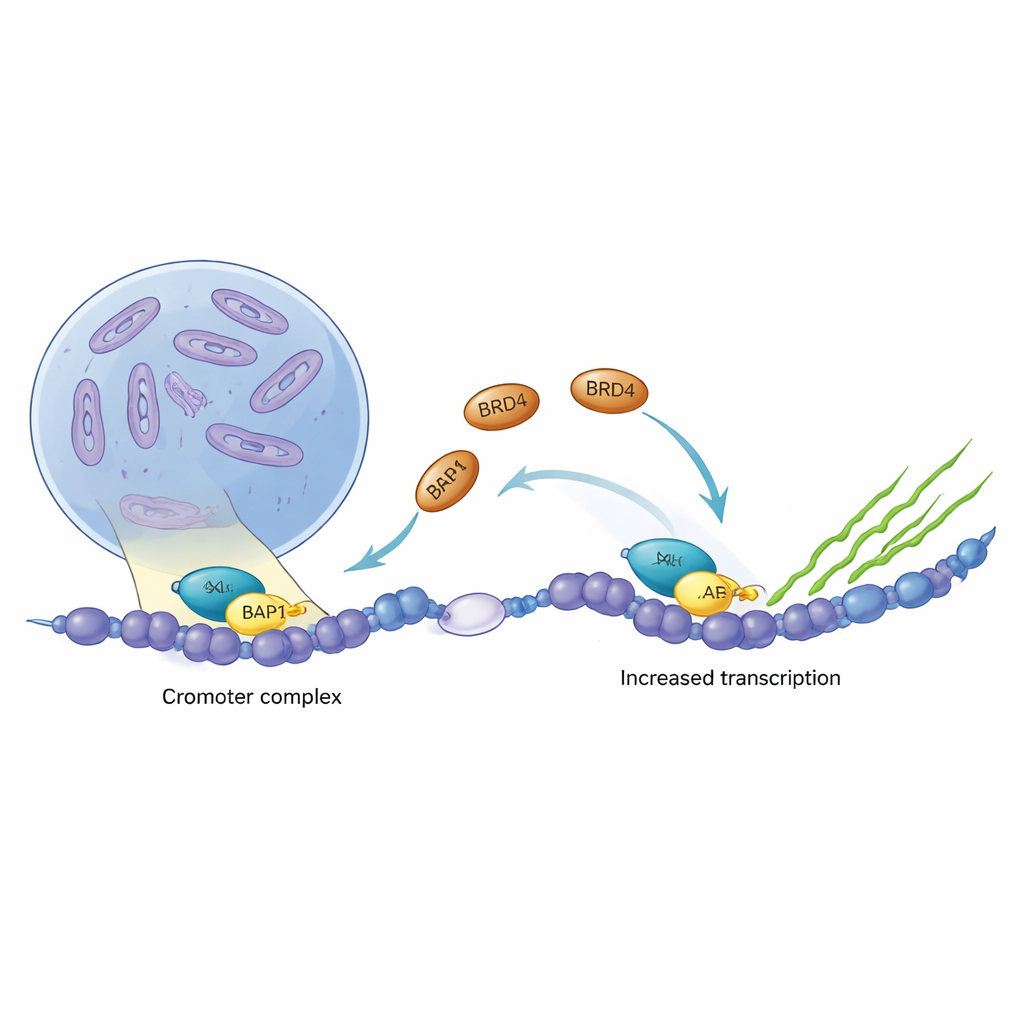
Eine Partnerschaft im Zentrum der Genkontrolle
ASXL1 ist Teil eines Proteinensembles, das fein reguliert, wie dicht DNA verpackt ist, und somit entscheidet, welche Gene stillgelegt und welche aktiviert werden. BRD4 wirkt dagegen als starker Zündschalter für die Transkription, den Prozess, der Gene in RNA übersetzt. Anhand von Krebsdaten aus mehreren Tumorarten zeigten die Autorinnen und Autoren, dass ASXL1 und BRD4 häufig gemeinsam ansteigen und fallen und dass BRD4 vielfach die DNA‑Region besetzt, die die eigene Produktion von ASXL1 antreibt. Diese enge Korrelation deutete darauf hin, dass die beiden Proteine direkt zusammenarbeiten könnten, um bestimmte Genprogramme in Krebszellen zu verstärken.
Heranzoomen an den molekularen Handschlag
Um zu verstehen, wie ASXL1 und BRD4 sich verbinden, nutzte das Team hochauflösende Strukturmethoden und biochemische Tests. Sie zeigten, dass ein kurzer Abschnitt innerhalb von ASXL1 passgenau in eine Furche der sogenannten extra‑terminalen (ET) Region von BRD4 passt und dort einen stabilen Komplex bildet. Kernspinresonanzexperimente legten nahe, dass ASXL1 einen kurzen, gestreckten Strang beisteuert, der sich mit einem Teil von BRD4 verbindet, während hydrophe und geladene Seitenketten wie Zähnchen eines Reißverschlusses ineinandergreifen. Das Verändern nur eines oder zweier dieser Schlüsselreste in ASXL1 oder BRD4 reichte aus, um die Bindung weitgehend zu unterbinden, was beweist, dass die Wechselwirkung hochspezifisch und strukturell klar definiert ist. Interessanterweise nutzen die nahen Verwandten ASXL2 und ASXL3 ähnliche kurze Motive, um dieselbe ET‑Furche zu binden, was auf einen erhaltenen Erkennungsmechanismus hinweist.
Wie krebsassoziierte Trunkierungen den Komplex umgestalten
Viele Patientinnen und Patienten mit myeloiden Blutkrebserkrankungen tragen getrunkene (trunkierte) Versionen von ASXL1, die etwa in der Mitte des Proteins enden. Die Autoren konzentrierten sich auf zwei häufige Varianten, die bei den Positionen 591 bzw. 645 enden. Beide verkürzen das Protein, erhalten jedoch die BRD4‑Binderegion. Wenn diese Varianten in menschliche Zellen eingebracht wurden, zogen sie BRD4 genauso effizient an wie das normale Protein, sofern nicht eine einzelne kritische Kontaktstelle verändert war. Genomweite Bindungskarten zeigten, dass BRD4 an Promotoren, an denen ASXL1 präsent ist, stark angereichert ist, und dass diese Anreicherung abnimmt, wenn der ASXL1–BRD4‑Kontakt gestört wird. Überraschenderweise war die etwas längere Trunkierung (Ende bei 645) besser darin, BRD4 zu bestimmten Genpromotoren zu bringen als die kürzere, was darauf hindeutet, dass der Verlust einiger ASXL1‑Abschnitte paradox eine stärkere, krebsfördernde Brücke zu BRD4 erzeugen kann.
Ein dreifaches Zentrum zur Genaktivierung
Vom molekularen Einblick zu Therapiekonzepten
Durch die Kombination von Strukturbiologie, Genomkartierung und Krebsgenomik zeigt die Studie, dass die ET‑Region von BRD4 physikalisch an ein kurzes Motiv in ASXL1 andockt und dass dieser „molekulare Handschlag“ entscheidend dafür ist, BRD4 zu ASXL1‑kontrollierten Genen zu leiten. Krebsassoziierte ASXL1‑Trunkierungen erhalten diesen Handschlag nicht nur, sondern können in einigen Fällen die BRD4‑Rekrutierung verstärken und zusätzlich die Fähigkeit gewinnen, MLL3/4 zu verankern, wodurch die Genaktivierung verstärkt wird. Da diese Interaktionen auf einer klar definierten Oberfläche von BRD4 und einer kurzen ASXL1‑Sequenz beruhen, liefern sie eine eindeutige Blaupause für die Entwicklung kleiner Moleküle, die die ASXL1–BRD4‑Verbindung selektiv stören könnten und so krebsfördernde Genprogramme dämpfen, während andere BRD4‑Funktionen erhalten bleiben dürften.
Zitation: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Schlüsselwörter: epigenetische Regulation, BRD4, ASXL1, Chromatin‑Komplexe, Krebs‑Transkription