Clear Sky Science · fr
Le recrutement de BRD4 sur les cibles génomiques d’ASXL1 dépend du domaine extra-terminal de BRD4
Pourquoi cette étude est importante
Le cancer détourne souvent les interrupteurs génétiques de la cellule, activant des programmes de croissance au moment où ils devraient être éteints. Deux régulateurs clés de ces programmes, ASXL1 et BRD4, sont fréquemment altérés ou hyperactifs dans les cancers du sang et les tumeurs cérébrales. Cette étude révèle, au niveau moléculaire, comment ces deux protéines se connectent physiquement sur l’ADN, comment les formes d’ASXL1 liées au cancer renforcent cette connexion, et pourquoi ce partenariat pourrait constituer une cible séduisante pour de nouveaux traitements anticancéreux. 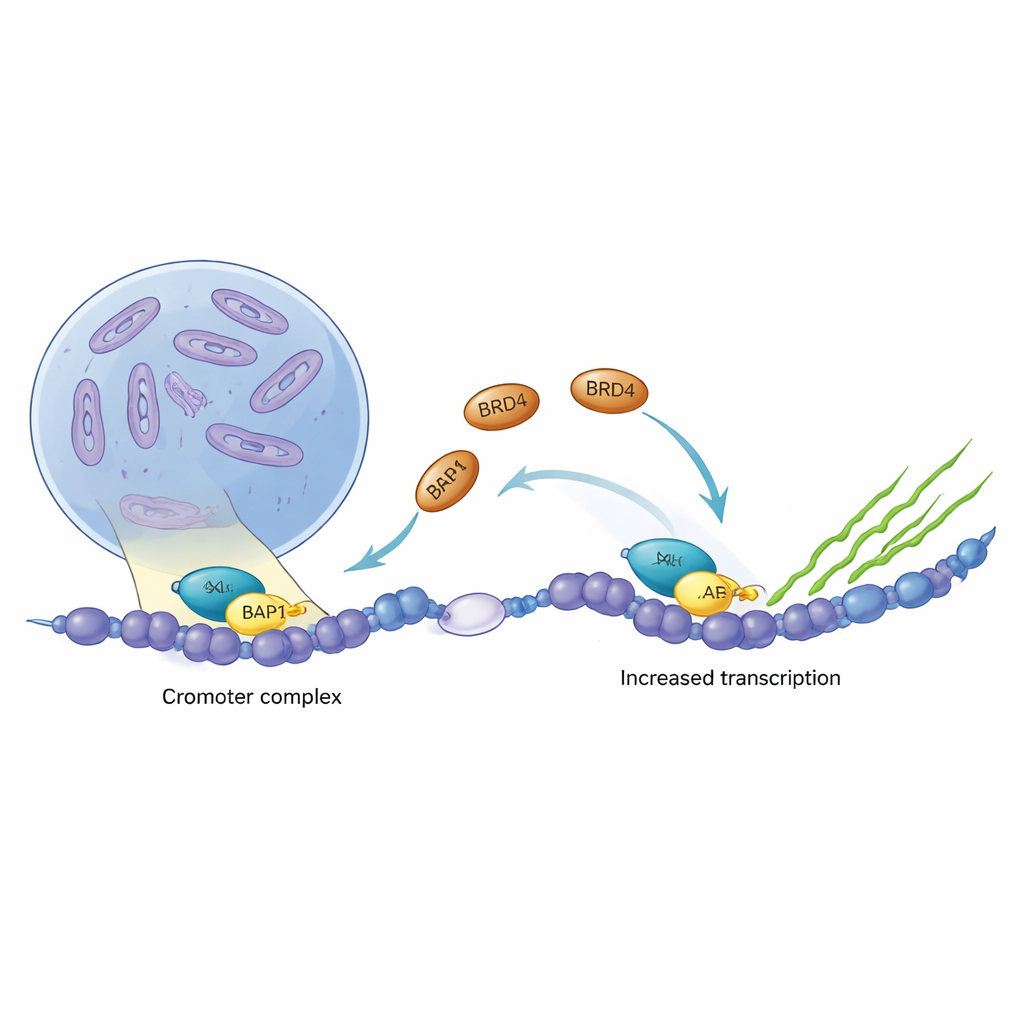
Un partenariat au cœur du contrôle des gènes
ASXL1 fait partie d’un ensemble protéique qui règle finement la compaction de l’ADN, contribuant à décider quels gènes sont silencieux et lesquels sont actifs. BRD4, en revanche, agit comme un puissant interrupteur d’allumage pour la transcription, le processus qui lit les gènes en ARN. En analysant des données de cancers issus de plusieurs types tumoraux, les auteurs ont constaté qu’ASXL1 et BRD4 ont tendance à monter et descendre ensemble, et que BRD4 occupe fréquemment la région d’ADN qui pilote la propre production d’ASXL1. Cette corrélation étroite a suggéré que les deux protéines pourraient collaborer directement pour stimuler des programmes géniques spécifiques dans les cellules cancéreuses.
Zoom sur la poignée de main moléculaire
Pour comprendre comment ASXL1 et BRD4 se connectent, l’équipe a utilisé des outils structuraux à haute résolution et des tests biochimiques. Ils ont montré qu’un court segment à l’intérieur d’ASXL1 s’insère parfaitement dans une gouttière de la région dite extra‑terminale (ET) de BRD4, formant un complexe serré. Des expériences de résonance magnétique nucléaire ont révélé qu’ASXL1 apporte une courte chaîne étendue qui s’apparie avec une partie de BRD4, tandis que des chaînes latérales hydrophobes et chargées s’emboîtent comme les dents d’une fermeture éclair. La mutation d’une seule ou de deux de ces résidus clés d’ASXL1 ou de BRD4 suffisait à abolir en grande partie l’interaction, prouvant que la liaison est hautement spécifique et structurellement bien définie. Fait intrigant, les proches parents d’ASXL1, ASXL2 et ASXL3, utilisent des motifs courts similaires pour se lier à la même gouttière ET, suggérant un code de reconnaissance conservé.
Comment les truncations liées au cancer reconfigurent le complexe
De nombreux patients atteints de cancers myéloïdes présentent des versions tronquées d’ASXL1 qui s’arrêtent à peu près à mi‑protéine. Les auteurs se sont concentrés sur deux formes courantes qui s’arrêtent aux positions 591 et 645. Les deux raccourcissent la protéine mais conservent la région de liaison à BRD4. Lorsque ces variants furent exprimés dans des cellules humaines, ils ont capturé BRD4 aussi efficacement que la protéine normale, à moins qu’un seul résidu de contact critique n’ait été altéré. Des cartes de liaison à l’échelle du génome ont montré que BRD4 est fortement enrichi aux promoteurs où ASXL1 est présent, et cet enrichissement diminue lorsque le contact ASXL1–BRD4 est perturbé. De manière surprenante, la troncation légèrement plus longue (se terminant à 645) recrutait mieux BRD4 sur certains promoteurs que la plus courte, indiquant que la perte de certaines parties d’ASXL1 peut paradoxalement créer un pont plus fort favorisant le cancer vers BRD4.
Un carrefour à trois voies pour l’activation des gènes
De l’éclairage moléculaire aux pistes thérapeutiques
En combinant biologie structurale, cartographie du génome et génomique du cancer, l’étude montre que la région ET de BRD4 s’accroche physiquement à un court motif d’ASXL1 et que cette « poignée de main moléculaire » est essentielle pour guider BRD4 vers les gènes contrôlés par ASXL1. Les truncations d’ASXL1 associées au cancer non seulement préservent cette interaction mais, dans certains cas, renforcent le recrutement de BRD4 et ajoutent la capacité de lier MLL3/4, amplifiant l’activation génique. Parce que ces interactions reposent sur une surface bien définie de BRD4 et un court segment d’ASXL1, elles fournissent une feuille de route claire pour concevoir de petites molécules capables de perturber sélectivement le lien ASXL1–BRD4, atténuant potentiellement les programmes géniques oncogènes tout en épargnant d’autres fonctions de BRD4.
Citation: Selvam, K., Lu, S., Messmer, C. et al. Recruitment of BRD4 to the ASXL1 genomic targets depends on the extra-terminal domain of BRD4. Nat Commun 17, 2852 (2026). https://doi.org/10.1038/s41467-026-69565-z
Mots-clés: régulation épigénétique, BRD4, ASXL1, complexes de chromatine, transcription cancéreuse