Clear Sky Science · zh
用于无串扰全光神经干预的有源像素功率控制
在不干扰大脑的情况下照亮它
现代神经科学常常依赖光来同时观察和控制脑细胞的活动。这一强大理念——用激光读取与写入神经信号——有望深入揭示大脑如何产生行为与疾病。但问题在于:用于拍摄神经活动的光,可能会意外触发科学家用来控制神经元的光敏开关,从而模糊实验结果。本文介绍了一种方法,能够在图像的每个微小点上精确调节激光光强,使研究人员可以在不相互干扰的情况下同时监测和操纵大脑。
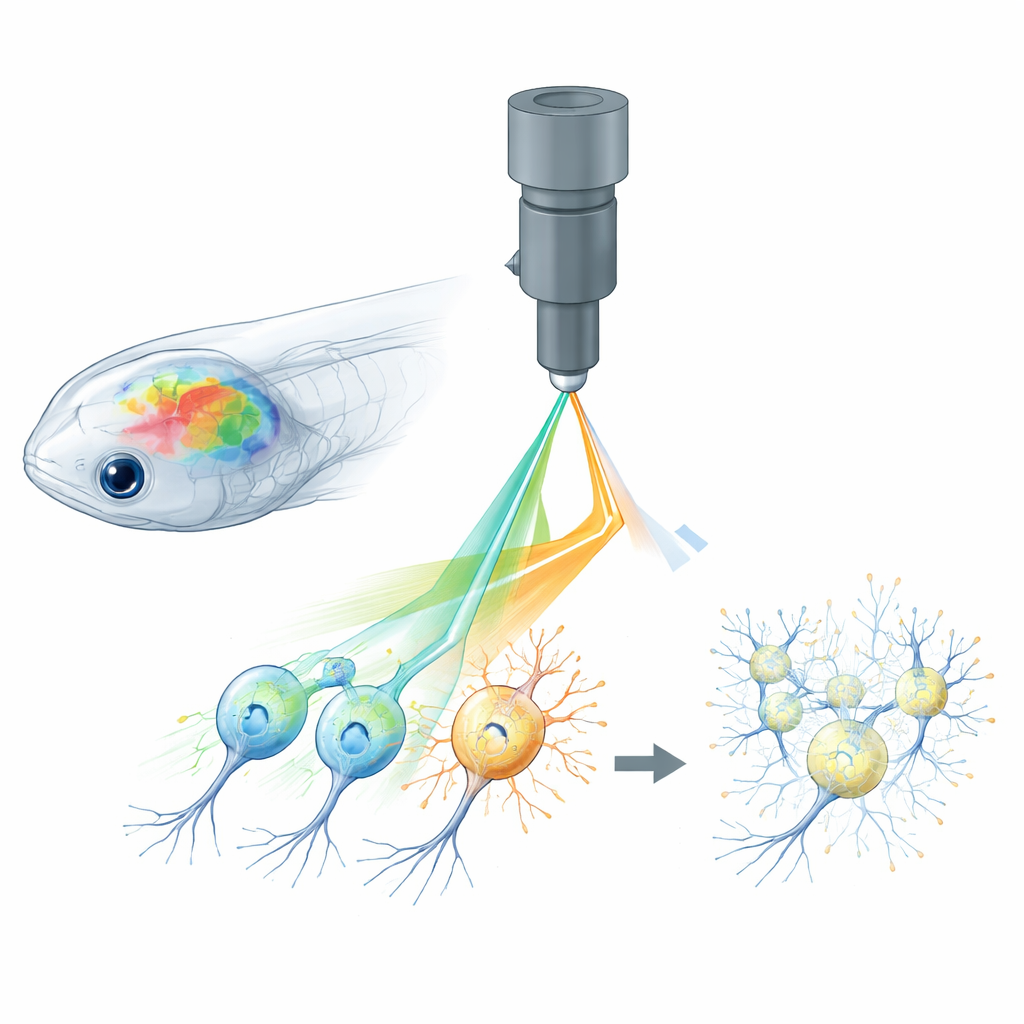
为什么观察与控制神经元很困难
全光神经科学结合了两类工具:在神经元活动时发光的传感器,以及能让科学家打开或关闭神经元的光激活蛋白。在斑马鱼、果蝇和小鼠等小型动物中,双光子显微镜可以将激光光束聚焦到大脑深处,三维读取整个细胞网络;而全息光刺激可以以极高精度激活特定神经元。然而,用于读取荧光钙信号的同一激光,可能会无意间激活用于控制的光门通道。这种“串扰”意味着成像过程本身会改变大脑的活动,使真实反应与实验产生的伪影难以区分。
像素级的精确功率控制
作者提出了他们称之为有源像素功率控制(APPC)的方法来解决这一问题。他们不是在图像的每个点上使用相同的激光功率,而是用一个极快的光调制器在扫描时为每个微小像素调整激光强度。在实验前,通过成像与这些光敏蛋白融合的标准荧光标记来记录光激活通道的位置。根据该地图,他们构建了定制的功率分布:与光敏区域重叠的像素使用更低功率,而其他像素保持用于获取清晰钙信号的较高功率。调制器与显微镜的快速扫描镜实时同步更新,使激光功率在大脑中以单像素精度被塑形。
在微小透明大脑中测试该方法
为了验证APPC是否真正防止了不必要的激活,研究团队在幼年斑马鱼中开展实验,这些小而透明的大脑非常适合全脑成像。他们使用常用的光遗传通道(如ChR2和一种红移变体ChrimsonR)以及绿色钙传感器,全部由单一飞秒激光驱动。通过在表达光敏通道的神经元上有选择性地降低成像功率,同时在其他区域保持正常功率,研究者们找到了一个约5毫瓦的“最佳点”:此时成像仍能产生可靠的钙信号,但不再在那些神经元中引发额外的人工活动。重要的是,他们还证明这种局部功率降低能阻止串扰效应向下游神经元扩散,从而保留回路的真实连通性和信号流动。
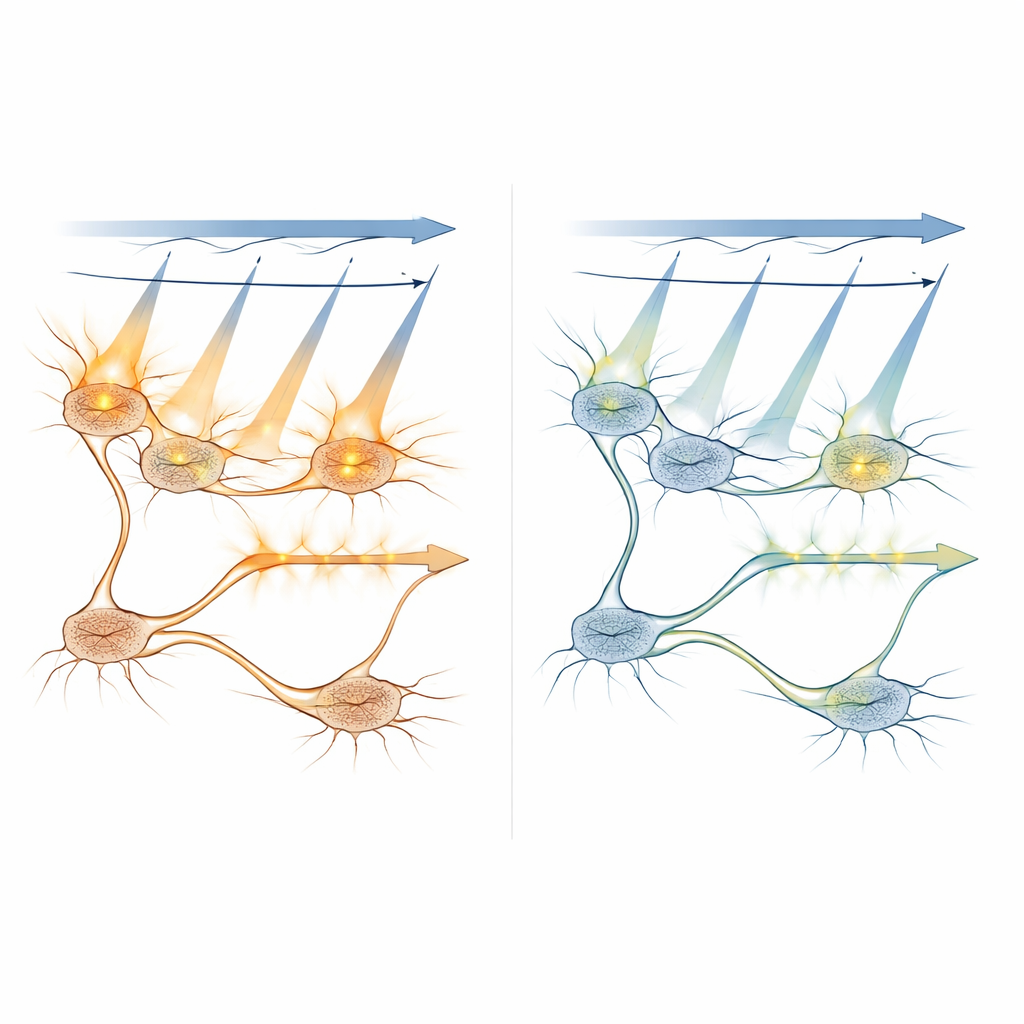
探索光如何传播并激活细胞
研究者将计算模型与体内测量相结合,以理解在不同条件下扫描光如何激活光敏蛋白。他们模拟了激光扫过神经元时单个分子被打开的频率,以及这种概率随激光功率、曝光时间和焦点与细胞中心距离的变化。实验证实,离焦平面大约超过8–10微米时,几乎不对不必要的激活产生贡献,这有助于确定三维扫描中成像层之间的安全间距。他们还测试了一种策略,即将明亮的成像光限制在细胞体的内侧——远离嵌入膜上的光门通道——结果表明,这可以进一步减少串扰,尽管会降低信号强度。
让精密大脑实验更易普及
除了提供一个巧妙的技术解决方案外,APPC还有实际优势。它可与许多实验室已有的标准双光子显微镜兼容,仅需一台激光,且不要求使用特殊改造的蛋白或完美的颜色分离。作者认为,APPC可以扩展到更复杂的系统,包括使用两台激光器的设置,在那里它可与通过波长分离刺激与成像的其它策略互补。通过为每种神经元类型和实验经验性地调节“近乎无串扰”的功率水平,APPC为研究特定细胞如何影响全脑活动提供了通用方案,而不会意外引入额外信号。通俗地说,它让科学家准确调暗那些会蒙蔽自身仪器的光,从而澄清对活体大脑活动的观察。
引用: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
关键词: 光遗传学, 双光子成像, 神经回路, 斑马鱼大脑, 有源像素功率控制