Clear Sky Science · fr
Contrôle actif de la puissance par pixel pour une interrogation neuronale tout-optique sans diaphonie
Éclairer le cerveau sans le perturber
La neuroscience moderne repose souvent sur la lumière pour observer et contrôler l’activité des cellules nerveuses. Cette idée puissante — utiliser des lasers pour lire et modifier les signaux neuronaux — promet une compréhension profonde de la façon dont le cerveau génère comportement et maladie. Mais il y a un problème : la même lumière utilisée pour imager l’activité neurale peut involontairement activer les mêmes interrupteurs sensibles à la lumière que les chercheurs emploient pour contrôler les neurones, brouillant ainsi les résultats. Cet article présente une méthode pour ajuster précisément la puissance du laser à chaque point minuscule de l’image afin que les chercheurs puissent surveiller et manipuler le cerveau simultanément, sans que les deux opérations n’interfèrent.
Pourquoi il est difficile de regarder et de contrôler les neurones
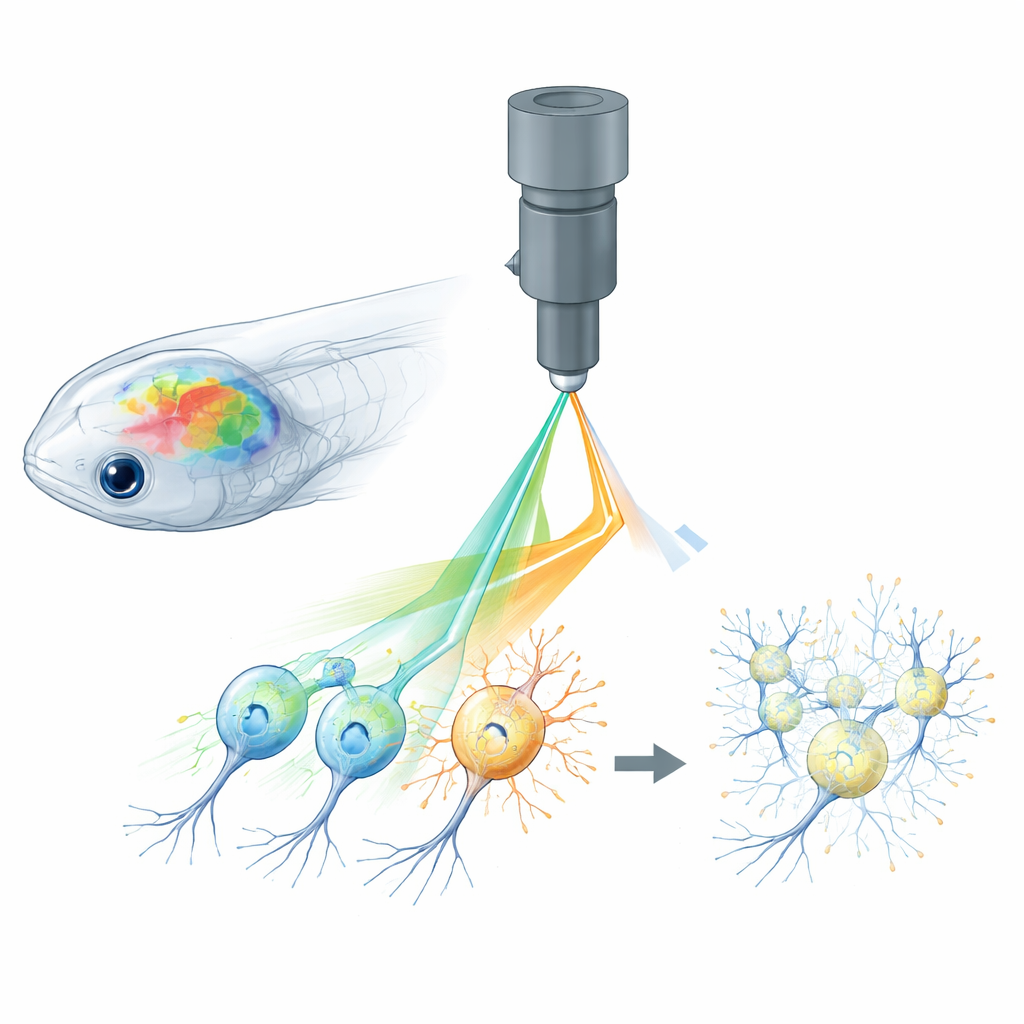
La neuroscience tout-optique combine deux outils : des capteurs fluorescents qui signalent l’activité neuronale et des protéines activées par la lumière qui permettent d’allumer ou d’éteindre les neurones. Chez de petits animaux comme le poisson zèbre, la drosophile et la souris, les microscopes biphotoniques peuvent focaliser la lumière laser profondément dans le cerveau pour lire des réseaux entiers de cellules en 3D, tandis que des motifs holographiques stimulent des neurones choisis avec une grande précision. Cependant, le même laser utilisé pour lire les signaux calciques des capteurs fluorescents peut activer par inadvertance les canaux sensibles à la lumière employés pour le contrôle. Cette « diaphonie » signifie que l’imagerie modifie elle-même l’activité cérébrale, estompant la frontière entre réponses authentiques et artefacts induits par l’expérience.
Contrôle de puissance au niveau du pixel
Les auteurs s’attaquent à ce problème avec ce qu’ils appellent le contrôle actif de la puissance par pixel, ou APPC. Plutôt que d’appliquer la même puissance laser à chaque point de l’image, ils utilisent un modulateur de lumière très rapide pour ajuster l’intensité du laser pour chaque pixel minuscule pendant le balayage du faisceau. Avant les expériences, ils enregistrent où se trouvent les canaux activés par la lumière en imageant un tag fluorescent standard fusionné à ces protéines. À partir de cette carte, ils construisent un motif de puissance personnalisé : les pixels qui chevauchent des régions sensibles à la lumière reçoivent beaucoup moins de puissance, tandis que les autres conservent la puissance plus élevée nécessaire pour des signaux calciques clairs. Le modulateur se met à jour en temps réel, synchronisé avec les miroirs de balayage rapides du microscope, de sorte que la puissance laser est sculptée à travers le cerveau avec une précision au niveau du pixel unique.
Tester la méthode dans un tout petit cerveau transparent
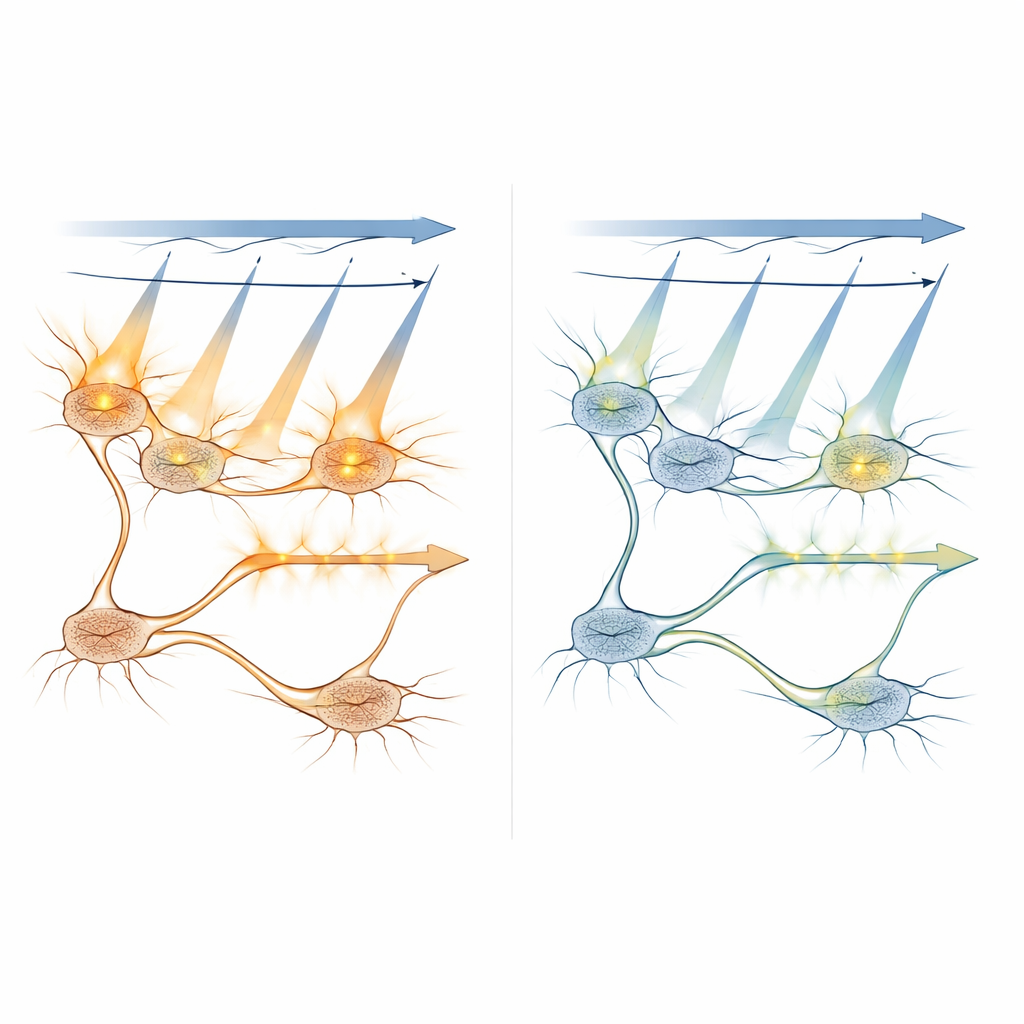
Pour vérifier si l’APPC empêche vraiment l’activation indésirable, l’équipe a travaillé sur des larves de poisson zèbre, dont les petits cerveaux transparents sont idéaux pour l’imagerie de l’ensemble du cerveau. Ils ont utilisé des canaux optogénétiques populaires (comme ChR2 et une variante décalée vers le rouge appelée ChrimsonR) avec un capteur calcique vert, le tout alimenté par un seul laser femtoseconde. En abaissant systématiquement la puissance d’imagerie uniquement sur les neurones exprimant des canaux sensibles à la lumière, tout en maintenant une puissance normale ailleurs, ils ont trouvé un « point idéal » autour de 5 milliwatts où l’imagerie produisait encore des signaux calciques fiables mais n’entraînait plus d’activité supplémentaire artificielle dans ces neurones. Fait important, ils ont montré que cette réduction locale de puissance empêchait aussi les effets de diaphonie de se propager vers les neurones en aval, préservant ainsi la connectivité et le flux de signal réels du circuit.
Explorer la diffusion de la lumière et l’activation cellulaire
Les chercheurs ont combiné modèles informatiques et mesures in vivo pour comprendre comment la lumière de balayage active les protéines sensibles à la lumière dans différentes conditions. Ils ont simulé la fréquence à laquelle des molécules individuelles seraient activées au passage du laser sur un neurone, et comment cette probabilité variait avec la puissance du laser, le temps d’exposition et la distance du point focal par rapport au centre de la cellule. Les expériences ont confirmé que des plans hors foyer à plus d’environ 8–10 micromètres contribuent peu à l’activation indésirable, aidant à définir un espacement sûr entre les couches d’imagerie dans les balayages 3D. Ils ont aussi testé une stratégie qui limite la lumière d’imagerie intense à la partie interne du soma — éloignée de la membrane où se trouvent les canaux sensibles à la lumière — montrant que cela peut encore réduire la diaphonie, même si cela diminue la force du signal.
Rendre les expériences cérébrales de précision plus accessibles
Au-delà d’une astuce technique ingénieuse, l’APPC présente des avantages pratiques. Elle fonctionne avec des microscopes biphotoniques standard déjà répandus dans de nombreux laboratoires, n’utilise qu’un seul laser et ne nécessite pas de protéines spécialement conçues ni une séparation parfaite des couleurs entre les outils. Les auteurs soutiennent que l’APPC peut être étendue à des systèmes plus complexes, y compris des configurations à deux lasers, où elle complèterait d’autres stratégies séparant stimulation et imagerie par longueur d’onde. En ajustant empiriquement le niveau de puissance « quasi sans diaphonie » pour chaque type de neurone et chaque expérience, l’APPC fournit une recette générale pour étudier comment des cellules spécifiques influent sur l’activité à l’échelle du cerveau sans déclencher accidentellement des signaux supplémentaires. Dit autrement, elle permet aux scientifiques d’atténuer la lumière exactement là où elle aveuglerait leurs propres instruments, clarifiant la vue du cerveau vivant en action.
Citation: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Mots-clés: optogénétique, imagerie biphotonique, circuits neuronaux, cerveau de poisson zèbre, contrôle actif de la puissance par pixel