Clear Sky Science · es
Control activo de potencia por píxel para una interrogación neural totalmente óptica sin diafonía
Iluminar el cerebro sin alterarlo
La neurociencia moderna a menudo se basa en la luz tanto para observar como para controlar la actividad de las células cerebrales. Esta idea poderosa —usar láseres para leer y escribir señales neuronales— promete una profunda comprensión de cómo los cerebros generan comportamiento y enfermedad. Pero hay una pega: la propia luz utilizada para tomar imágenes de la actividad neural puede activar accidentalmente los mismos interruptores sensibles a la luz que los científicos usan para controlar neuronas, enturbiando los resultados. Este artículo presenta una manera de ajustar cuidadosamente la luz del láser en cada punto diminuto de la imagen para que los investigadores puedan monitorizar y manipular el cerebro al mismo tiempo, sin que ambas tareas se interfieran.
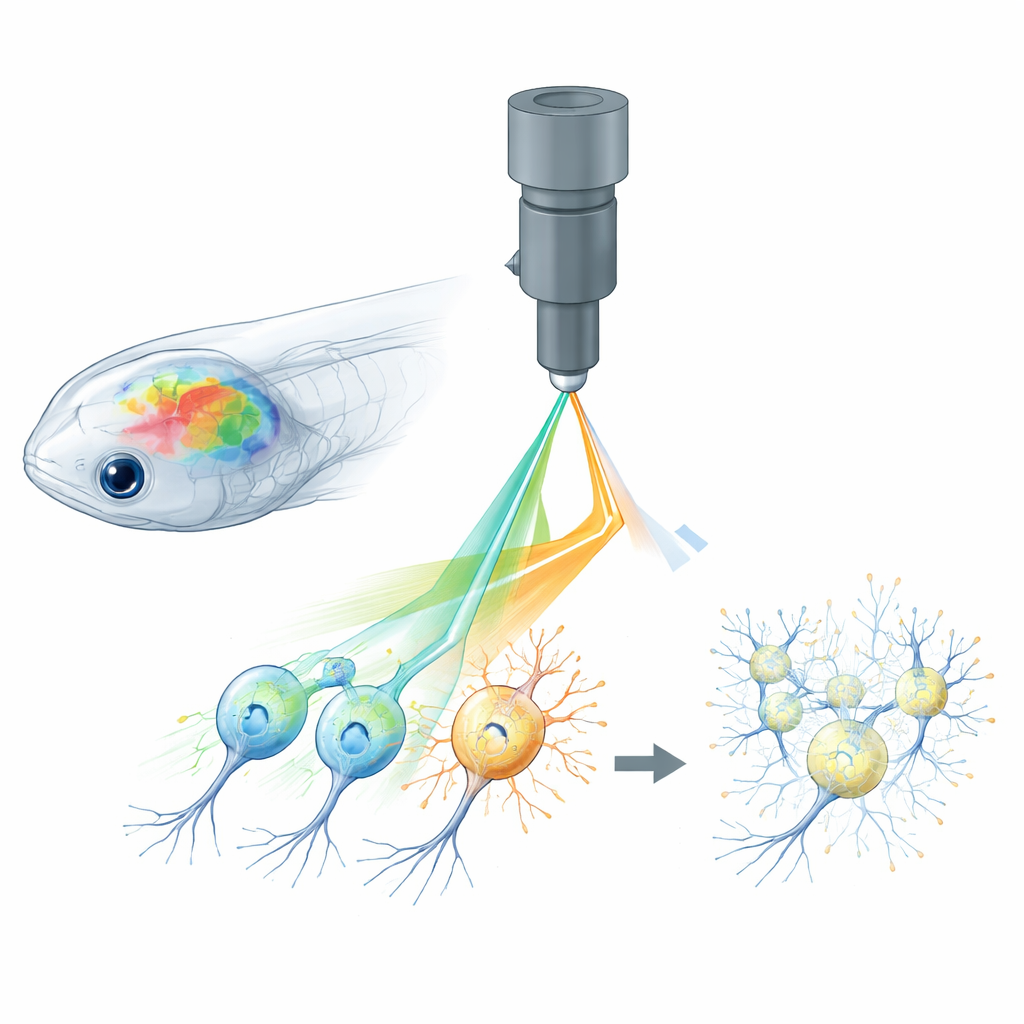
Por qué es difícil observar y controlar neuronas
La neurociencia totalmente óptica combina dos herramientas: sensores fluorescentes que informan cuándo las neuronas están activas y proteínas activadas por luz que permiten a los científicos encender o apagar neuronas. En animales pequeños como el pez cebra, la mosca de la fruta y el ratón, los microscopios de dos fotones pueden enfocar luz láser en profundidad para leer redes completas de células en 3D, mientras que patrones holográficos de luz estimulan neuronas elegidas con precisión. Sin embargo, el mismo láser usado para leer señales de calcio de sensores fluorescentes puede activar de forma involuntaria los canales activados por luz empleados para el control. Esta “diafonía” significa que el propio proceso de imagen altera la actividad cerebral, difuminando la línea entre respuestas genuinas y artefactos creados por el experimento.
Control de potencia puntual a nivel de píxel
Los autores abordan este problema con lo que llaman control activo de potencia por píxel, o APPC. En lugar de iluminar con la misma potencia en cada punto de la imagen, emplean un modulador de luz muy rápido para ajustar la intensidad del láser en cada píxel diminuto mientras el haz escanea. Antes de los experimentos, registran dónde se localizan los canales activados por luz mediante la imagen de una etiqueta fluorescente estándar fusionada a esas proteínas. A partir de este mapa, construyen un patrón de potencia personalizado: los píxeles que se solapan con regiones sensibles a la luz reciben mucha menos potencia, mientras que otros píxeles mantienen la potencia más alta necesaria para obtener señales de calcio claras. El modulador se actualiza en tiempo real, sincronizado con los espejos de escaneo rápidos del microscopio, de modo que la potencia del láser se esculpe a través del cerebro con precisión de un solo píxel.
Probando el método en un cerebro diminuto y transparente
Para comprobar si APPC realmente evita la activación no deseada, el equipo trabajó en larvas de pez cebra, cuyos cerebros pequeños y transparentes son ideales para la imagen de todo el cerebro. Usaron canales optogenéticos populares (como ChR2 y una variante desplazada al rojo llamada ChrimsonR) junto con un sensor de calcio verde, todo impulsado por un único láser de femtosegundos. Reduciendo sistemáticamente la potencia de imagen solo en las neuronas que expresaban canales sensibles a la luz, mientras mantenían la potencia normal en otras áreas, encontraron un “punto óptimo” alrededor de 5 milivatios donde la imagen todavía producía señales de calcio fiables pero ya no provocaba actividad artificial adicional en esas neuronas. Es importante que mostraron que esta reducción local de potencia también evitó que los efectos de diafonía se propagasen a neuronas aguas abajo, preservando el cableado real y el flujo de señales del circuito.
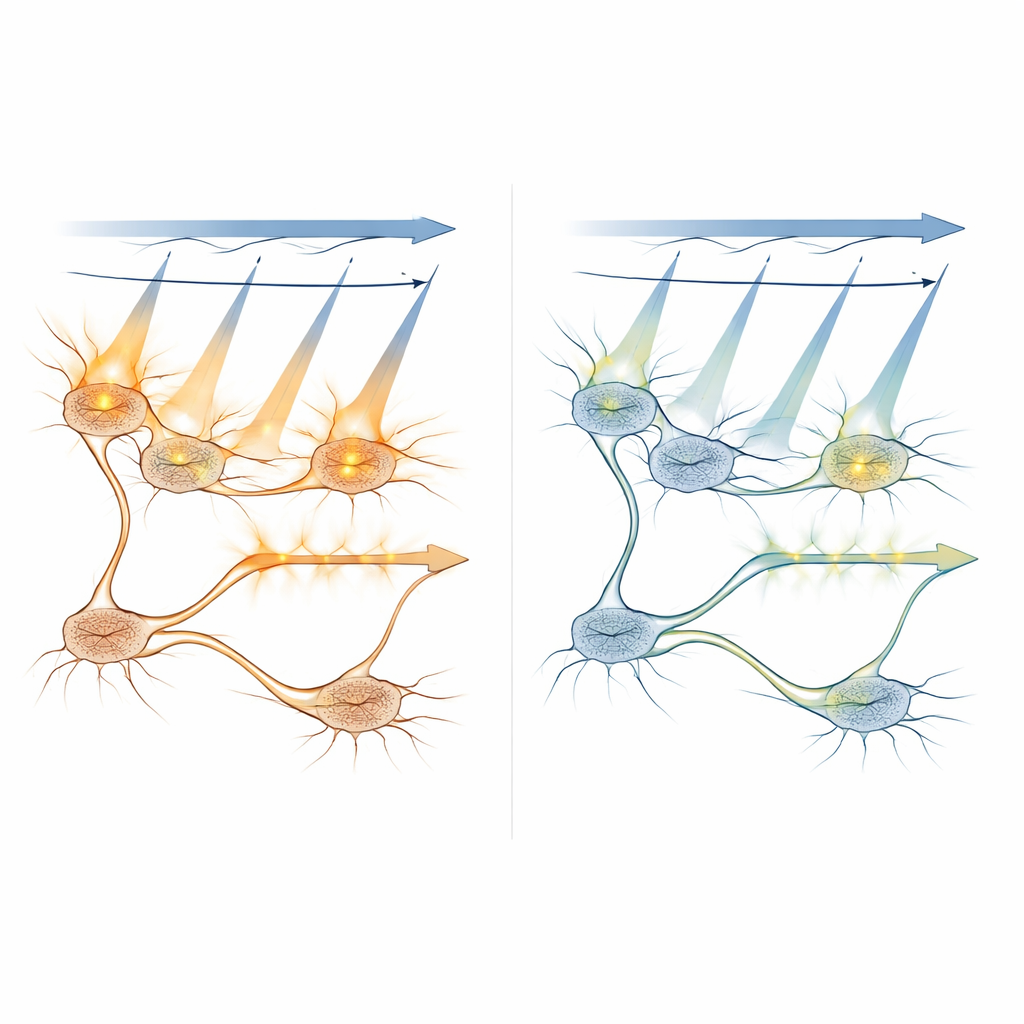
Explorando cómo la luz se propaga y activa las células
Los investigadores combinaron modelos por ordenador con medidas in vivo para entender cómo la luz de escaneo activa proteínas sensibles en distintas condiciones. Simularon con qué frecuencia moléculas individuales se activarían mientras el láser barría una neurona, y cómo cambiaba esa probabilidad con la potencia del láser, el tiempo de exposición y la distancia del punto focal al centro de la célula. Los experimentos confirmaron que planos fuera de foco a más de unos 8–10 micrómetros contribuyen poco a la activación indeseada, lo que ayuda a definir el espaciado seguro entre capas de imagen en exploraciones 3D. También probaron una estrategia que restringe la luz de imagen brillante a la parte interna del soma—lejos de la membrana donde se sitúan los canales activados por luz—mostrando que esto puede reducir aún más la diafonía, aunque disminuye la intensidad de la señal.
Haciendo los experimentos cerebrales de precisión más accesibles
Más allá de ofrecer una solución técnica ingeniosa, APPC tiene ventajas prácticas. Funciona con microscopios de dos fotones estándar que ya son comunes en muchos laboratorios, necesita solo un láser y no requiere proteínas especialmente diseñadas ni una separación cromática perfecta entre herramientas. Los autores sostienen que APPC puede extenderse a sistemas más complejos, incluidos montajes con dos láseres, donde complementaría otras estrategias que separan estimulación e imagen por longitud de onda. Al ajustar empíricamente el nivel de potencia “casi libre de diafonía” para cada tipo de neurona y experimento, APPC proporciona una receta general para estudiar cómo células específicas influyen en la actividad a escala cerebral sin provocar señales extra por accidente. En términos cotidianos, permite a los científicos atenuar exactamente la luz donde ésta de otro modo cegaría sus propios instrumentos, despejando la vista del cerebro vivo en acción.
Cita: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Palabras clave: optogenética, imagen por dos fotones, circuitos neuronales, cerebro de pez cebra, control activo de potencia por píxel