Clear Sky Science · pl
Aktywna kontrola mocy piksela dla bezzakłóceniowego, w pełni optycznego badania neuronów
Oświetlanie mózgu bez jego zakłócania
Współczesna neurobiologia często polega na świetle zarówno do obserwacji, jak i kontroli aktywności komórek mózgowych. Ten potężny pomysł — użycie laserów do odczytywania i zapisywania sygnałów neuronowych — obiecuje głębokie zrozumienie mechanizmów stojących za zachowaniem i chorobami. Jest jednak jedno „ale”: samo światło wykorzystywane do obrazowania aktywności neuronów może przypadkowo uruchamiać te same światłoczułe przełączniki, których naukowcy używają do kontrolowania neuronów, zacierając wyniki. W artykule przedstawiono metodę pozwalającą precyzyjnie dostosować światło lasera w każdym drobnym punkcie obrazu, tak aby badacze mogli jednocześnie obserwować i manipulować mózgiem bez wzajemnego zakłócania tych dwóch zadań.
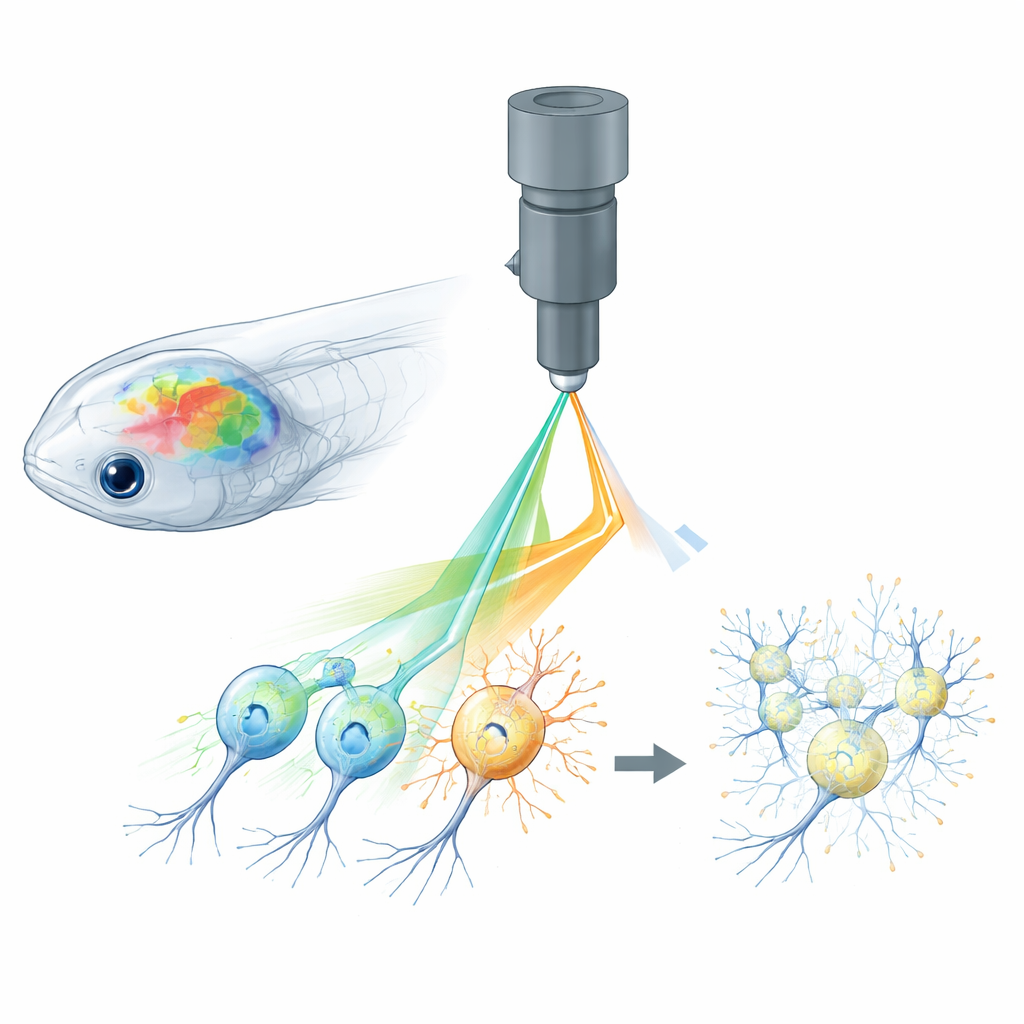
Dlaczego obserwacja i kontrola neuronów jest trudna
W pełni optyczna neurobiologia łączy dwa narzędzia: fluorescencyjne sensory raportujące, kiedy neurony są aktywne, oraz światłoczułe białka pozwalające włączać lub wyłączać neurony. W małych zwierzętach, takich jak danio pręgowany, muszki owocowe czy myszy, mikroskopy dwu-fotonowe mogą ogniskować światło lasera głęboko w mózgu, aby odczytywać sieci komórek w 3D, podczas gdy holograficzne wzory światła stymulują wybrane neurony z precyzją. Jednak ten sam laser używany do odczytu sygnałów wapniowych z fluoroscencyjnych sensorów może mimowolnie aktywować kanały sterowane światłem używane do manipulacji. Taki „prześwietlający wpływ” (cross-talk) oznacza, że proces obrazowania sam zmienia aktywność mózgu, zacierając granicę między prawdziwymi odpowiedziami a artefaktami eksperymentalnymi.
Precyzyjna kontrola mocy na poziomie piksela
Autorzy rozwiązują ten problem za pomocą rozwiązania nazwanego aktywną kontrolą mocy piksela (APPC). Zamiast stosować jednakową moc lasera na każdym punkcie obrazu, używają bardzo szybkiego modulatora światła, który dostosowuje intensywność lasera dla każdego małego piksela w miarę skanowania wiązki. Przed eksperymentami rejestrują, gdzie znajdują się kanały wrażliwe na światło, obrazując standardowy znacznik fluorescencyjny złączony z tymi białkami. Na podstawie tej mapy konstruują niestandardowy wzorzec mocy: piksele nachodzące na obszary światłoczułe otrzymują znacznie mniejszą moc, podczas gdy inne piksele zachowują wyższą moc potrzebną do uzyskania wyraźnych sygnałów wapniowych. Modulator aktualizuje się w czasie rzeczywistym, zsynchronizowany z szybkim ruchem luster skanujących mikroskopu, tak że moc lasera jest rzeźbiona w mózgu z precyzją pojedynczego piksela.
Testowanie metody w małym, przezroczystym mózgu
Aby sprawdzić, czy APPC rzeczywiście zapobiega niechcianej aktywacji, zespół pracował na larwach danio pręgowanego, których małe, przezroczyste mózgi są idealne do obrazowania całego mózgu. Wykorzystali popularne kanały optogenetyczne (takie jak ChR2 i czerwonoprzesuwny wariant ChrimsonR) wraz z zielonym sensorem wapniowym, wszystko zasilane jednym femtosekundowym laserem. Systematycznie obniżając moc obrazowania jedynie na neuronach wyrażających kanały światłoczułe, przy zachowaniu normalnej mocy w innych miejscach, znaleźli „optymalny punkt” wokół 5 miliwatów, gdzie obrazowanie wciąż dawało wiarygodne sygnały wapniowe, lecz przestało wywoływać dodatkową, sztuczną aktywność w tych neuronach. Co ważne, wykazali, że to lokalne zmniejszenie mocy zapobiegało także rozprzestrzenianiu się efektów cross-talk na neurony położone dalej w obwodzie, zachowując prawdziwe połączenia i przepływ sygnału w sieci.
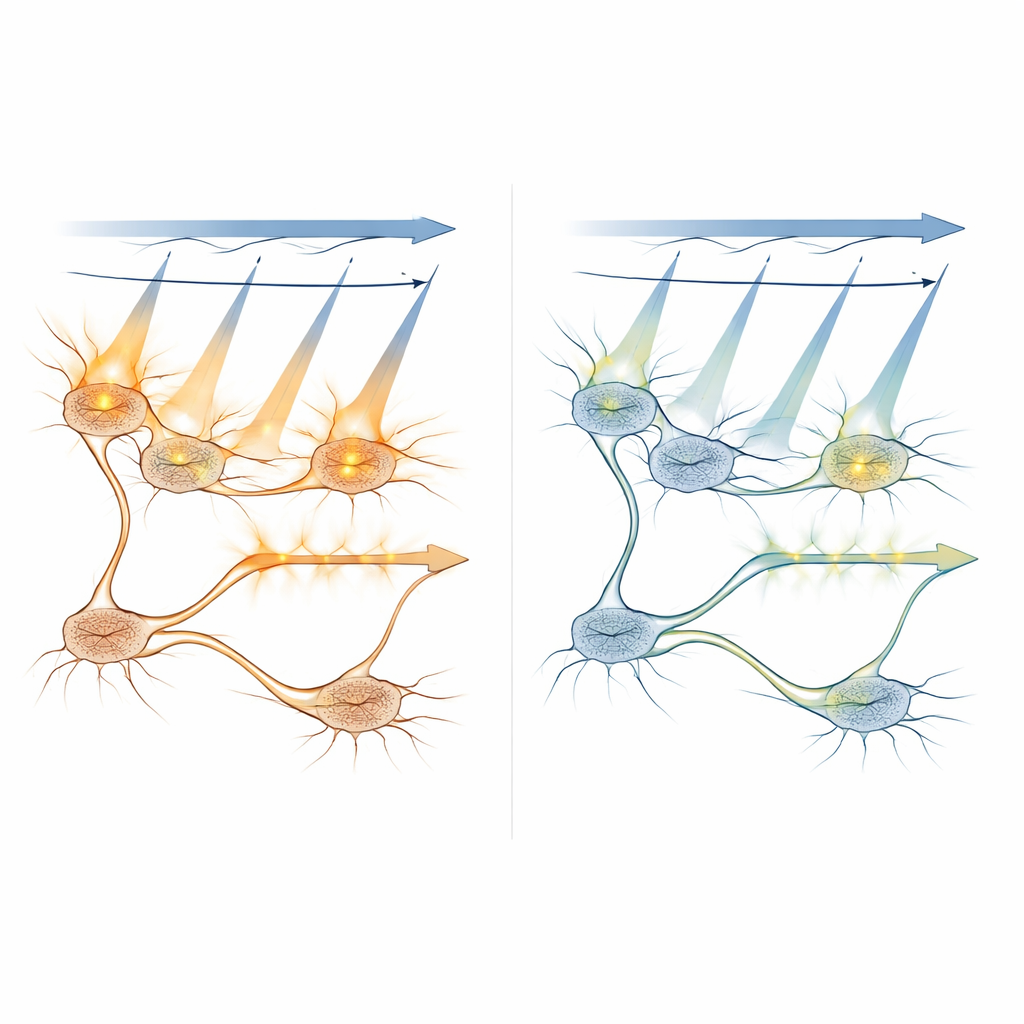
Badanie, jak światło rozchodzi się i aktywuje komórki
Naukowcy połączyli modele komputerowe z pomiarami in vivo, aby zrozumieć, jak skanujące światło aktywuje białka światłoczułe w różnych warunkach. Symulowali, jak często pojedyncze cząsteczki byłyby włączane w miarę przesuwania lasera po neuronie oraz jak prawdopodobieństwo to zmieniało się wraz z mocą lasera, czasem ekspozycji i odległością punktu ogniskowania od środka komórki. Eksperymenty potwierdziły, że płaszczyzny poza ogniskiem oddalone o więcej niż około 8–10 mikrometrów wnoszą niewielki wkład do niechcianej aktywacji, co pomaga określić bezpieczne odstępy między warstwami obrazowania w skanach 3D. Przetestowali także strategię ograniczającą jasne światło obrazujące do wnętrza ciała komórki — z dala od błony, gdzie znajdują się kanały sterowane światłem — wykazując, że może to dodatkowo zredukować cross-talk, choć kosztem mniejszej siły sygnału.
Ułatwianie precyzyjnych badań mózgu
Poza sprytnym rozwiązaniem technicznym, APPC ma praktyczne zalety. Działa ze standardowymi mikroskopami dwu-fotonowymi, które są już powszechne w wielu laboratoriach, wymaga tylko jednego lasera i nie potrzebuje specjalnie zmodyfikowanych białek ani idealnego rozdzielenia barw między narzędziami. Autorzy twierdzą, że APPC można rozszerzyć na bardziej złożone systemy, w tym konfiguracje z dwoma laserami, gdzie uzupełniałoby inne strategie rozdzielania stymulacji i obrazowania według długości fali. Poprzez empiryczne dobranie „niemal bez cross-talk” poziomu mocy dla każdego typu neuronu i eksperymentu, APPC daje ogólną receptę na badanie, jak konkretne komórki wpływają na aktywność w całym mózgu, nie wywołując przypadkowo dodatkowych sygnałów. Mówiąc prościej: pozwala naukowcom przyciemnić światło dokładnie tam, gdzie w przeciwnym razie oślepiłoby własne instrumenty, oczyszczając widok działającego, żywego mózgu.
Cytowanie: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Słowa kluczowe: opto-genetyka, mikroskopia dwu-fotonowa, obwody nerwowe, Mózg danio pręgowanego, aktywna kontrola mocy piksela