Clear Sky Science · nl
Actieve pixelvermogensregeling voor crosstalk-vrije volledig-optische neurale interrogatie
Licht werpen op het brein zonder het te verstoren
De moderne neurowetenschap gebruikt vaak licht om zowel de activiteit van hersencellen te observeren als te sturen. Dit krachtige idee — lasers gebruiken om neurale signalen te lezen en te schrijven — belooft diepgaand inzicht in hoe breinen gedrag en ziekte voortbrengen. Er is echter een kink in de kabel: het licht waarmee men neurale activiteit afbeeldt, kan per ongeluk dezelfde lichtgevoelige schakelaars activeren die onderzoekers gebruiken om neuronen te beheersen, waardoor de resultaten vertroebeld raken. Dit artikel introduceert een methode om het laserlicht per klein beeldpunt zorgvuldig aan te passen, zodat onderzoekers het brein tegelijk kunnen monitoren en manipuleren zonder dat de twee taken elkaar beïnvloeden.
Waarom neuronen bekijken en sturen zo lastig is
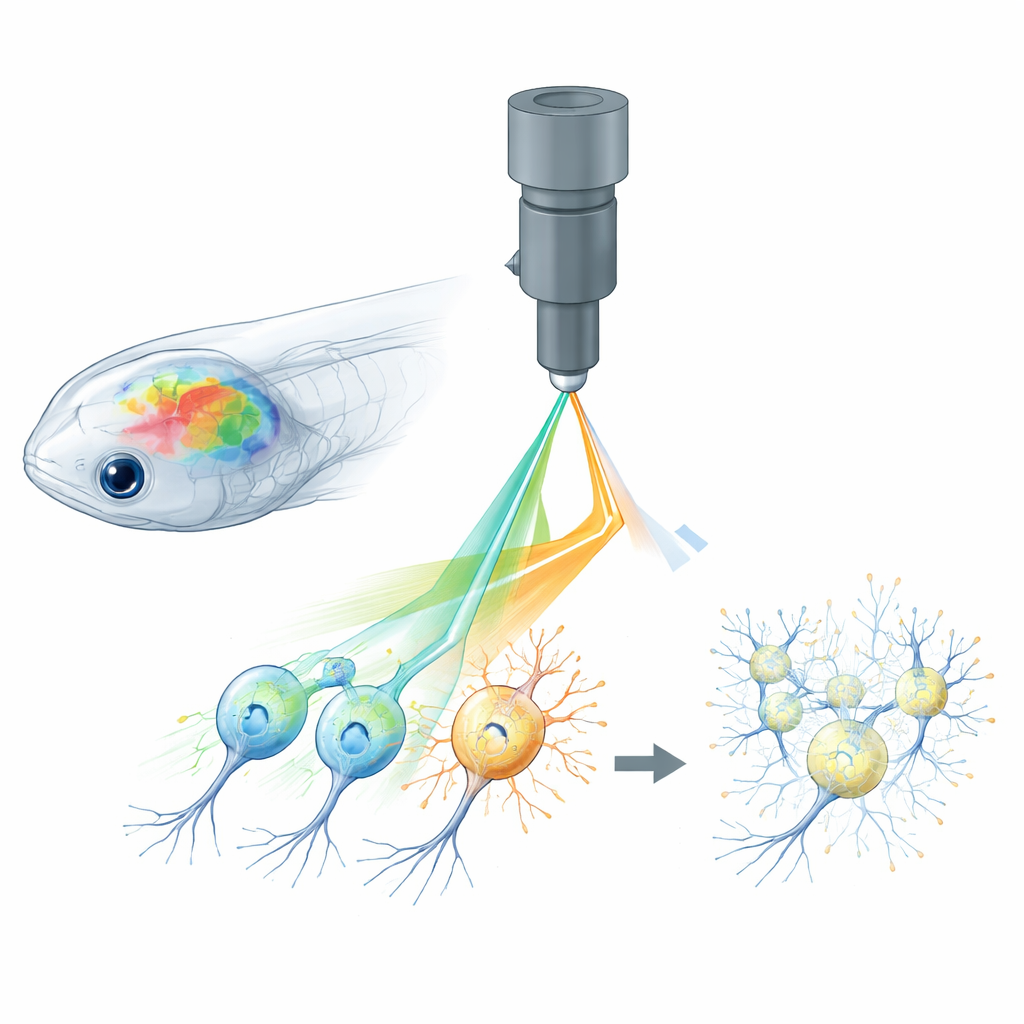
Volledig-optische neurowetenschap combineert twee instrumenten: fluorescerende sensoren die melden wanneer neuronen actief zijn, en licht-geactiveerde eiwitten waarmee onderzoekers neuronen aan of uit kunnen zetten. Bij kleine dieren zoals zebravissen, fruitvliegen en muizen kunnen twee-fotonmicroscopen laserlicht diep in het brein focussen om netwerken van cellen driedimensionaal uit te lezen, terwijl holografische lichtpatronen geselecteerde neuronen met precisie stimuleren. Toch kan hetzelfde laserlicht dat calciumsignalen van fluorescerende sensoren leest, onbedoeld de lichtgestuurde kanalen voor controle activeren. Deze “crosstalk” betekent dat het afbeeldingsproces zelf de hersenactiviteit verandert, waardoor het verschil tussen echte responsen en door het experiment veroorzaakte artefacten vervaagt.
Puntprecisie in vermogensregeling op pixelniveau
De auteurs pakken dit probleem aan met wat zij actieve pixelvermogensregeling noemen, of APPC. In plaats van op elk beeldpunt hetzelfde laservermogen te gebruiken, passen ze met een zeer snelle lichtmodulator de laserintensiteit aan voor elk klein pixel terwijl de bundel scant. Voorafgaand aan experimenten bepalen ze waar de lichtgeactiveerde kanalen zitten door een standaard fluorescerende tag aan die eiwitten te laten zien. Vanuit deze kaart construeren ze een aangepast vermogenspatroon: pixels die samenvallen met lichtgevoelige gebieden krijgen veel minder vermogen, terwijl andere pixels het hogere vermogen behouden dat nodig is voor heldere calciumsignalen. De modulator werkt in realtime, gesynchroniseerd met de snelle scanspiegels van de microscoop, zodat het laservermogen over het brein heen in detail wordt gevormd met precisie op enkel-pixelniveau.
De methode testen in een klein transparant brein
Om te beoordelen of APPC werkelijk ongewenste activering voorkomt, werkte het team met larvale zebravissen, waarvan de kleine, doorzichtige hersenen ideaal zijn voor beeldvorming van het hele brein. Ze gebruikten gangbare optogenetische kanalen (zoals ChR2 en een naar het rode verschoven variant genaamd ChrimsonR) samen met een groene calciumsensor, allemaal aangedreven door één femtoseconde-laser. Door het afbeeldingsvermogen systematisch alleen te verlagen op neuronen die lichtgevoelige kanalen uitdrukten, terwijl het normale vermogen elders werd aangehouden, vonden ze een “sweet spot” rond 5 milliwatt waarbeelden nog steeds betrouwbare calciumsignalen opleverden maar niet langer extra, kunstmatige activiteit in die neuronen veroorzaakten. Belangrijk is dat ze aantonen dat deze lokale vermogensverlaging ook verhindert dat crosstalk-effecten zich verspreiden naar downstream-neuronen, waardoor de werkelijke bedrading en signaalstroom van het circuit behouden blijft.
Onderzoeken hoe licht zich verspreidt en cellen activeert
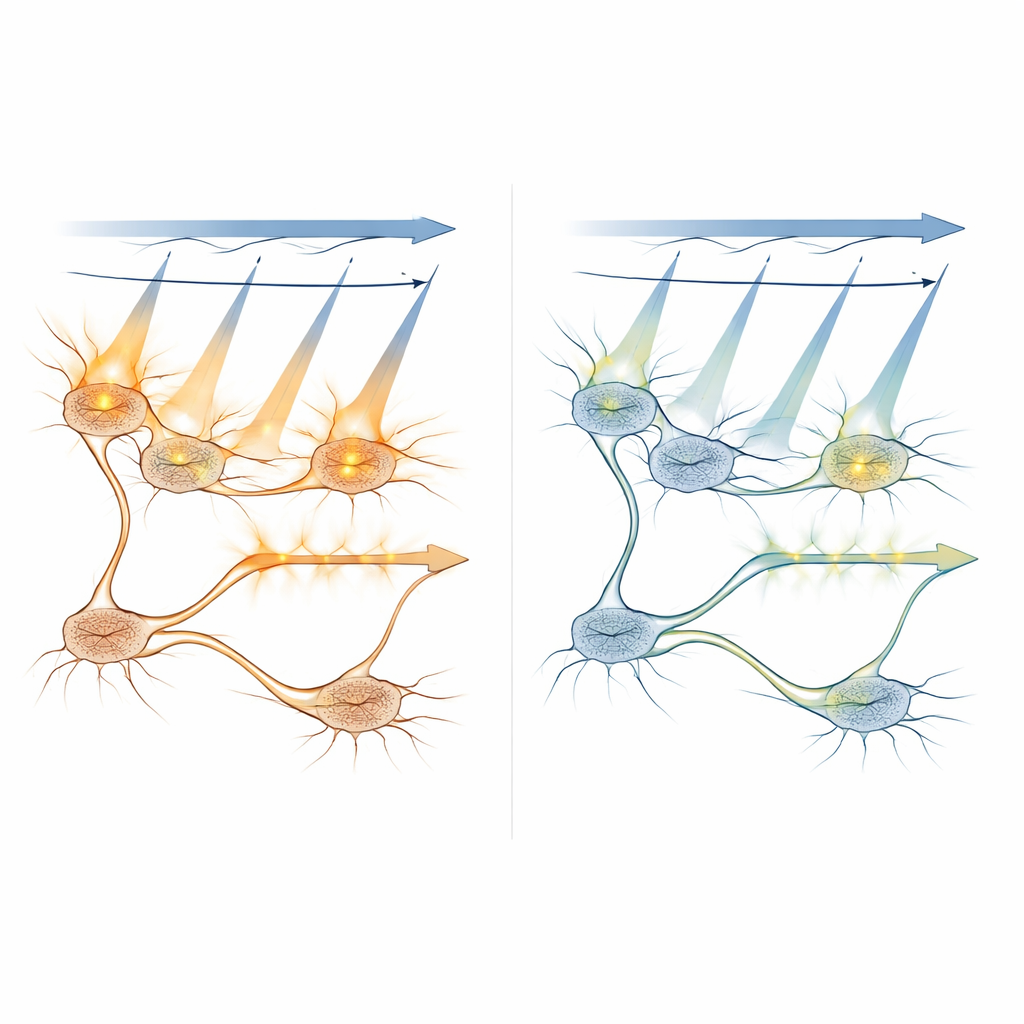
De onderzoekers combineerden computermodellen met in vivo-metingen om te begrijpen hoe scannend licht lichtgevoelige eiwitten activeert onder verschillende condities. Ze simuleerden hoe vaak individuele moleculen zouden worden ingeschakeld terwijl de laser over een neuron schreed, en hoe deze waarschijnlijkheid veranderde met laservermogen, belichtingstijd en hoe ver het focuspunt van het midden van de cel afstond. Experimenten bevestigden dat uit-focus lagen verder dan ongeveer 8–10 micrometer weinig bijdragen aan ongewenste activering, wat helpt veilige afstanden tussen afbeeldingslagen in 3D-scans te bepalen. Ze testten ook een strategie die het felle afbeeldingslicht beperkt tot het binnenste deel van het cellichaam — weg van het membraan waar de lichtgestuurde kanalen zitten — en toonden aan dat dit crosstalk verder kan verminderen, hoewel het de signaalsterkte verlaagt.
Precisie-experimenten met het brein toegankelijker maken
Buiten het aanbieden van een slimme technische oplossing heeft APPC ook praktische voordelen. Het werkt met standaard twee-fotonmicroscopen die al in veel laboratoria aanwezig zijn, heeft slechts één laser nodig en vereist geen speciaal ontworpen eiwitten of perfecte kleurenscheiding tussen instrumenten. De auteurs beargumenteren dat APPC kan worden uitgebreid naar complexere systemen, inclusief opstellingen met twee lasers, waar het complementair zou zijn aan andere strategieën die stimulatie en beeldvorming scheiden op basis van golflengte. Door empirisch het bijna crosstalk-vrije vermogensniveau voor elk type neuron en experiment af te stemmen, biedt APPC een algemene werkwijze om te bestuderen hoe specifieke cellen hersenbrede activiteit beïnvloeden zonder per ongeluk extra signalen op te roepen. In gewone bewoordingen laat het wetenschappers precies daar het licht dimmen waar het anders hun eigen instrumenten zou verblinden, waardoor het zicht op het levende brein in actie helderder wordt.
Bronvermelding: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Trefwoorden: optogenetica, twee-foton imaging, neurale circuits, zebravisbrein, actieve pixelvermogensregeling