Clear Sky Science · ru
Активное управление мощностью пикселя для безперекрестного полностью оптического исследования нейронов
Освещая мозг, не нарушая его работы
Современная нейронаука часто использует свет одновременно для наблюдения и управления активностью нервных клеток. Эта мощная идея — чтение и запись нейронных сигналов с помощью лазеров — даёт глубокое представление о том, как мозг порождает поведение и болезни. Но есть загвоздка: тот же свет, который используется для съёмки активности нейронов, может случайно активировать светочувствительные переключатели, применяемые для управления нейронами, и искажать результаты. В этой работе предлагается способ точно регулировать лазерный свет в каждой маленькой точке изображения, чтобы учёные могли одновременно наблюдать и манипулировать мозгом без взаимных помех.
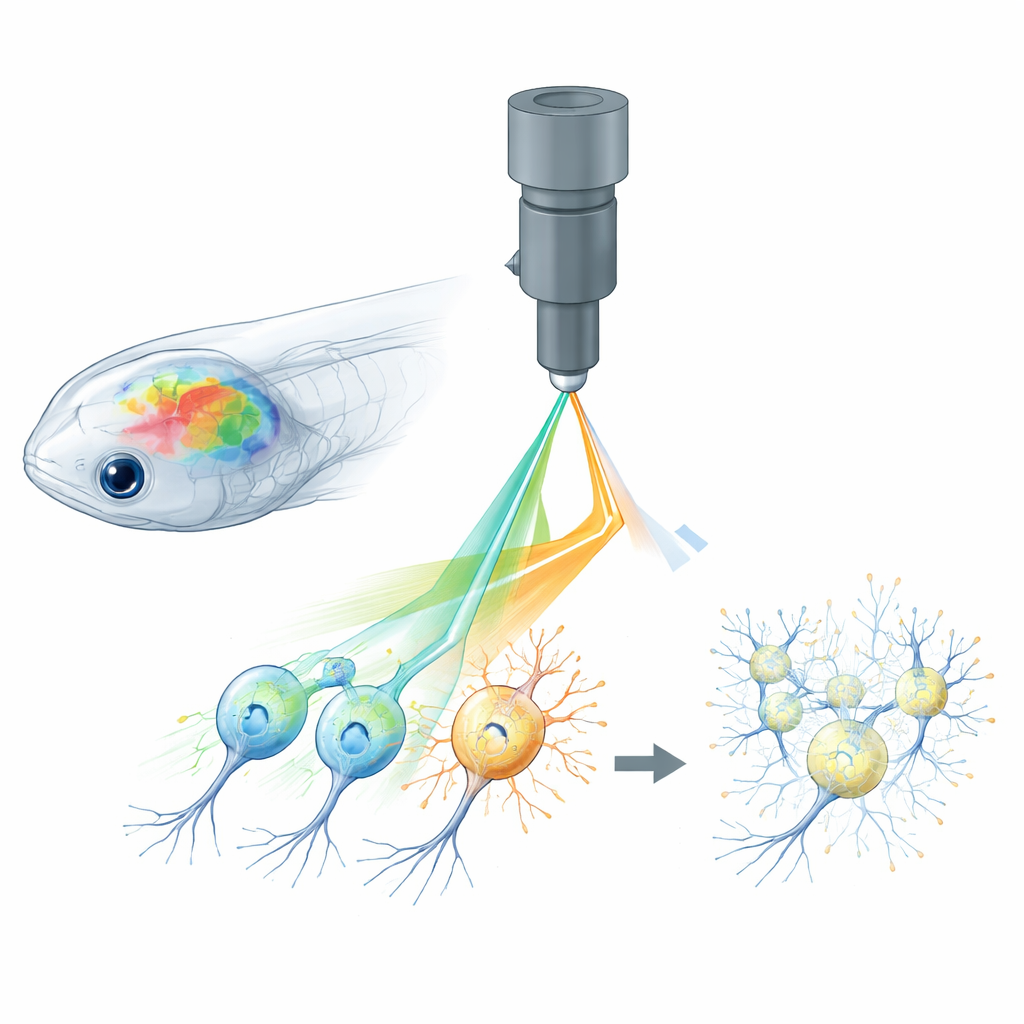
Почему наблюдать и контролировать нейроны трудно
Полностью оптические методы в нейронауке объединяют два инструмента: светящиеся датчики, которые сообщают о том, когда нейроны активны, и светочувствительные белки, позволяющие включать или выключать нейроны. В небольших животных, таких как зебрафиш, плодовые мухи и мыши, двухфотонные микроскопы могут фокусировать лазерный свет глубоко в мозге, считывая сети клеток в 3D, а голографические световые паттерны стимулируют выбранные нейроны с высокой точностью. Однако тот же лазер, который читают кальциевые сигналы от флуоресцентных датчиков, может непреднамеренно активировать светочувствительные каналы, используемые для управления. Этот «перекрестный шум» означает, что сам процесс визуализации изменяет активность мозга, размывая грань между настоящими реакциями и артефактами эксперимента.
Точное управление мощностью на уровне пикселя
Авторы решают проблему с помощью того, что они называют активным управлением мощностью пикселя, или APPC. Вместо того чтобы посылать одинаковую мощность лазера по всем точкам изображения, они используют очень быстрый модулятор света, который настраивает интенсивность лазера для каждого крошечного пикселя во время сканирования пучка. До экспериментов они определяют расположение светочувствительных каналов, изображая стандартную флуоресцентную метку, связанную с этими белками. По этой карте строится индивидуальный шаблон мощности: пиксели, перекрывающиеся со светочувствительными областями, получают значительно меньшую мощность, тогда как остальные пиксели сохраняют более высокую мощность, необходимую для чётких кальциевых сигналов. Модулятор обновляется в реальном времени, синхронизируясь с быстрыми сканирующими зеркалами микроскопа, так что мощность лазера формуется по всему мозгу с точностью до отдельного пикселя.
Тестирование метода в крошечном прозрачном мозге
Чтобы проверить, действительно ли APPC предотвращает нежелательную активацию, команда работала с личинками зебрафиш: их маленькие прозрачные мозги идеальны для съёмки всего мозга. Они использовали распространённые оптогенетические каналы (такие как ChR2 и красно-смещённый вариант ChrimsonR) вместе с зелёным кальциевым сенсором, управляемыми одним фемтосекундным лазером. Систематически снижая мощность визуализации только на нейронах, экспрессирующих светочувствительные каналы, при сохранении нормальной мощности в остальных областях, они обнаружили «золотую середину» примерно около 5 милливатт, где изображение по-прежнему давало надёжные кальциевые сигналы, но уже не вызывало дополнительной артефактной активности в этих нейронах. Важно, что они показали: такое локальное снижение мощности также предотвращает распространение эффектов перекрестного шума на последующие нейроны, сохраняя истинную проводимость и поток сигналов в цепи.
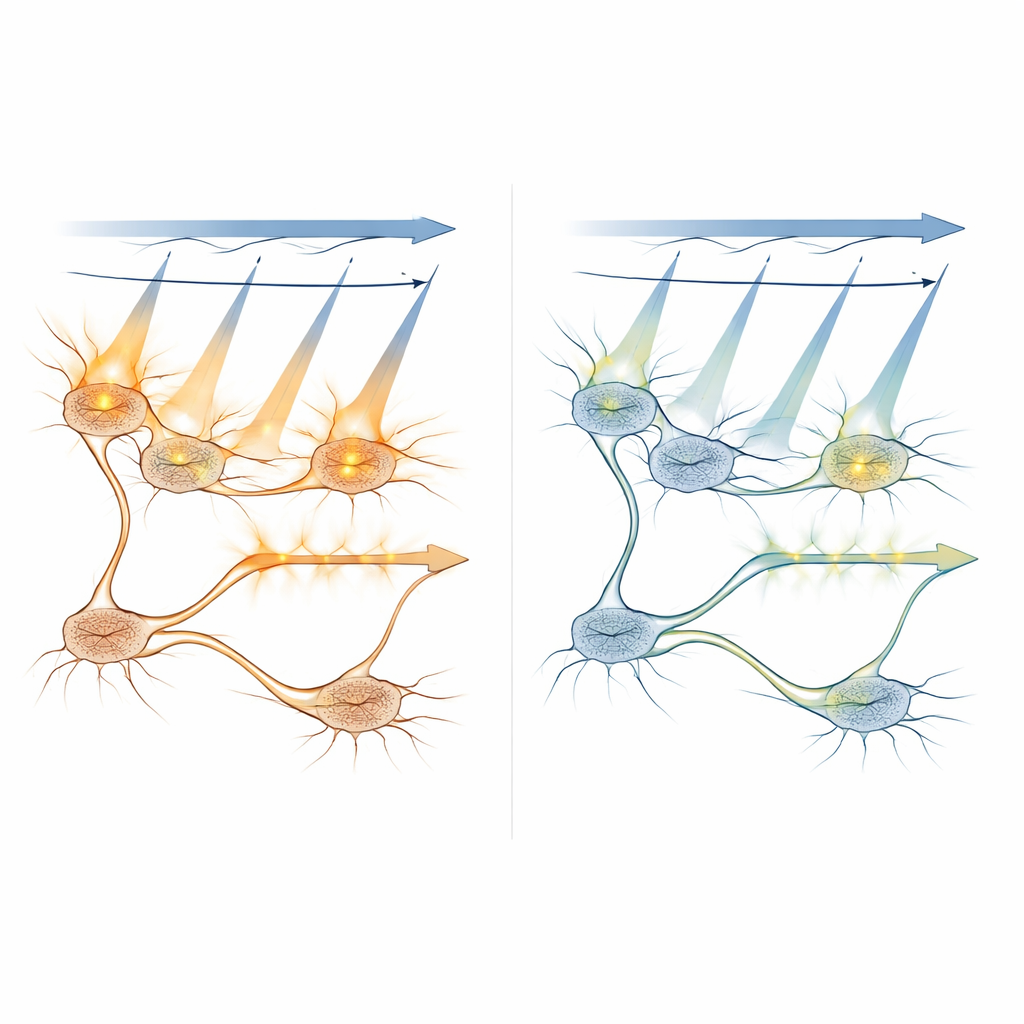
Изучение того, как свет распространяется и активирует клетки
Исследователи сочетали компьютерные модели с измерениями in vivo, чтобы понять, как сканирующий свет активирует светочувствительные белки при разных условиях. Они моделировали, как часто отдельные молекулы будут переключаться по мере того, как лазер проходит через нейрон, и как эта вероятность меняется с мощностью лазера, временем экспозиции и расстоянием фокальной точки от центра клетки. Эксперименты подтвердили, что внефокусные плоскости на расстоянии более примерно 8–10 микрометров вносят небольшой вклад в нежелательную активацию, что помогает определить безопасный интервал между слоями при 3D-сканировании. Они также опробовали стратегию, ограничивающую яркий свет визуализации внутренней частью тела клетки — вдали от мембраны, где расположены светочувствительные каналы — показав, что это дополнительно снижает перекрестный шум, хотя и уменьшает силу сигнала.
Сделать точные эксперименты с мозгом более доступными
Помимо хитрого технического решения, APPC имеет практические преимущества. Метод совместим со стандартными двухфотонными микроскопами, которые уже распространены во многих лабораториях, требует всего одного лазера и не нуждается в специальных инженерных белках или идеальном цветовом разделении инструментов. Авторы утверждают, что APPC можно расширить на более сложные системы, включая установки с двумя лазерами, где он будет дополнять стратегии разделения стимуляции и визуализации по длине волны. Подбирая эмпирически «почти свободный от перекрестного шума» уровень мощности для каждого типа нейронов и эксперимента, APPC даёт универсальный рецепт для изучения того, как отдельные клетки влияют на активность всего мозга, не вызывая случайных дополнительных сигналов. Проще говоря, метод позволяет учёным приглушать свет там, где он в противном случае заслонил бы их собственные инструменты, проясняя картину живого мозга в действии.
Цитирование: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Ключевые слова: оптогенетика, двухфотонная визуализация, нейронные цепи, мозг цыплят-рыб (зебрафиш), активное управление мощностью пикселя