Clear Sky Science · pt
Controle ativo de potência por pixel para investigação neural totalmente óptica sem interferência
Iluminando o cérebro sem perturbá‑lo
A neurociência moderna frequentemente usa luz tanto para observar quanto para controlar a atividade de células cerebrais. Essa ideia poderosa — usar lasers para ler e escrever sinais neurais — promete oferecer insights profundos sobre como cérebros geram comportamento e doenças. Mas há um problema: a própria luz usada para fazer imagens da atividade neural pode, acidentalmente, ativar os mesmos interruptores sensíveis à luz que os cientistas usam para controlar neurônios, comprometendo os resultados. Este artigo apresenta uma maneira de moldar cuidadosamente a luz do laser em cada ponto minúsculo da imagem, para que pesquisadores possam monitorar e manipular o cérebro ao mesmo tempo, sem que as duas tarefas interfiram entre si.
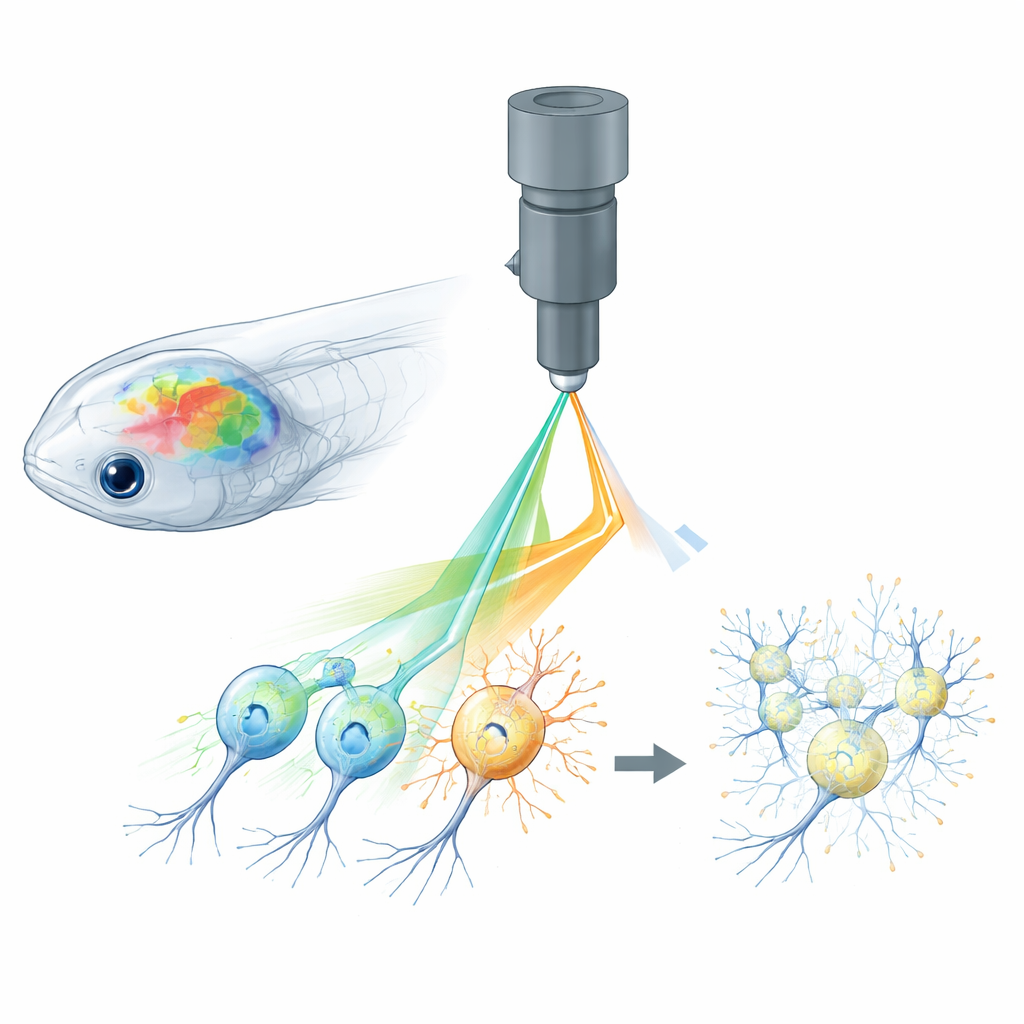
Por que é difícil observar e controlar neurônios
A neurociência totalmente óptica combina duas ferramentas: sensores fluorescentes que indicam quando neurônios estão ativos e proteínas ativadas por luz que permitem ligar ou desligar neurônios. Em animais pequenos como zebrafish, moscas-das-frutas e camundongos, microscópios de dois fótons podem focar luz de laser profundamente no cérebro para ler redes inteiras de células em 3D, enquanto padrões holográficos de luz estimulam neurônios escolhidos com precisão pontual. No entanto, o mesmo laser usado para ler sinais de cálcio dos sensores fluorescentes pode, involuntariamente, ativar os canais sensíveis à luz usados para controle. Esse “crosstalk” (interferência cruzada) significa que o processo de imagem em si altera a atividade cerebral, borrando a linha entre respostas genuínas e artefatos criados pelo experimento.
Controle de potência pontual ao nível do pixel
Os autores enfrentam esse problema com o que chamam de controle ativo de potência por pixel, ou APPC. Em vez de aplicar a mesma potência do laser a cada ponto da imagem, eles usam um modulador de luz muito rápido para ajustar a intensidade do laser para cada pixel minúsculo enquanto o feixe varre. Antes dos experimentos, eles registram onde os canais ativados por luz estão localizados ao imagem um marcador fluorescente padrão fundido a essas proteínas. A partir desse mapa, constroem um padrão de potência personalizado: pixels que se sobrepõem a regiões sensíveis à luz recebem bem menos potência, enquanto outros pixels mantêm a potência mais alta necessária para sinais claros de cálcio. O modulador atualiza em tempo real, sincronizado com os espelhos de varredura rápidos do microscópio, de modo que a potência do laser é esculpida pelo cérebro com precisão de um único pixel.
Testando o método em um cérebro transparente minúsculo
Para verificar se o APPC realmente evita ativações indesejadas, a equipe trabalhou com larvas de zebrafish, cujos cérebros pequenos e translúcidos são ideais para imagem de cérebro inteiro. Eles usaram canais optogenéticos populares (como ChR2 e uma variante deslocada para o vermelho chamada ChrimsonR) juntamente com um sensor de cálcio verde, todos acionados por um único laser de femtossegundo. Ao reduzir sistematicamente a potência de imagem apenas nos neurônios que expressavam canais sensíveis à luz, enquanto mantinham potência normal em outras regiões, encontraram um “ponto ideal” em torno de 5 miliwatts onde a imagem ainda produzia sinais de cálcio confiáveis, mas não mais induzia atividade artificial extra nesses neurônios. Importante, demonstraram que essa redução local de potência também impedia que efeitos de crosstalk se propagassem para neurônios a jusante, preservando a verdadeira conectividade e fluxo de sinais do circuito.
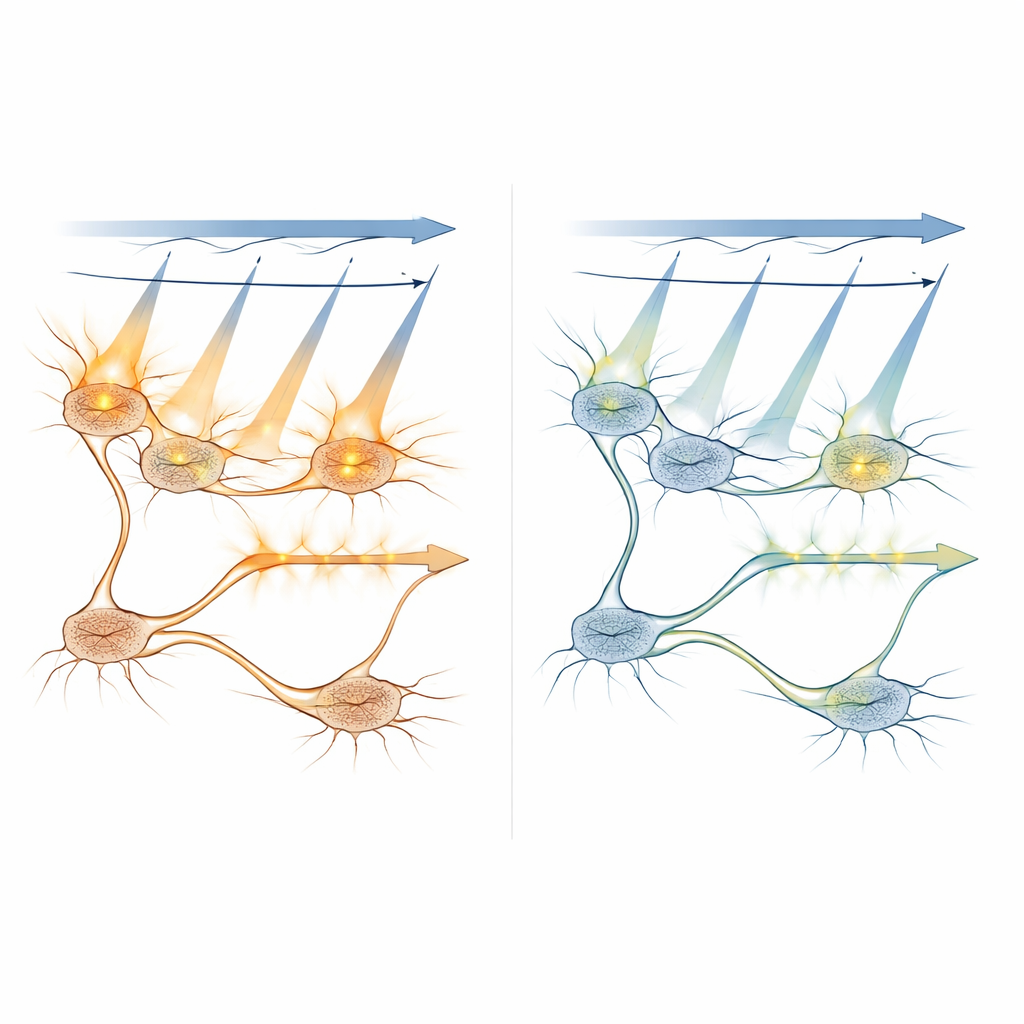
Explorando como a luz se espalha e ativa células
Os pesquisadores combinaram modelos computacionais com medidas in vivo para entender como a luz de varredura ativa proteínas sensíveis à luz sob diferentes condições. Eles simularam com que frequência moléculas individuais seriam ativadas enquanto o laser percorria um neurônio e como essa probabilidade mudava com a potência do laser, tempo de exposição e a distância do ponto focal ao centro da célula. Experimentos confirmaram que planos fora de foco a mais de cerca de 8–10 micrômetros contribuem pouco para ativações indesejadas, ajudando a definir espaçamentos seguros entre camadas de imagem em varreduras 3D. Também testaram uma estratégia que restringe a luz brilhante de imagem para a parte interna do corpo celular — longe da membrana onde os canais sensíveis à luz se situam — mostrando que isso pode reduzir ainda mais o crosstalk, embora diminua a intensidade do sinal.
Tornando experimentos cerebrais precisos mais acessíveis
Além de oferecer uma solução técnica inteligente, o APPC tem vantagens práticas. Funciona com microscópios de dois fótons padrões já comuns em muitos laboratórios, precisa de apenas um laser e não requer proteínas especialmente engenheiradas nem separação de cores perfeita entre as ferramentas. Os autores argumentam que o APPC pode ser estendido a sistemas mais complexos, incluindo configurações com dois lasers, onde complementaria outras estratégias que separam estimulação e imagem por comprimento de onda. Ao ajustar empiricamente o nível de potência “quase sem crosstalk” para cada tipo de neurônio e experimento, o APPC fornece uma receita geral para estudar como células específicas influenciam a atividade em todo o cérebro sem inadvertidamente provocar sinais extras. Em termos simples, permite aos cientistas diminuir a luz exatamente onde ela iria ofuscar seus próprios instrumentos, clareando a visão do cérebro vivo em ação.
Citação: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Palavras-chave: optogenética, microscopia de dois fótons, circuitos neurais, cérebro de zebrafish, controle ativo de potência por pixel