Clear Sky Science · de
Aktive Pixel-Leistungssteuerung für kreuzsprechungsfreie rein optische neuronale Untersuchung
Licht auf das Gehirn richten, ohne es zu stören
Die moderne Neurowissenschaft nutzt Licht, um die Aktivität von Nervenzellen zugleich zu beobachten und zu steuern. Diese mächtige Idee – Laser zu verwenden, um neuronale Signale zu lesen und zu schreiben – verspricht tiefere Einblicke, wie Gehirne Verhalten und Erkrankungen erzeugen. Doch es gibt einen Haken: Dasselbe Licht, das zur Bildgebung neuronaler Aktivität eingesetzt wird, kann unbeabsichtigt genau die lichtempfindlichen Schalter aktivieren, die Forschende zur Kontrolle von Neuronen nutzen, und so die Ergebnisse verfälschen. Dieses Paper stellt eine Methode vor, die die Laserintensität an jedem winzigen Bildpunkt so anpasst, dass man das Gehirn gleichzeitig überwachen und manipulieren kann, ohne dass sich die beiden Aufgaben gegenseitig stören.
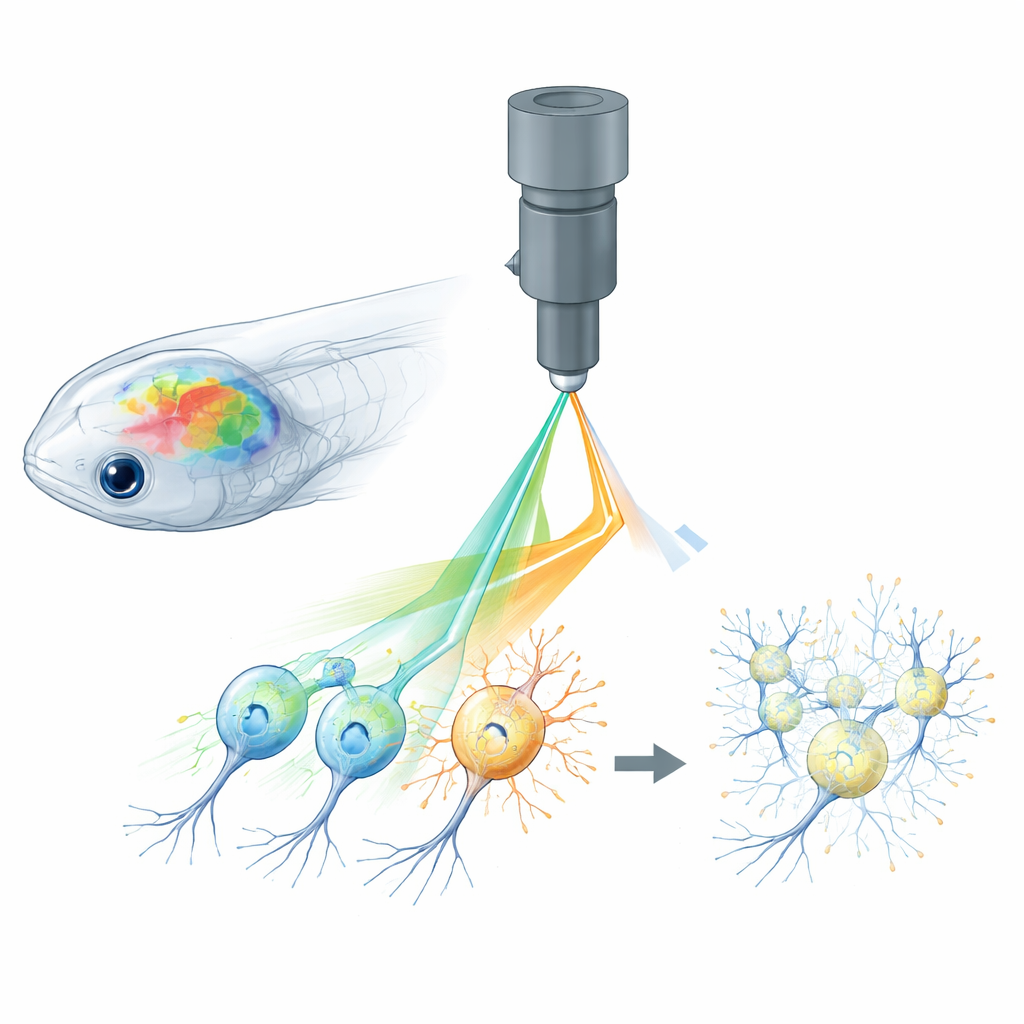
Warum Beobachten und Steuern von Neuronen schwierig ist
Die rein optische Neurowissenschaft verbindet zwei Werkzeuge: fluoreszierende Sensoren, die anzeigen, wann Neuronen aktiv sind, und lichtaktivierbare Proteine, mit denen Forschende Neuronen an- oder ausschalten können. Bei kleinen Tieren wie Zebrafischen, Fruchtfliegen und Mäusen können Zweiphotonen-Mikroskope Laserlicht tief ins Gehirn fokussieren, um ganze Netzwerke von Zellen in 3D auszulesen, während holographische Lichtmuster gezielt ausgewählte Neuronen stimulieren. Dasselbe Laserlicht, mit dem Calcium-Signale von fluoreszierenden Sensoren gelesen werden, kann jedoch unbeabsichtigt die lichtgesteuerten Kanäle für die Steuerung aktivieren. Dieses „Cross-talk“ bedeutet, dass der Bildgebungsvorgang die Gehirnaktivität selbst verändert und echte Reaktionen von durch das Experiment erzeugten Artefakten verwischt.
Präzise Leistungssteuerung auf Pixelebene
Die Autorinnen und Autoren gehen dieses Problem mit einer sogenannten aktiven Pixel-Leistungssteuerung (APPC) an. Anstatt über jeden Punkt im Bild dieselbe Laserleistung zu legen, verwenden sie einen sehr schnellen Lichtmodulator, der die Laserintensität für jedes winzige Pixel während des Scanvorgangs anpasst. Vor den Experimenten erfassen sie, wo sich die lichtaktivierbaren Kanäle befinden, indem sie ein Standard‑Fluoreszenz‑Tag, das an diese Proteine gekoppelt ist, abbilden. Aus dieser Karte erstellen sie ein maßgeschneidertes Leistungsmuster: Pixel, die mit lichtempfindlichen Regionen überlappen, erhalten deutlich weniger Leistung, während andere Pixel die höhere Leistung für klare Calcium-Signale behalten. Der Modulator aktualisiert in Echtzeit, synchronisiert mit den schnellen Scanspiegeln des Mikroskops, sodass die Laserleistung über das Gehirn mit Einzelpixel-Präzision modelliert wird.
Die Methode in einem winzigen transparenten Gehirn testen
Um zu prüfen, ob APPC unerwünschte Aktivierung tatsächlich verhindert, arbeiteten die Forschenden an Larven von Zebrafischen, deren kleine, durchsichtige Gehirne ideal für Ganzhirn‑Bildgebung sind. Sie verwendeten gängige optogenetische Kanäle (wie ChR2 und eine rotverschobene Variante namens ChrimsonR) zusammen mit einem grünen Calcium‑Sensor, betrieben alle mit einem einzigen Femtosekundenlaser. Indem sie die Bildgebungsleistung systematisch nur bei Neuronen reduzierten, die lichtempfindliche Kanäle exprimierten, und ansonsten normale Leistung beibehielten, fanden sie einen „Sweet Spot“ bei etwa 5 Milliwatt, bei dem die Bildgebung weiterhin zuverlässige Calcium-Signale lieferte, aber keine zusätzlichen, künstlichen Aktivitäten in diesen Neuronen auslöste. Wichtig ist, dass sie zeigten, dass diese lokale Leistungsreduktion auch verhinderte, dass Cross‑Talk‑Effekte in nachgeschaltete Neuronen auslaufen, wodurch die echte Verschaltung und Signalweiterleitung des Kreises erhalten blieb.
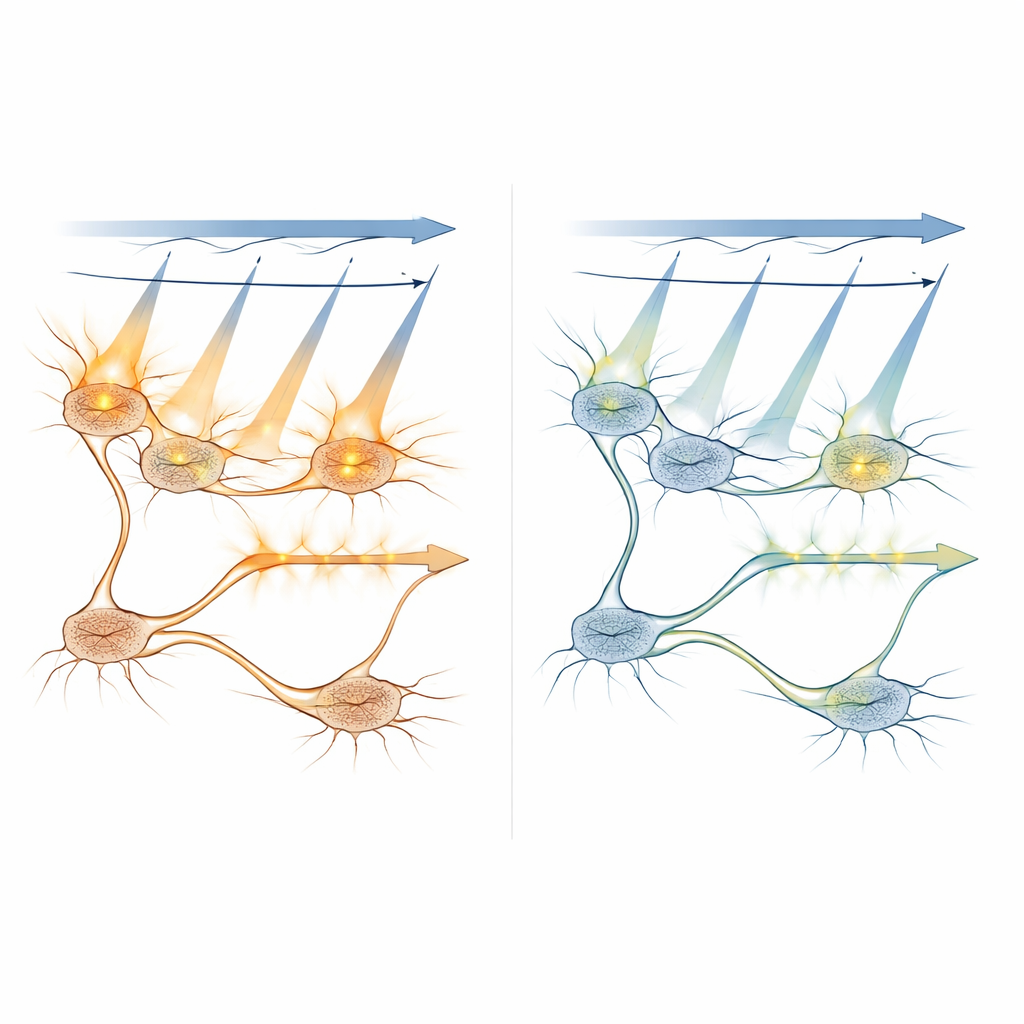
Untersuchung, wie Licht sich ausbreitet und Zellen aktiviert
Die Forschenden kombinierten Computermodelle mit In‑vivo‑Messungen, um zu verstehen, wie sich scanndes Licht unter verschiedenen Bedingungen lichtempfindliche Proteine aktiviert. Sie simulierten, wie oft einzelne Moleküle eingeschaltet würden, während der Laser über ein Neuron schwenkte, und wie diese Wahrscheinlichkeit mit Laserleistung, Belichtungszeit und dem Abstand des Brennpunkts vom Zellzentrum variiert. Experimente bestätigten, dass außerhalb des Fokus liegende Ebenen, die mehr als etwa 8–10 Mikrometer entfernt sind, nur wenig zur unerwünschten Aktivierung beitragen, was hilft, sichere Abstände zwischen Bildgebungsebenen bei 3D‑Scans zu definieren. Sie testeten auch eine Strategie, die das helle Bildlicht auf den inneren Teil des Zellkörpers beschränkt – weg von der Membran, wo die lichtgesteuerten Kanäle sitzen – und zeigten, dass dies das Cross‑Talk weiter reduzieren kann, obwohl dabei das Signal stärker abgeschwächt wird.
Präzise Gehirnexperimente zugänglicher machen
Über die clevere technische Lösung hinaus bietet APPC praktische Vorteile. Es funktioniert mit standardmäßigen Zweiphotonen‑Mikroskopen, die in vielen Labors bereits verbreitet sind, benötigt nur einen Laser und erfordert weder speziell entwickelte Proteine noch perfekte Farbtrennung zwischen den Werkzeugen. Die Autorinnen und Autoren argumentieren, dass sich APPC auf komplexere Systeme erweitern lässt, einschließlich Aufbauten mit zwei Lasern, wo es andere Strategien ergänzen würde, die Stimulation und Bildgebung durch Wellenlängen zu trennen. Indem man für jeden Neuronentyp und jedes Experiment empirisch das „nahezu kreuzsprechungsfreie“ Leistungsniveau anpasst, bietet APPC ein allgemeines Rezept dafür, wie man untersuchen kann, wie bestimmte Zellen die Gehirnaktivität beeinflussen, ohne versehentlich zusätzliche Signale zu erzeugen. Alltagssprachlich erlaubt es Forschenden, das Licht genau dort zu dimmen, wo es sonst ihre eigenen Instrumente blenden würde, und so den Blick auf das lebende Gehirn in Aktion zu klären.
Zitation: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Schlüsselwörter: Optogenetik, Zweiphotonen-Bildgebung, neuronale Schaltkreise, Zebrafischgehirn, aktive Pixel-Leistungssteuerung