Clear Sky Science · it
Controllo della potenza a pixel attivo per un’interrogazione neurale totalmente ottica senza interferenze
Illuminare il cervello senza disturbarlo
La neuroscienza moderna spesso si basa sulla luce sia per osservare sia per controllare l’attività delle cellule cerebrali. Questa potente idea — usare laser per leggere e scrivere segnali neurali — promette approfondimenti su come i cervelli generano comportamenti e malattie. Ma c’è un problema: la stessa luce impiegata per registrare l’attività neurale può involontariamente attivare gli stessi interruttori sensibili alla luce che gli scienziati usano per controllare i neuroni, confondendo i risultati. Questo articolo introduce un modo per modellare finemente la luce laser in ogni punto dell’immagine in modo che i ricercatori possano monitorare e manipolare il cervello contemporaneamente, senza che i due compiti si interferiscano a vicenda.
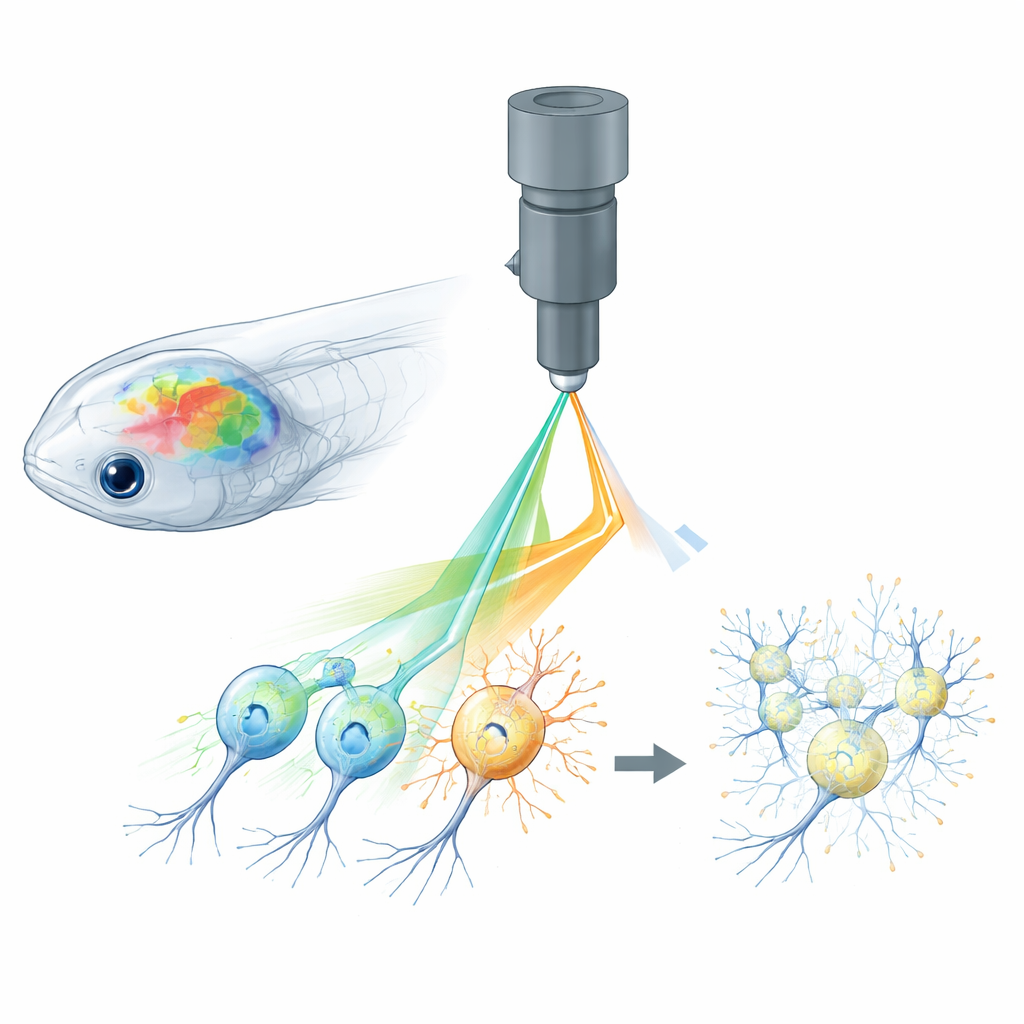
Perché osservare e controllare i neuroni è difficile
La neuroscienza totalmente ottica combina due strumenti: sensori fluorescenti che segnalano quando i neuroni sono attivi e proteine attivabili dalla luce che permettono agli scienziati di accendere o spegnere i neuroni. In animali piccoli come il pesce zebra, la mosca della frutta e il topo, i microscopi a due fotoni possono concentrare la luce laser in profondità nel cervello per leggere intere reti cellulari in 3D, mentre pattern olografici di luce stimolano neuroni scelti con precisione puntiforme. Tuttavia, lo stesso laser usato per leggere i segnali di calcio dai sensori fluorescenti può attivare involontariamente i canali sensibili alla luce usati per il controllo. Questo “cross-talk” significa che il processo di imaging altera di per sé l’attività cerebrale, sfocando il confine tra risposte genuine e artefatti creati dall’esperimento.
Controllo puntuale della potenza a livello di pixel
Gli autori affrontano questo problema con ciò che chiamano controllo attivo della potenza a pixel, o APPC. Invece di irradiare la stessa potenza laser su ogni punto dell’immagine, usano un modulatore di luce molto veloce per regolare l’intensità del laser per ciascun minuscolo pixel mentre il fascio scansiona. Prima degli esperimenti, registrano dove si trovano i canali attivati dalla luce mediante l’imaging di un marcatore fluorescente standard fuso a quelle proteine. Da questa mappa costruiscono un pattern di potenza personalizzato: i pixel che si sovrappongono a regioni sensibili alla luce ricevono molta meno potenza, mentre gli altri pixel mantengono la potenza elevata necessaria per segnali di calcio nitidi. Il modulatore si aggiorna in tempo reale, sincronizzato con gli specchi di scansione rapida del microscopio, così che la potenza del laser venga scolpita nel cervello con precisione a livello di singolo pixel.
Testare il metodo in un piccolo cervello trasparente
Per verificare se l’APPC previene davvero attivazioni indesiderate, il team ha lavorato su larve di pesce zebra, il cui cervello piccolo e trasparente è ideale per l’imaging dell’intero cervello. Hanno usato canali optogenetici popolari (come ChR2 e una variante spostata verso il rosso chiamata ChrimsonR) insieme a un sensore di calcio verde, tutti eccitati da un singolo laser a femtosecondi. Abbassando sistematicamente la potenza di imaging solo sui neuroni che esprimevano canali sensibili alla luce, mantenendo la potenza normale altrove, hanno individuato un “punto ottimale” intorno a 5 milliwatt in cui l’imaging continuava a produrre segnali di calcio affidabili ma non attivava più attività artificiale in quei neuroni. È importante che abbiano dimostrato che questa riduzione locale di potenza impedisce anche che gli effetti di cross-talk si propaghino ai neuroni a valle, preservando il reale cablaggio e il flusso di segnali del circuito.
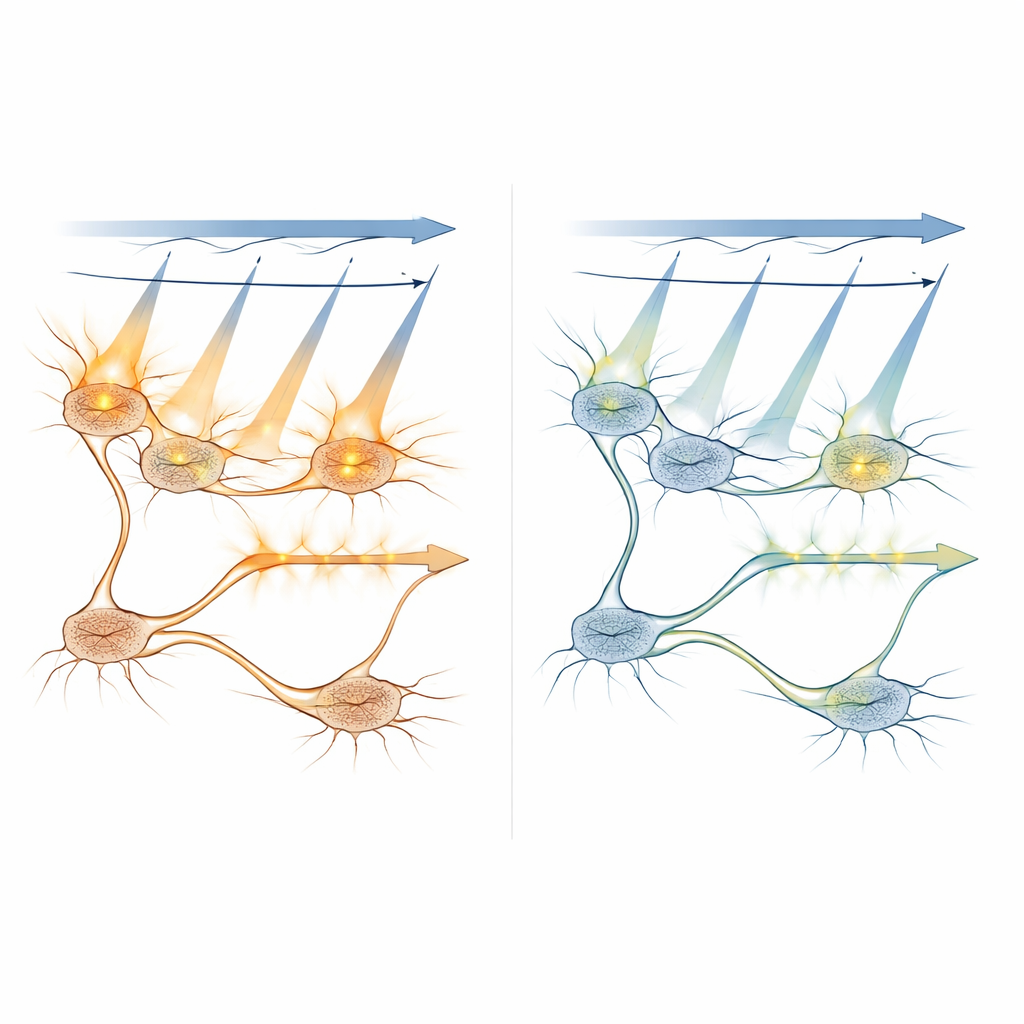
Esplorare come la luce si diffonde e attiva le cellule
I ricercatori hanno combinato modelli al computer con misurazioni in vivo per comprendere come la luce di scansione attiva le proteine sensibili alla luce in condizioni diverse. Hanno simulato con quale frequenza singole molecole verrebbero attivate mentre il laser attraversava un neurone e come questa probabilità cambiasse con la potenza del laser, il tempo di esposizione e la distanza del punto focale dal centro della cellula. Gli esperimenti hanno confermato che i piani fuori fuoco a più di circa 8–10 micrometri di distanza contribuiscono poco all’attivazione indesiderata, aiutando a definire spazi di sicurezza tra i livelli di imaging nelle scansioni 3D. Hanno anche testato una strategia che limita la luce intensa di imaging alla parte interna del soma — lontano dalla membrana dove si trovano i canali sensibili alla luce — dimostrando che questo può ridurre ulteriormente il cross-talk, sebbene riduca l’intensità del segnale.
Rendere gli esperimenti cerebrali di precisione più accessibili
Oltre a offrire una soluzione tecnica intelligente, l’APPC ha vantaggi pratici. Funziona con microscopi a due fotoni standard già presenti in molti laboratori, richiede un solo laser e non necessita di proteine ingegnerizzate speciali né di una separazione cromatica perfetta tra gli strumenti. Gli autori sostengono che l’APPC può essere estesa a sistemi più complessi, inclusi allestimenti con due laser, dove completerebbe altre strategie che separano stimolazione e imaging per lunghezza d’onda. Regolando empiricamente il livello di potenza “quasi privo di cross-talk” per ogni tipo di neurone e per ciascun esperimento, l’APPC fornisce una ricetta generale per studiare come cellule specifiche influenzano l’attività cerebrale globale senza innescare segnali aggiuntivi involontari. In termini pratici, permette agli scienziati di abbassare la luce esattamente dove altrimenti accecherebbe i loro stessi strumenti, chiarendo la visione del cervello vivente in azione.
Citazione: Yan, G., Tian, G., Fu, Y. et al. Active pixel power control for crosstalk-free all-optical neural interrogation. Nat Commun 17, 3195 (2026). https://doi.org/10.1038/s41467-026-69419-8
Parole chiave: optogenetica, microscopia a due fotoni, circuiti neuronali, cervello di zebra fish, controllo attivo della potenza a pixel