Clear Sky Science · zh
MYCN通过干扰PKA信号通路抑制神经母细胞瘤细胞中TrkC介导的分化
这项儿童癌症研究为何重要
神经母细胞瘤是一种儿童癌症,临床表现可大相径庭:有些肿瘤会悄然成熟并缩小,而有些则侵袭性强并耐药。本文提出了一个看似简单但临床后果重大的问题:为什么相同的信号会促使某些神经母细胞成熟为无害的类神经细胞,而驱动另一些细胞增殖为癌?通过揭示一个名为MYCN的强致癌基因如何阻断天然的成熟信号,作者们指出了一种可能将高危肿瘤诱导到更安全、更易治疗状态的新策略。
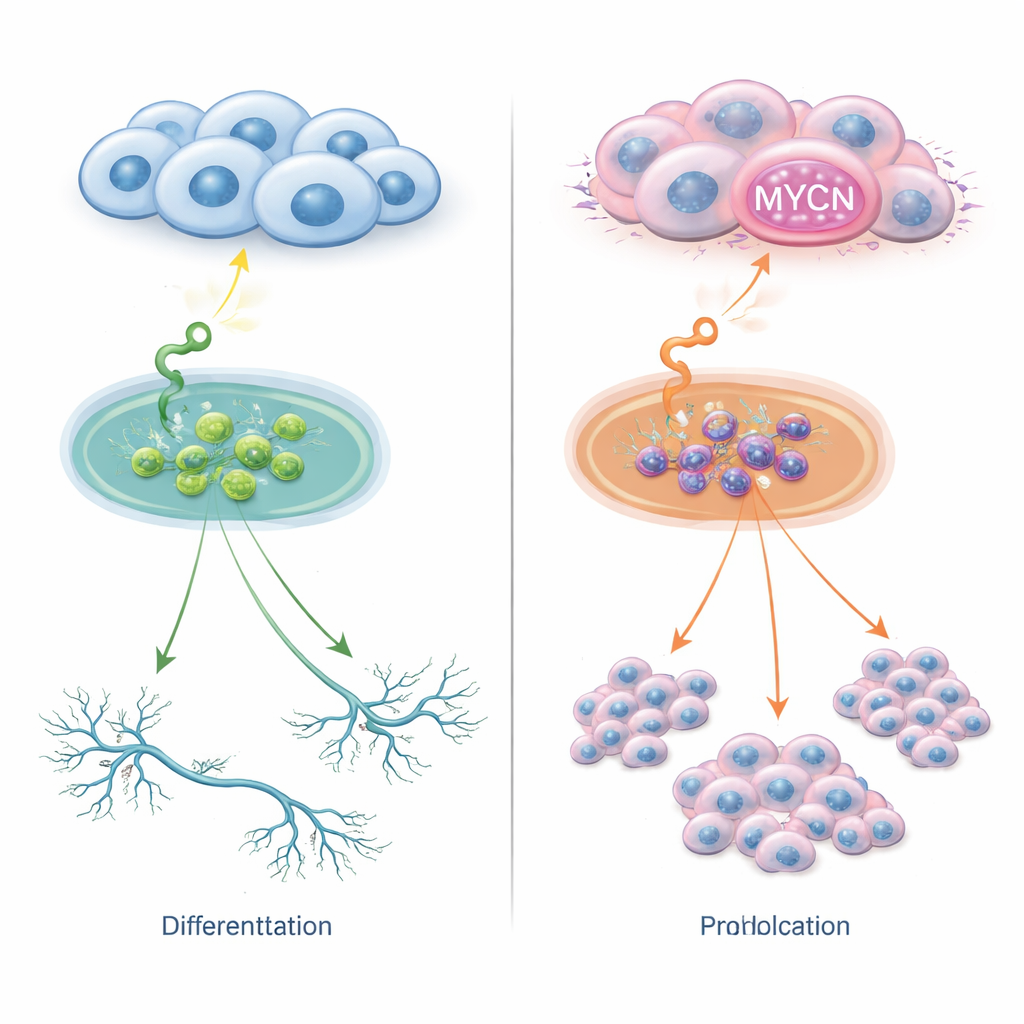
同一信号的两条出路
神经母细胞瘤细胞在表面表达受体以感知周围的生长因子。其中一种受体TrkC能识别名为NT‑3的分子。在正常情况下,这一配对会鼓励幼稚的神经细胞向更成熟的形态发育。研究人员给若干神经母细胞瘤细胞系导入TrkC并用NT‑3刺激。在没有额外MYCN拷贝的细胞中,NT‑3促使细胞伸长出类似神经的分支并呈现更成熟的外观,细胞数量变化很小。相比之下,在MYCN过量——无论是过表达还是基因扩增——的细胞中,同样的NT‑3信号不再触发分化,反而促进了快速的细胞分裂。因此,单一外界信号可导致分化或侵袭性增长,依赖于细胞内MYCN的含量。
追踪细胞内的信号足迹
为理解这种行为分歧的来源,团队用一种称为磷酸化蛋白组学的技术随时间绘制细胞内化学“开/关”开关。他们比较了不同细胞系中经NT‑3刺激后成千上万种修饰蛋白的变化。未发生MYCN扩增的细胞表现出强烈且独特的激活模式,而富含MYCN的细胞反应较为迟钝。聚焦于最活跃的信号酶时,分化细胞中反复出现的一个关键角色浮现:蛋白激酶A(PKA)通路及其伴侣CREB——一种在细胞核内开启成熟相关基因的调控因子。通路分析进一步证实,当PKA/CREB活性上升时,与神经发育和结构重塑相关的过程(如轴突引导和细胞骨架变化)被特异性富集。
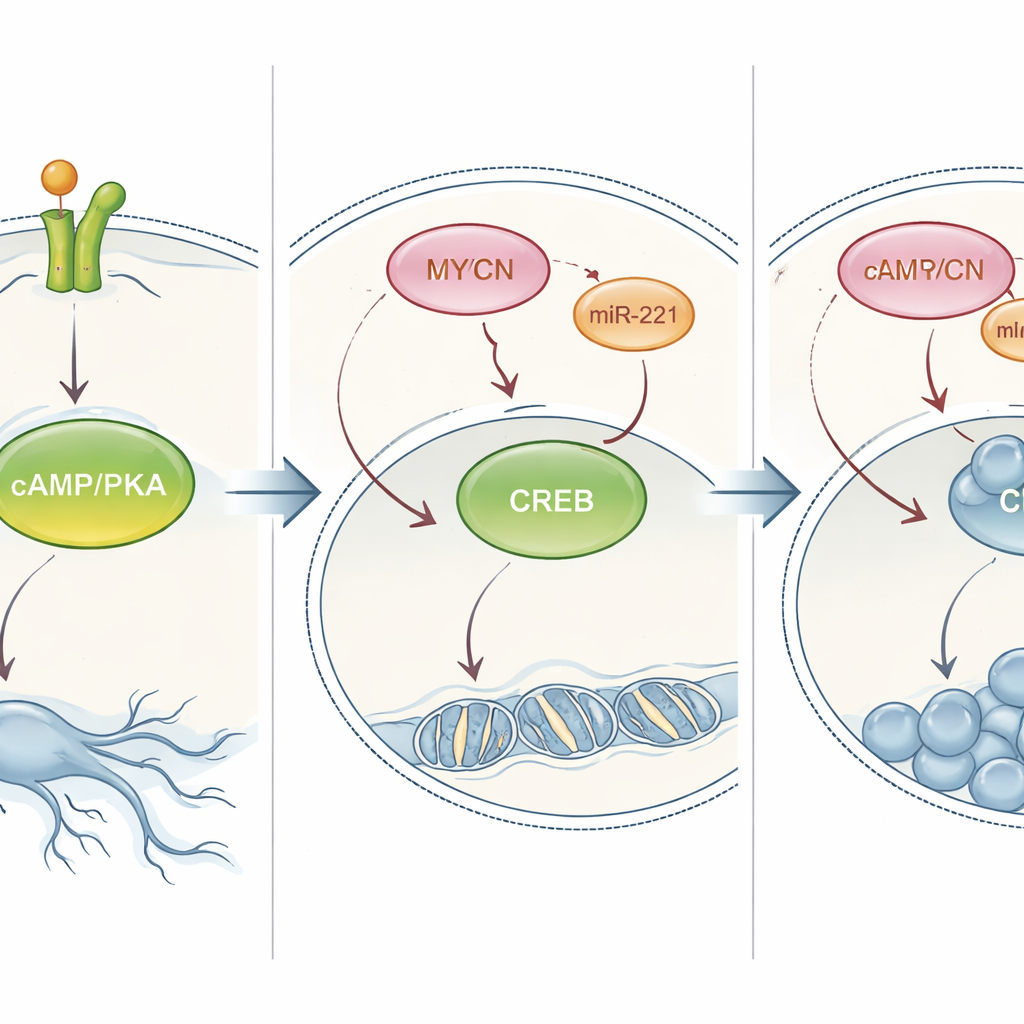
翻转PKA开关以改变肿瘤行为
研究人员接着检验了PKA通路是否真的是决定细胞走向分化或增殖的控制开关。在通常对NT‑3产生分化反应的细胞中,化学抑制PKA会减少其类神经的突起并增加细胞数量。在通常仅增殖的MYCN扩增细胞中,人工激活PKA——不论是用模拟天然信号分子的药物,还是强制细胞表达始终活跃的PKA或CREB——都能逆转其行为:细胞分裂变慢并长出类似神经元的长突起。这一效应不仅在细胞培养中出现,在斑马鱼模型中也成立:激活PKA会导致移植的人类神经母细胞瘤肿瘤缩小。综上实验表明,PKA/CREB信号是一个中心杠杆,可将高危神经母细胞瘤细胞重新导向更成熟、危害更小的状态。
MYCN与一种微小RNA如何堵塞分化回路
随后研究考察了MYCN如何关闭这一有益通路。当在扩增的细胞中降低MYCN水平时,PKA和CREB蛋白增加,NT‑3再次推动分化而非增殖。对患者肿瘤数据的分析显示,编码PKA组分的基因在MYCN扩增肿瘤中的表达低于其他病例,提示MYCN在高危病人中广泛抑制该通路。作者还发现了一种小调控RNA——miR‑221的作用,它与MYCN和不良预后高度相关。高水平的miR‑221在肿瘤和细胞系中都与MYCN表达相关联。在MYCN扩增的细胞中阻断miR‑221后,CREB水平上升,NT‑3再次能够驱动神经元样分化。这表明MYCN既通过下调关键基因,又通过提高miR‑221水平来进一步降低CREB,从而双重压制PKA/CREB回路。
这对未来治疗意味着什么
总体而言,该研究勾勒出一幅清晰图景:在低危神经母细胞瘤中,NT‑3通过TrkC并借助活跃的PKA/CREB通路,帮助未成熟的肿瘤细胞成熟为良性的类神经细胞。在具有额外MYCN的高危肿瘤中,这一路径被阻断,同一信号被改道为促进失控生长,部分由miR‑221协助。通过恢复PKA/CREB活性——使用能增强该通路的药物或抑制MYCN驱动的阻断因子——临床上有望将侵袭性神经母细胞瘤转变为更分化、更易治疗的肿瘤。这一策略契合儿童癌症治疗的更广泛目标:不仅消灭癌细胞,还将它们引回正常发育轨道。
引用: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
关键词: 神经母细胞瘤, MYCN, TrkC, PKA CREB通路, 肿瘤分化