Clear Sky Science · pl
MYCN hamuje różnicowanie zależne od TrkC w komórkach neuroblastomy poprzez zakłócenie szlaku sygnalizacyjnego PKA
Dlaczego to badanie nad nowotworem wieku dziecięcego ma znaczenie
Neuroblastoma to nowotwór wieku dziecięcego, który może zachowywać się diametralnie różnie: niektóre guzy dojrzewają i zmniejszają się, podczas gdy inne szybko rozsiewają się i opierają leczeniu. W badaniu zadano pozornie proste, ale o dużych konsekwencjach klinicznych pytanie: dlaczego te same sygnały skłaniają jedne komórki neuroblastomy do „dorastania” i przybrania łagodnego, nerwopodobnego fenotypu, a inne do intensywnego mnożenia jako rakowe? Odkrywając, jak potężny gen onkogenny MYCN blokuje naturalny sygnał dojrzewania, autorzy ujawniają potencjalny nowy sposób skłonienia guzów wysokiego ryzyka do bardziej bezpiecznego, podatnego na leczenie stanu.
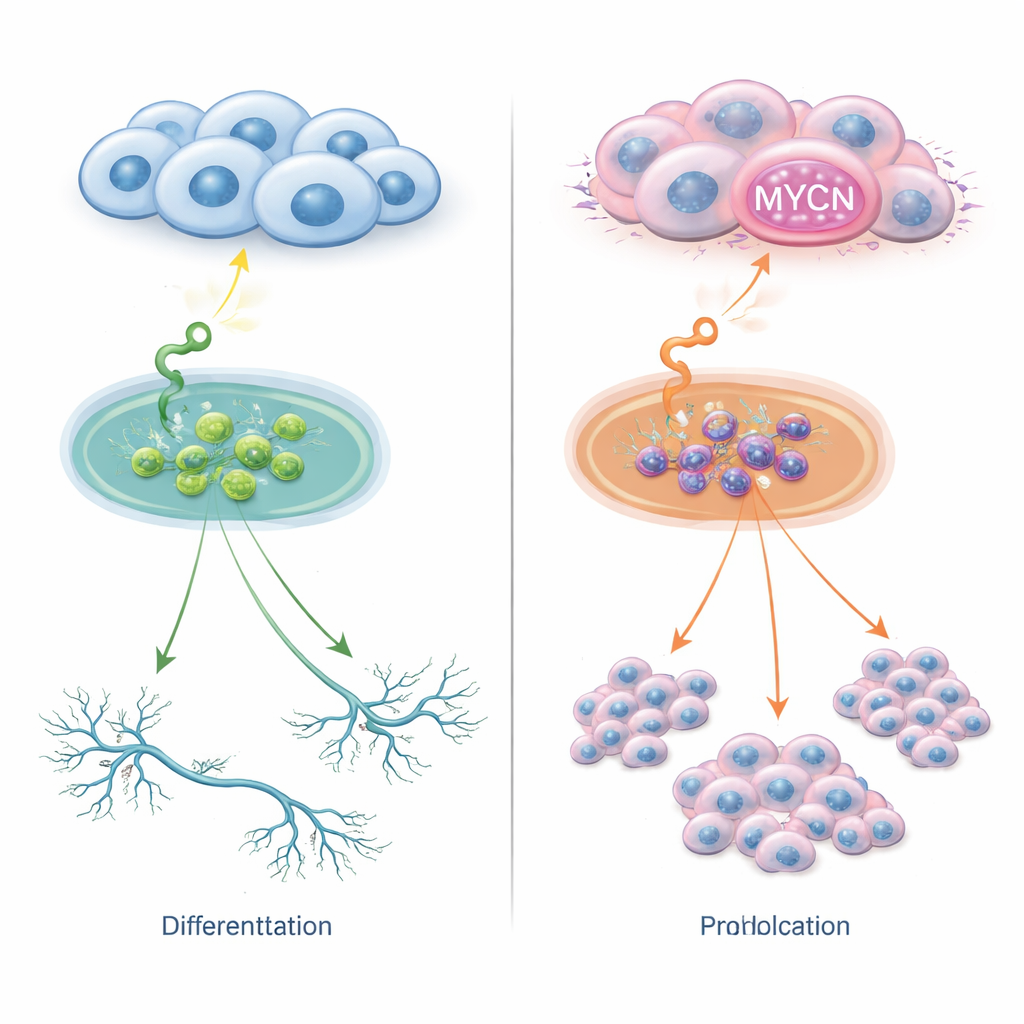
Dwie ścieżki dla tego samego sygnału
Komórki neuroblastomy mają na powierzchni receptory wykrywające czynniki wzrostowe w otoczeniu. Jeden z tych receptorów, zwany TrkC, rozpoznaje cząsteczkę o nazwie NT‑3. W normalnych warunkach to połączenie może zachęcać młode komórki nerwowe do różnicowania się w bardziej dojrzałe formy. Badacze wprowadzili TrkC do kilku linii komórkowych neuroblastomy, a następnie pobudzili je NT‑3. W komórkach bez dodatkowych kopii genu MYCN NT‑3 skłoniło je do wydłużenia długich, nerwopodobnych wypustek i przybrania bardziej dojrzałego wyglądu, przy niewielkiej zmianie liczby komórek. W wyraźnym kontraście, w komórkach z nadmiarem MYCN — przez nadekspresję lub amplifikację genu — ten sam sygnał NT‑3 nie wywoływał już dojrzewania, lecz napędzał szybki podział komórek. Tak więc jeden zewnętrzny bodziec może prowadzić do różnicowania albo agresywnego wzrostu, w zależności od poziomu MYCN w komórkach.
Śledzenie śladów sygnalizacji wewnątrz komórki
Aby zrozumieć, jak powstaje to rozgałęzienie zachowań, zespół odwzorował chemiczne „włączniki/wyłączniki” wewnątrz komórek w czasie, używając techniki zwanej fosfoproteomiką. Porównali tysiące zmodyfikowanych białek po stymulacji NT‑3 w różnych liniach komórkowych. Komórki bez amplifikacji MYCN wykazały silny i charakterystyczny wzór aktywacji, podczas gdy komórki bogate w MYCN miały stłumioną odpowiedź. Gdy autorzy skupili się na najbardziej aktywnych enzymach sygnalizacyjnych, w wyróżniających się komórkach różnicujących się pojawił się powtarzający się gracz: szlak kinazy białkowej A (PKA) i jej partner CREB, regulator w jądrze komórkowym, który włącza geny potrzebne do dojrzewania. Analiza szlaków potwierdziła, że procesy związane z rozwojem nerwów i przebudową strukturalną — takie jak prowadzenie aksonów i zmiany cytoszkieletu — były wzbogacone właśnie wtedy, gdy wzrastała aktywność PKA/CREB.
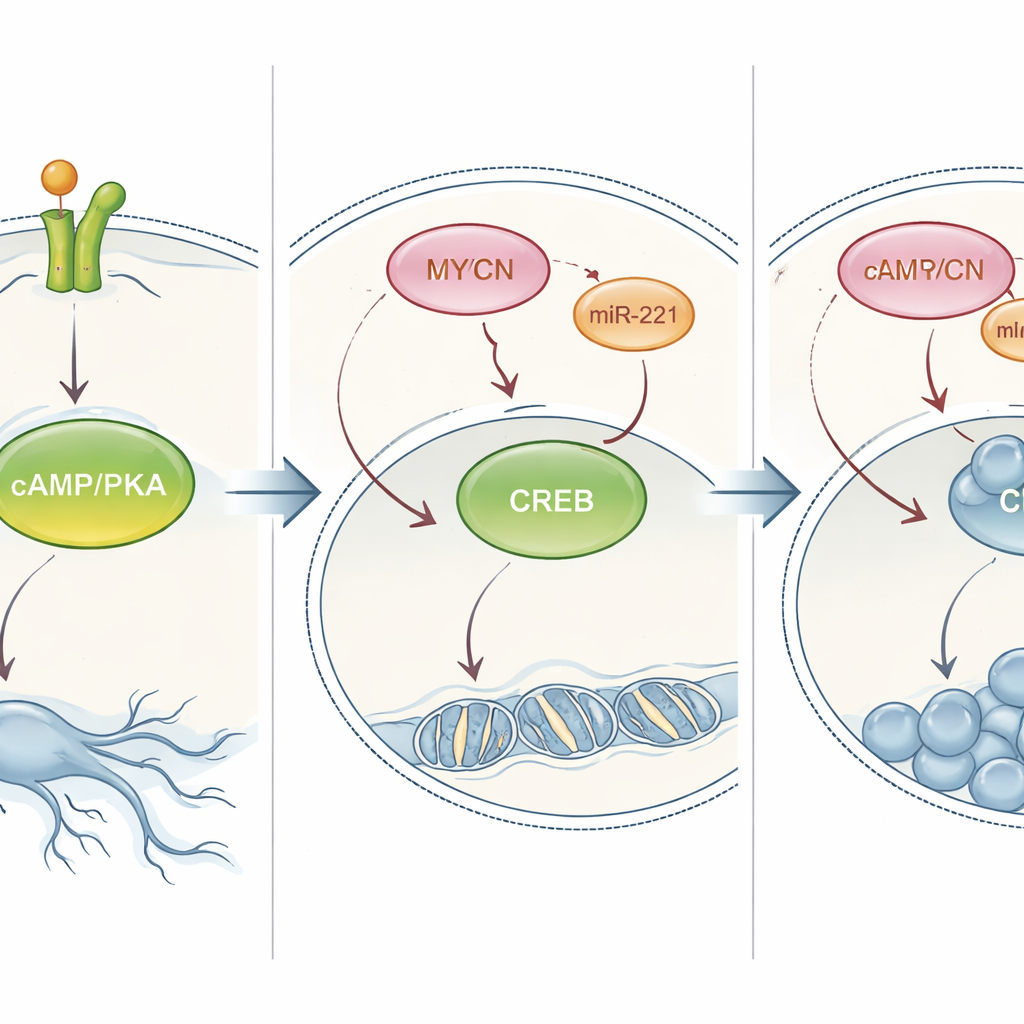
Przełączenie PKA, by zmienić zachowanie guza
Następnie badacze sprawdzili, czy ten szlak PKA rzeczywiście kontroluje decyzję komórki między dojrzewaniem a proliferacją. W komórkach, które normalnie różnicowały się po ekspozycji na NT‑3, chemiczne zablokowanie PKA zmniejszało ich nerwopodobne wypustki i zwiększało liczbę komórek. W komórkach z amplifikowanym MYCN, które zwykle tylko proliferują, sztuczne pobudzenie PKA — albo lekiem naśladującym naturalny przekaźnik, albo przez wymuszenie ekspresji zawsze aktywnych form PKA lub CREB — odwracało ich zachowanie: komórki zwalniały podział i rozwijały długie wypustki przypominające neurony. Efekt ten występował nie tylko w hodowlach komórkowych, lecz także w modelu z zebrafiszem, gdzie aktywacja PKA spowodowała skurczenie się wszczepionych ludzkich guzów neuroblastomy. Razem te eksperymenty pokazują, że sygnalizacja PKA/CREB jest centralną dźwignią, która może przekierować komórki neuroblastomy wysokiego ryzyka ku bardziej dojrzałemu, mniej niebezpiecznemu stanowi.
Jak MYCN i mikroRNA blokują obwód różnicowania
Badanie przeanalizowało następnie, jak MYCN wyłącza ten korzystny szlak. Gdy poziomy MYCN zostały zmniejszone w komórkach z amplifikacją, białka PKA i CREB wzrosły, a NT‑3 ponownie promowało różnicowanie zamiast wzrostu. Analizy danych z guzów pacjentów wykazały, że geny kodujące składniki PKA są wyrażane na niższym poziomie w nowotworach z amplifikacją MYCN niż w innych przypadkach, co sugeruje, że MYCN szeroko tłumi ten szlak u dzieci z chorobą wysokiego ryzyka. Autorzy odkryli też rolę małego regulatorowego RNA, miR‑221, które jest silnie związane z MYCN i złym rokowaniem. Wysokie poziomy miR‑221 korelowały z ekspresją MYCN zarówno w guzach, jak i w liniach komórkowych. Gdy zablokowano miR‑221 w komórkach z amplifikacją MYCN, poziomy CREB wzrosły i NT‑3 znów mogło napędzać dojrzewanie neuronalne. Wskazuje to, że MYCN tłumi obwód PKA/CREB zarówno przez obniżanie ekspresji kluczowych genów, jak i przez podnoszenie miR‑221, które dodatkowo obniża CREB.
Co to oznacza dla przyszłych terapii
Podsumowując, praca układa czytelny obraz: w niskozagrożeniowej neuroblastomie NT‑3 działające przez TrkC i aktywny szlak PKA/CREB pomaga niedojrzałym komórkom guza „dorosnąć” do łagodnych, nerwopodobnych komórek. W nowotworach wysokiego ryzyka z nadmiarem MYCN ta droga dojrzewania jest zablokowana, a ten sam sygnał zostaje przekierowany, by napędzać niekontrolowany wzrost, wspierany częściowo przez mikroRNA miR‑221. Przywrócenie aktywności PKA/CREB — za pomocą leków wzmacniających ten szlak lub przez stłumienie blokad napędzanych przez MYCN — może w przyszłości pozwolić przekształcić agresywne neuroblastomy w bardziej zróżnicowane, podatne na leczenie guzy. Strategia ta wpisuje się w szerszy cel terapii nowotworów wieku dziecięcego: nie tylko zabijać komórki nowotworowe, lecz także nakłaniać je do powrotu na normalną ścieżkę rozwojową.
Cytowanie: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Słowa kluczowe: neuroblastoma, MYCN, TrkC, szlak PKA CREB, różnicowanie guza