Clear Sky Science · tr
MYCN, PKA sinyal yolunu bozarak nöroblastom hücrelerinde TrkC aracılı farklılaşmayı engelliyor
Bu çocukluk çağı kanseri çalışması neden önemli
Nöroblastom, bazı tümörlerin sessizce olgunlaşıp küçülürken bazılarının agresifçe yayılıp tedaviye direnç göstermesi gibi çok farklı davranışlar sergileyebilen bir çocukluk çağı kanseridir. Bu çalışma, klinik sonuçları büyük olan, aldatıcı derecede basit bir soruyu soruyor: neden bazı sinyaller bazı nöroblastom hücrelerini zararsız sinir benzeri hücrelere olgunlaştırırken, diğerlerini kanser olarak çoğalmaya itiyor? Güçlü bir onkogen olan MYCN’nin doğal bir olgunlaştırma sinyalini nasıl engellediğini ortaya koyarak, yüksek riskli tümörleri daha güvenli ve tedavi edilebilir bir duruma yönlendirmek için potansiyel yeni bir yol gösteriyorlar.
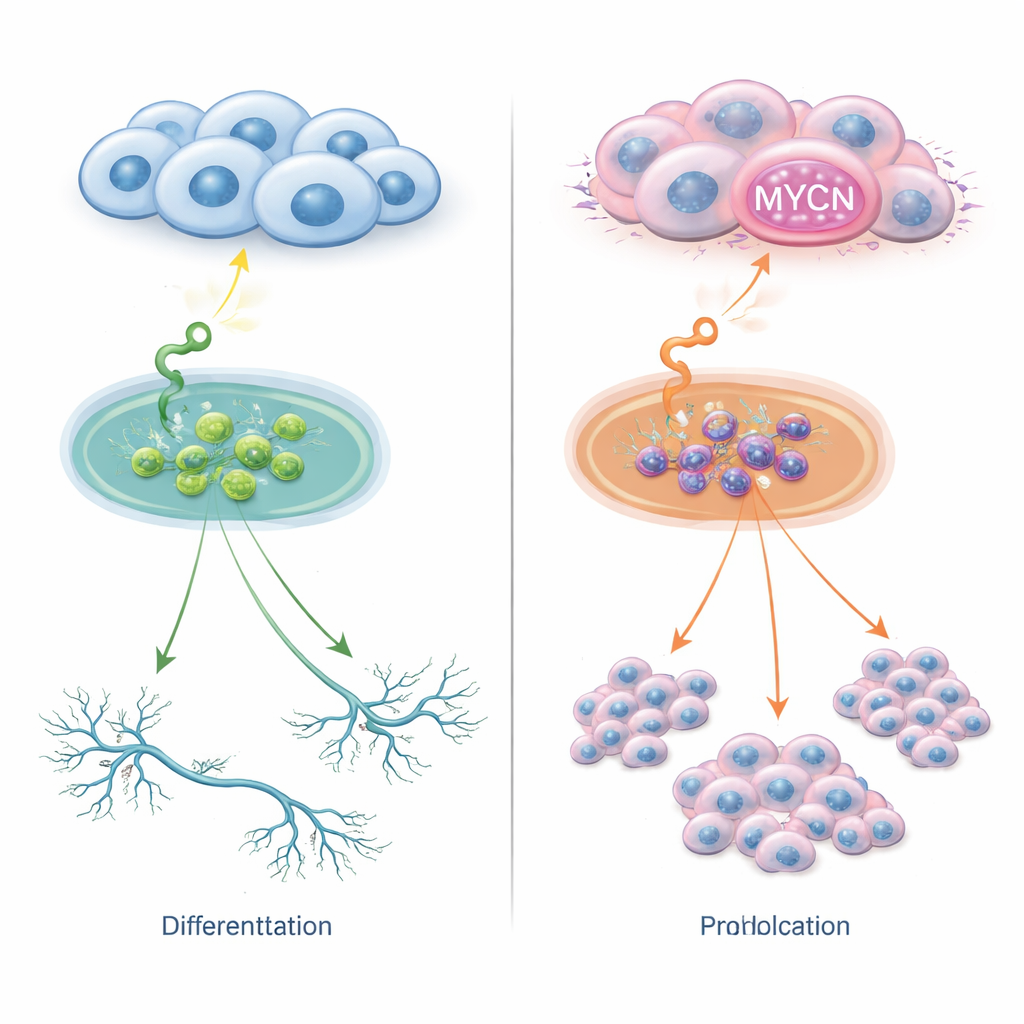
Aynı sinyal için iki yol
Nöroblastom hücrelerinin yüzeyinde çevrelerindeki büyüme faktörlerini algılayan reseptörler bulunur. Bu reseptörlerden biri, NT‑3 molekülünü algılayan TrkC olarak adlandırılır. Normal koşullarda bu eşleşme genç sinir hücrelerinin daha olgun formlara gelişmesini teşvik edebilir. Araştırmacılar, birkaç nöroblastom hücre hattını TrkC taşıyacak şekilde tasarlayıp NT‑3 ile uyardılar. MYCN’nin fazla kopyası olmayan hücrelerde NT‑3, hücreleri uzun, sinir benzeri dallar uzatmaya ve daha olgun bir görünüm edinmeye zorladı; hücre sayısında ise az değişim görüldü. Buna keskin bir tezat oluşturacak şekilde, MYCN çok fazla olan hücrelerde—ya aşırı ifade ya da gen amplifikasyonu yoluyla—aynı NT‑3 sinyali artık farklılaşmayı tetiklemedi; bunun yerine hızlı hücre bölünmesini körükledi. Böylece tek bir dış ipucu, hücrelerin içerdiği MYCN miktarına bağlı olarak ya farklılaşma ya da agresif büyüme yoluna gidebilir.
Hücre içindeki sinyal izlerini izlemek
Bu davranış ayrımının nasıl ortaya çıktığını anlamak için ekip, fosfoproteomik adı verilen bir teknik kullanarak hücre içindeki kimyasal “açma/kapatma” anahtarlarını zaman içinde haritaladı. NT‑3 uyarısından sonra binlerce modifiye proteini farklı hücre hatlarında karşılaştırdılar. MYCN amplifikasyonu olmayan hücreler güçlü ve özgün bir aktivasyon paterni gösterirken, MYCN‑zengin hücrelerde yanıt daha sönük kaldı. Yazarlar en aktif olan sinyal enzilerine odaklandıklarında, farklılaşan hücrelerde tekrarlayan bir oyuncu öne çıktı: protein kinaz A (PKA) yolu ve onun eşlikçisi olan CREB; CREB, çekirdekte farklılaşma için gerekli genleri açan bir düzenleyicidir. Yol analizleri, PKA/CREB aktivitesi arttığında özellikle akson yönlendirme ve sitoskeletal değişiklikler gibi sinir gelişimi ve yapısal yeniden düzenlemeyle ilişkili süreçlerin zenginleştiğini doğruladı.
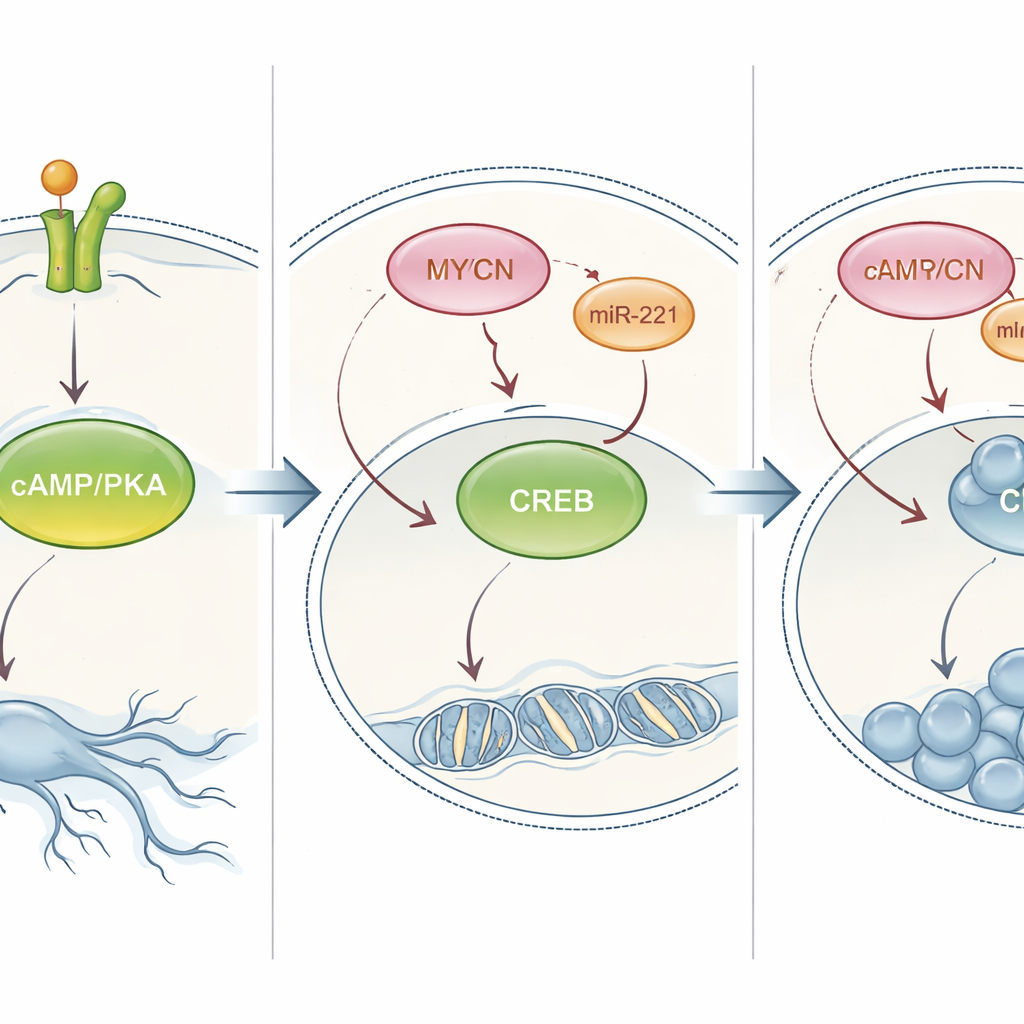
Tümör davranışını değiştirmek için PKA anahtarını çevirmek
Araştırmacılar, bu PKA yolunun gerçekten hücrenin olgunlaşma ile çoğalma arasındaki tercihine hükmedip hükmetmediğini test ettiler. NT‑3’e normalde yanıt verip farklılaşan hücrelerde PKA’yı kimyasal olarak bloke etmek, sinir benzeri uzantıları azalttı ve hücre sayısını artırdı. Genellikle sadece çoğalan MYCN‑amplifiye hücrelerde ise PKA’yı yapay olarak yükseltmek—ya doğal bir habercinin taklidini yapan bir ilaçla ya da hücreleri sürekli aktif PKA veya CREB versiyonları üretmeye zorlayarak—davranışı tersine çevirdi: hücreler bölünmeyi yavaşlattı ve nöronları andıran uzun uzantılar büyüttü. Bu etki sadece petri kutusunda değil, PKA aktivasyonu insan nöroblastom tümörlerinin küçülmesine neden olduğu zebrafish modelinde de gözlendi. Birlikte, bu deneyler PKA/CREB sinyalinin yüksek riskli nöroblastom hücrelerini daha olgun ve daha az tehlikeli bir duruma yönlendirebilen merkezi bir kaldıraç olduğunu gösteriyor.
MYCN ve bir mikroRNA farklılaşma devresini nasıl tıkıyor
Çalışma daha sonra MYCN’nin bu yararlı yolu nasıl kapattığını inceledi. Amplifiye hücrelerde MYCN düzeyleri azaltıldığında PKA ve CREB proteinleri artış gösterdi ve NT‑3 tekrar büyüme yerine farklılaşmayı teşvik etti. Hasta tümör verilerinin analizleri, PKA bileşenlerini kodlayan genlerin MYCN amplifiye tümörlerde diğer vakalara göre daha düşük seviyede ifade edildiğini ortaya koydu; bu da MYCN’nin yüksek riskli hastalardaki bu yolu genel olarak bastığını düşündürüyor. Yazarlar ayrıca MYCN ile güçlü biçimde ilişkili ve kötü sonuçlarla bağlantılı küçük düzenleyici bir RNA olan miR‑221’in rolünü de keşfettiler. Yüksek miR‑221 seviyeleri tümörlerde ve hücre hatlarında MYCN ekspresyonu ile korelasyon gösterdi. MYCN‑amplifiye hücrelerde miR‑221 engellendiğinde CREB düzeyleri yükseldi ve NT‑3 tekrar nöronal olgunlaşmayı tetikleyebildi. Bu, MYCN’nin PKA/CREB devresini anahtar genleri aşağı çevirerek ve CREB’i daha da düşüren miR‑221’i yükselterek çift yönlü bastırdığını gösterir.
Gelecek tedaviler için ne anlama geliyor
Genel olarak, çalışma şu net tabloyu çiziyor: düşük riskli nöroblastomda NT‑3’ün TrkC aracılığıyla ve aktif bir PKA/CREB yoluyla etkisi, olgunlaşmamış tümör hücrelerinin iyi huylu, sinir benzeri hücrelere dönüşmesine yardımcı olur. Ekstra MYCN içeren yüksek riskli tümörlerde ise bu olgunlaşma yolu bloke edilir ve aynı sinyal kısmen miR‑221 mikroRNA’sının da desteğiyle kontrolsüz büyümeyi besleyecek şekilde yönlendirilir. PKA/CREB aktivitesini geri getirerek—bu yolu güçlendiren ilaçlar kullanmak veya MYCN kaynaklı engelleyicileri bastırmak—hekimler bir gün agresif nöroblastomları daha farklılaşmış, tedavi edilebilir tümörlere dönüştürebilirler. Bu strateji, çocukluk çağı kanserlerinde yalnızca kanser hücrelerini öldürmek değil, aynı zamanda onları normal gelişim yoluna geri itmek hedefiyle uyumludur.
Atıf: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Anahtar kelimeler: nöroblastom, MYCN, TrkC, PKA CREB yolu, tümör farklılaşması