Clear Sky Science · sv
MYCN hämmar TrkC‑medierad differentiering i neuroblastomceller via störning av PKA‑signalvägen
Varför denna studie om barncancer är viktig
Neuroblastom är en barncancer som kan uppträda mycket olika: vissa tumörer mognar försiktigt och krymper, medan andra sprider sig aggressivt och motstår behandling. Denna studie ställer en förrädiskt enkel fråga med stora kliniska konsekvenser: varför får vissa signaler vissa neuroblastomceller att växa upp till ofarliga nervliknande celler, medan samma signaler driver andra att multiplicera som cancer? Genom att avslöja hur en kraftfull cancerogen kallad MYCN blockerar en naturlig mognadssignal visar författarna en potentiell ny väg för att tvinga hög‑risk tumörer in i ett säkrare, mer behandlingsbart tillstånd.
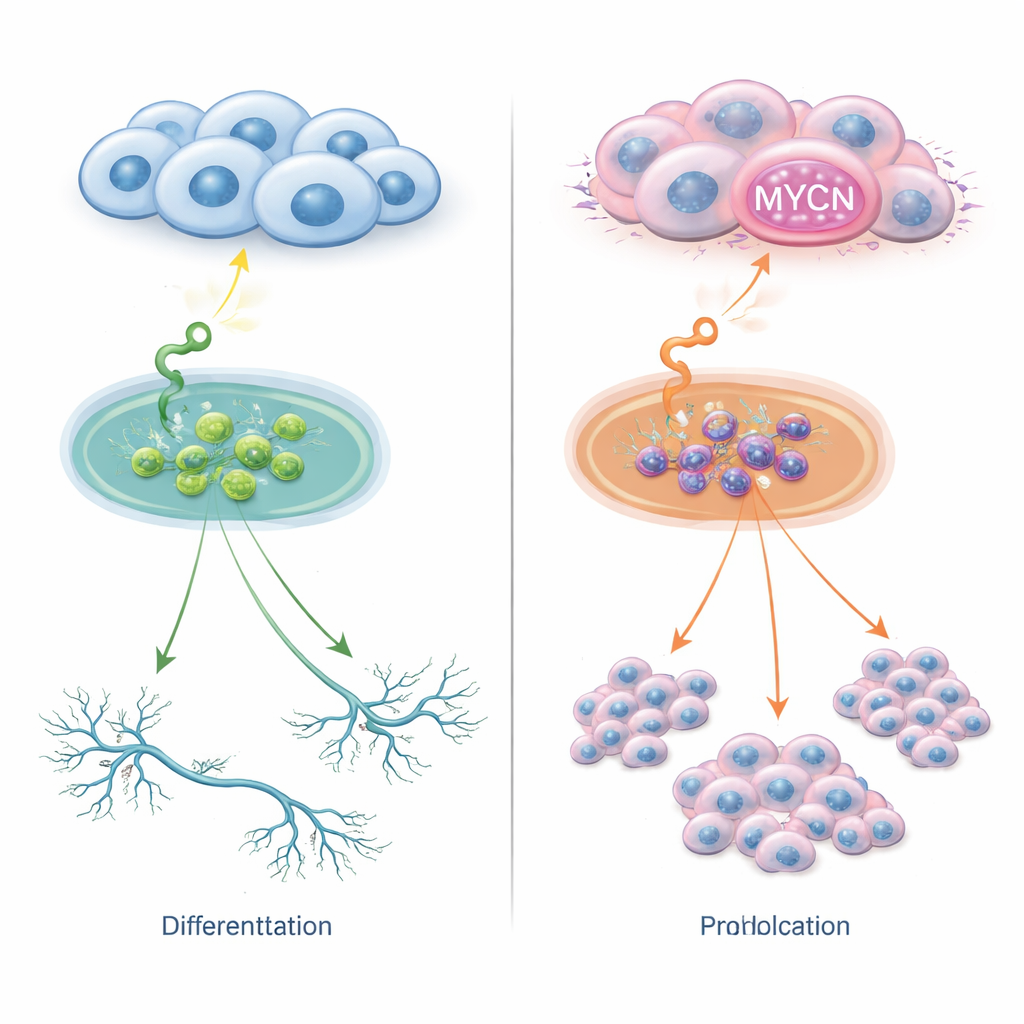
Två vägar för samma signal
Neuroblastomceller bär receptorer på ytan som känner av tillväxtfaktorer i omgivningen. En sådan receptor, TrkC, känner igen ett molekylärt ligandenamn NT‑3. I normala förhållanden kan detta par uppmuntra unga nervceller att utvecklas till mer mogna former. Forskarna konstruerade flera neuroblastomcellinjer för att uttrycka TrkC och stimulerade dem med NT‑3. I celler utan extra kopior av MYCN-genen drev NT‑3 cellerna att skjuta ut långa, nervliknande utskott och anta ett mer moget utseende, med liten förändring i cellantal. I skarp kontrast, i celler med för mycket MYCN—antingen genom överuttryck eller full genamplifikation—utlöste samma NT‑3‑signal ingen mognad utan snarare snabb celldelning. Således kan en enda yttre signal leda till antingen differentiering eller aggressiv tillväxt, beroende på hur mycket MYCN cellerna innehåller.
Följa signalspåren inne i cellen
För att förstå hur denna beteendesplit uppstår kartlade teamet kemiska "på/av"‑brytare inne i cellerna över tid med en teknik kallad fosfoproteomik. De jämförde tusentals modifierade proteiner efter NT‑3‑stimulering i de olika cellinjerna. Celler utan MYCN‑amplifikation visade ett starkt och unikt aktiveringsmönster, medan MYCN‑rika celler hade ett mer dämpat svar. När författarna fokuserade på vilka signaleringsenzym som var mest aktiva trädde en återkommande aktör fram i de differentierande cellerna: proteinkinas A (PKA)‑vägen och dess partner CREB, en reglerare i cellkärnan som slår på gener som behövs för mognad. Väg‑analys bekräftade att processer kopplade till nervutveckling och strukturell ombyggnad—såsom axonledning och cytoskelettförändringar—var särskilt förhöjda när PKA/CREB‑aktiviteten ökade.
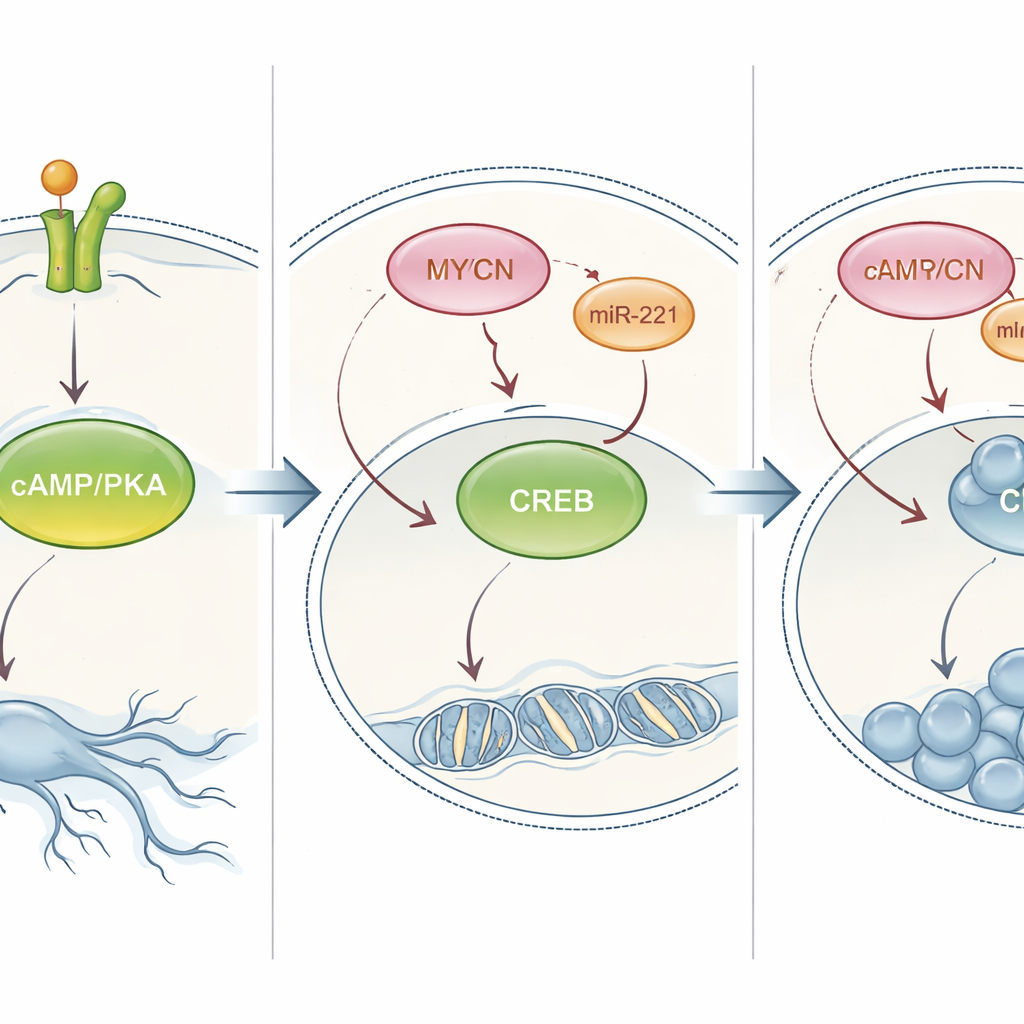
Vippa PKA‑brytaren för att ändra tumörbeteendet
Forskarna testade därefter om denna PKA‑väg verkligen styr cellens val mellan mognad och multiplikation. I celler som normalt differentierade vid NT‑3 minskade kemisk blockering av PKA deras nervliknande utskott och ökade cellantalet. I MYCN‑amplifierade celler som vanligen endast prolifererar vände artificiell förstärkning av PKA—antingen med ett läkemedel som imiterar en naturlig budbärare eller genom att tvinga cellerna att producera ständigt aktiva varianter av PKA eller CREB—deras beteende: cellerna saktade ned delningen och bildade långa processer som liknade neuroner. Denna effekt höll i sig inte bara i cellodlingar utan också i en zebrafiskmodell, där aktivering av PKA fick inplanterade mänskliga neuroblastomtumörer att krympa. Tillsammans visar dessa experiment att PKA/CREB‑signalering är en central spak som kan styra om hög‑risk neuroblastom mot ett mer moget, mindre farligt tillstånd.
Hur MYCN och en mikroRNA blockerar differentieringskretsen
Studien undersökte sedan hur MYCN stänger ner denna gynnsamma väg. När MYCN‑nivåerna minskades i amplifierade celler ökade PKA‑ och CREB‑proteinerna, och NT‑3 främjade återigen differentiering istället för tillväxt. Analyser av patienttumördata visade att gener som kodar för PKA‑komponenter uttrycks på lägre nivåer i MYCN‑amplifierade tumörer än i andra fall, vilket tyder på att MYCN överlag dämpar denna väg hos barn med hög‑risk‑sjukdom. Författarna upptäckte också en roll för en liten reglerande RNA, miR‑221, som starkt korrelerar med MYCN och dålig prognos. Höga nivåer av miR‑221 korrelerade med MYCN‑uttryck både i tumörer och cellinjer. När miR‑221 blockerades i MYCN‑amplifierade celler steg CREB‑nivåerna och NT‑3 kunde återigen driva neuronal mognad. Detta indikerar att MYCN undertrycker PKA/CREB‑kretsen både genom att dämpa viktiga gener och genom att höja miR‑221, vilket ytterligare sänker CREB.
Vad detta innebär för framtida behandlingar
Sammanfattningsvis målar arbetet en tydlig bild: i låg‑risk neuroblastom hjälper NT‑3 via TrkC och en aktiv PKA/CREB‑väg omogna tumörceller att växa upp till benigna, nervliknande celler. I hög‑risk tumörer med extra MYCN blockeras denna matureringsväg, och samma signal omdirigeras för att driva okontrollerad tillväxt, delvis underlättad av mikroRNA‑et miR‑221. Genom att återställa PKA/CREB‑aktivitet—med läkemedel som stärker denna väg eller genom att dämpa MYCN‑styrda blockeringar—kan kliniker en dag kanske omvandla aggressiva neuroblastom till mer differentierade, behandlingsbara tumörer. Denna strategi ligger i linje med ett bredare terapeutiskt mål inom barnonkologi: inte bara att döda cancerceller, utan att styra dem tillbaka mot en normal utvecklingsbana.
Citering: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Nyckelord: neuroblastom, MYCN, TrkC, PKA CREB‑väg, tumördifferentiering