Clear Sky Science · ru
MYCN подавляет дифференцировку, опосредованную TrkC, в клетках нейробластомы через нарушение сигнального пути PKA
Почему это исследование детской онкологии важно
Нейробластома — детский рак, который может вести себя очень по‑разному: одни опухоли спокойно созревают и уменьшаются, тогда как другие широко метастазируют и устойчивы к лечению. В этом исследовании поставлен на первый взгляд простой, но клинически значимый вопрос: почему одни сигналы побуждают некоторые клетки нейробластомы созревать в безвредные нервоподобные клетки, тогда как у других те же сигналы ведут к их размножению как у рака? Раскрывая, как мощный онкоген MYCN блокирует естественный сигнал к созреванию, авторы показывают потенциально новый способ склонить опухоли высокого риска к более безопасному и лечениюподдающемуся состоянию.
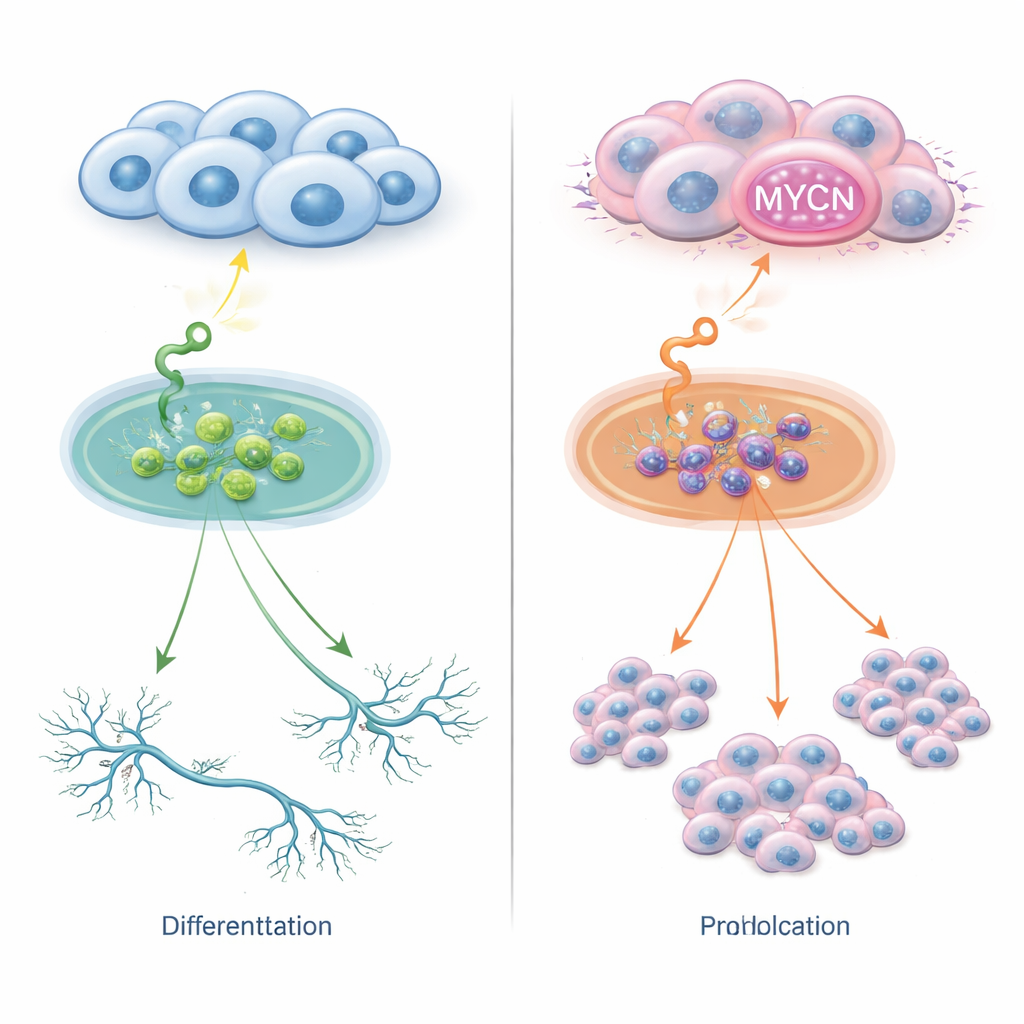
Два пути для одного и того же сигнала
Клетки нейробластомы несут на поверхности рецепторы, которые улавливают факторы роста в окружении. Один из таких рецепторов, называемый TrkC, реагирует на молекулу NT‑3. В обычных условиях это взаимодействие может стимулировать юные нервные клетки к развитию в более зрелые формы. Исследователи модифицировали несколько линий клеток нейробластомы так, чтобы те экспрессировали TrkC, и затем стимулировали их NT‑3. В клетках без увеличенного числа копий гена MYCN NT‑3 вызывал вытягивание длинных нервоподобных отростков и приобретение более зрелого вида при минимальном изменении числа клеток. В резком контрасте, в клетках с избытком MYCN — при его сверхэкспрессии или амплификации гена — тот же сигнал NT‑3 больше не вызывал созревания, а вместо этого стимулировал быстрое деление. Таким образом, один внешний сигнал может привести либо к дифференцировке, либо к агрессивному росту — в зависимости от количества MYCN в клетках.
Отслеживая следы сигналов внутри клетки
Чтобы понять, как возникает такое расхождение в поведении, команда картировала химические «вкл/выкл» переключатели внутри клеток с течением времени, используя метод фосфопротеомики. Они сравнили тысячи модифицированных белков после стимуляции NT‑3 в разных линиях. Клетки без амплификации MYCN продемонстрировали сильный и уникальный паттерн активации, тогда как ответ в клетках с высоким уровнем MYCN был более приглушён. При фокусировании на наиболее активных сигнальных ферментах в дифференцирующихся клетках выделялся повторяющийся участник: путь протеинкиназы A (PKA) и её партнёр CREB, регулятор в ядре клетки, включающий гены, необходимые для созревания. Анализ путей подтвердил, что процессы, связанные с развитием нервной ткани и перестройкой структуры — такие как навигация аксонов и изменения цитоскелета — обогащены именно при повышении активности PKA/CREB.
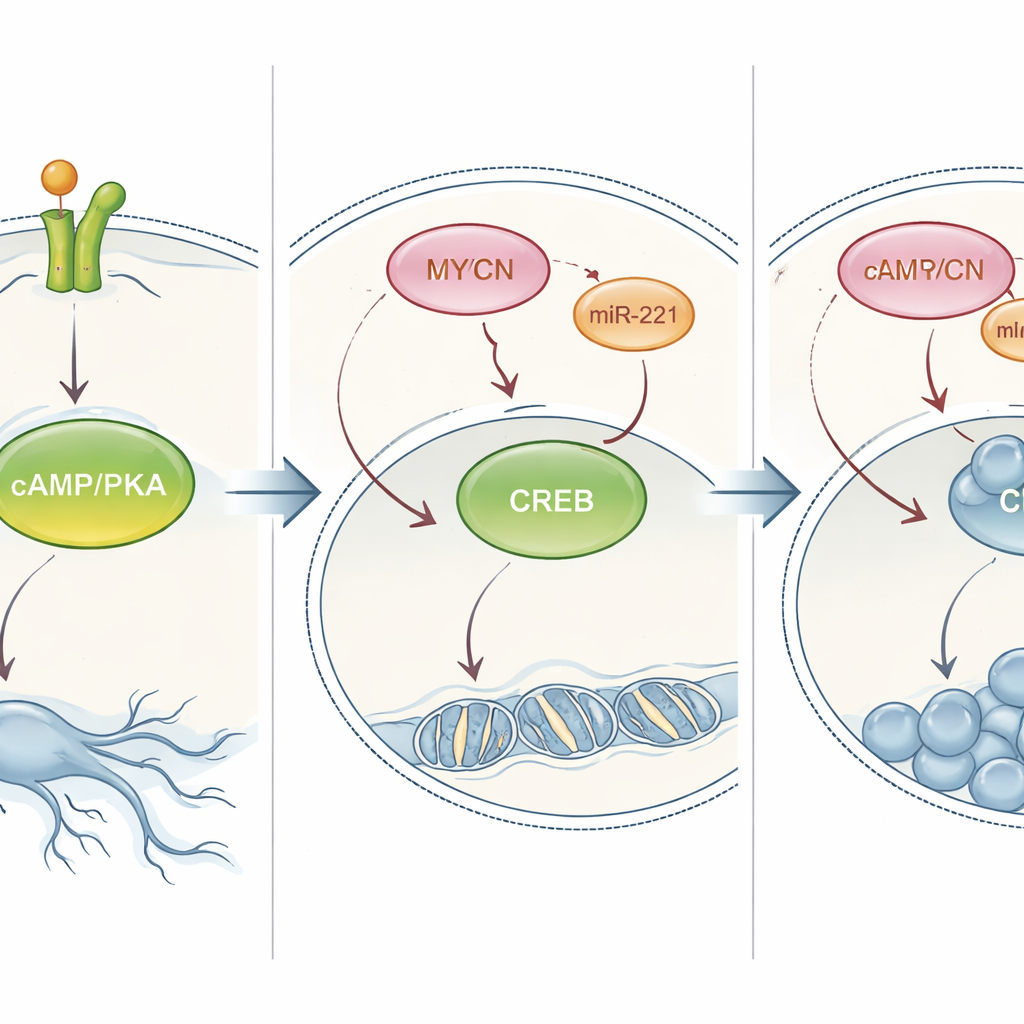
Переключение PKA, чтобы изменить поведение опухоли
Затем исследователи проверили, действительно ли путь PKA управляет выбором клетки между созреванием и размножением. В клетках, которые обычно дифференцируются в ответ на NT‑3, химическое блокирование PKA уменьшало их нервоподобные отростки и увеличивало число клеток. В клетках с амплификацией MYCN, которые обычно лишь пролиферируют, искусственное усиление PKA — либо с помощью препарата, имитирующего естественный посредник, либо путём принудительной экспрессии постоянно активных форм PKA или CREB — изменяло их поведение: клетки замедляли деление и развивали длинные отростки, похожие на нейрональные. Этот эффект наблюдался не только в культурах, но и в модели на данио‑русо (зебровой рыбке), где активация PKA вызывала уменьшение имплантированных человеческих опухолей нейробластомы. В совокупности эти эксперименты показывают, что сигнализация PKA/CREB является центральным рычагом, способным перенаправить клетки нейробластомы высокого риска в более зрелое, менее опасное состояние.
Как MYCN и микроРНК блокируют цепь дифференцировки
Далее исследование рассмотрело, как MYCN выключает этот полезный путь. При снижении уровней MYCN в амплифицированных клетках уровни белков PKA и CREB возрастали, и NT‑3 снова стимулировал дифференцировку вместо роста. Анализ данных опухолей пациентов показал, что гены, кодирующие компоненты PKA, экспрессируются на более низком уровне в опухолях с амплификацией MYCN по сравнению с другими случаями, что указывает на то, что MYCN в целом подавляет этот путь у детей с опухолью высокого риска. Авторы также выявили роль небольшой регуляторной РНК — miR‑221, которая тесно связана с MYCN и неблагоприятным прогнозом. Высокие уровни miR‑221 коррелировали с экспрессией MYCN как в опухолях, так и в клеточных линиях. При блокировании miR‑221 в клетках с амплификацией MYCN уровни CREB повышались, и NT‑3 вновь мог вызывать нейрональную дифференцировку. Это указывает на то, что MYCN подавляет цепь PKA/CREB как посредством понижения ключевых генов, так и через повышение miR‑221, что дополнительно снижает CREB.
Что это означает для будущего лечения
В целом работа рисует ясную картину: при низкорисковой нейробластоме NT‑3 через TrkC и активный путь PKA/CREB помогает незрелым опухолевым клеткам созревать в доброкачественные нервоподобные клетки. В опухолях высокого риска с избытком MYCN этот маршрут созревания блокируется, и тот же сигнал перенаправляется на питание неконтролируемого роста, чему частично способствует микроРНК miR‑221. Восстанавливая активность PKA/CREB — с помощью препаратов, усиливающих этот путь, или путем подавления блокирующих эффектов, индуцируемых MYCN — клиницисты в будущем, возможно, смогут превратить агрессивные нейробластомы в более дифференцированные, поддающиеся лечению опухоли. Эта стратегия согласуется с более широкой терапевтической целью в педиатрической онкологии: не только уничтожать раковые клетки, но и направлять их обратно на нормальную траекторию развития.
Цитирование: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Ключевые слова: нейробластома, MYCN, TrkC, путь PKA CREB, дифференцировка опухоли