Clear Sky Science · fr
MYCN inhibe la différenciation médiée par TrkC dans les cellules de neuroblastome via la perturbation de la voie de signalisation PKA
Pourquoi cette étude sur le cancer pédiatrique est importante
Le neuroblastome est un cancer de l’enfant qui peut évoluer de façons très différentes : certains tumeurs mûrissent doucement puis régressent, tandis que d’autres se disséminent de manière agressive et résistent au traitement. Cette étude pose une question apparemment simple mais aux lourdes conséquences cliniques : pourquoi certains signaux poussent-ils des cellules de neuroblastome à se transformer en cellules nerveuses inoffensives, alors que chez d’autres ils stimulent la prolifération cancéreuse ? En révélant comment un gène oncogénique puissant, MYCN, bloque un signal naturel de maturation, les auteurs mettent en lumière une nouvelle approche possible pour inciter les tumeurs à haut risque à adopter un état plus sûr et plus traitable.
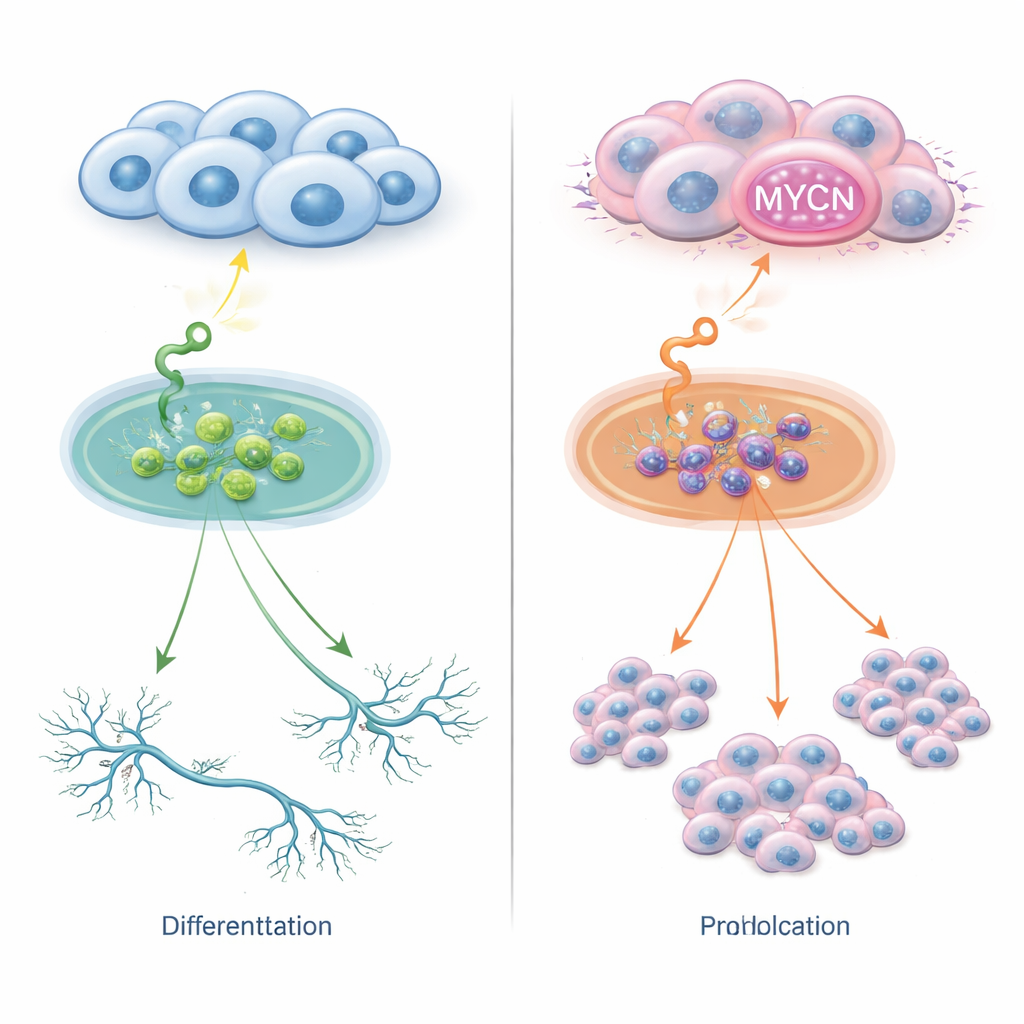
Deux destins pour un même signal
Les cellules de neuroblastome portent à leur surface des récepteurs qui détectent les facteurs de croissance du milieu. Un de ces récepteurs, appelé TrkC, détecte une molécule nommée NT‑3. Dans des conditions normales, cette interaction peut encourager les cellules nerveuses immatures à se développer en formes plus matures. Les chercheurs ont introduit TrkC dans plusieurs lignées de neuroblastome puis les ont stimulées avec NT‑3. Dans les cellules sans copies supplémentaires du gène MYCN, NT‑3 a poussé les cellules à étendre de longs prolongements de type nerveux et à adopter une apparence plus mature, sans variation notable du nombre de cellules. En contraste marqué, dans les cellules présentant un excès de MYCN — par surexpression ou amplification génique — ce même signal NT‑3 n’a plus déclenché la maturation mais a au contraire alimenté une division cellulaire rapide. Ainsi, un seul signal externe peut conduire soit à la différenciation, soit à une croissance agressive, selon la quantité de MYCN présente dans les cellules.
Suivre les traces du signal à l’intérieur de la cellule
Pour comprendre comment cette bifurcation de comportement survient, l’équipe a cartographié les interrupteurs chimiques d’activation/inactivation à l’intérieur des cellules au fil du temps en utilisant une technique appelée phosphoprotéomique. Ils ont comparé des milliers de protéines modifiées après stimulation par NT‑3 dans les différentes lignées cellulaires. Les cellules sans amplification de MYCN ont montré un motif d’activation fort et spécifique, tandis que les cellules riches en MYCN ont eu une réponse plus atténuée. En se concentrant sur les enzymes de signalisation les plus actives, un acteur récurrent s’est détaché dans les cellules en différenciation : la voie de la protéine kinase A (PKA) et son partenaire CREB, un régulateur nucléaire qui active des gènes nécessaires à la maturation. L’analyse des voies a confirmé que des processus liés au développement nerveux et au remodelage structurel — tels que le guidage des axones et les modifications du cytosquelette — étaient enrichis spécifiquement quand l’activité PKA/CREB augmentait.
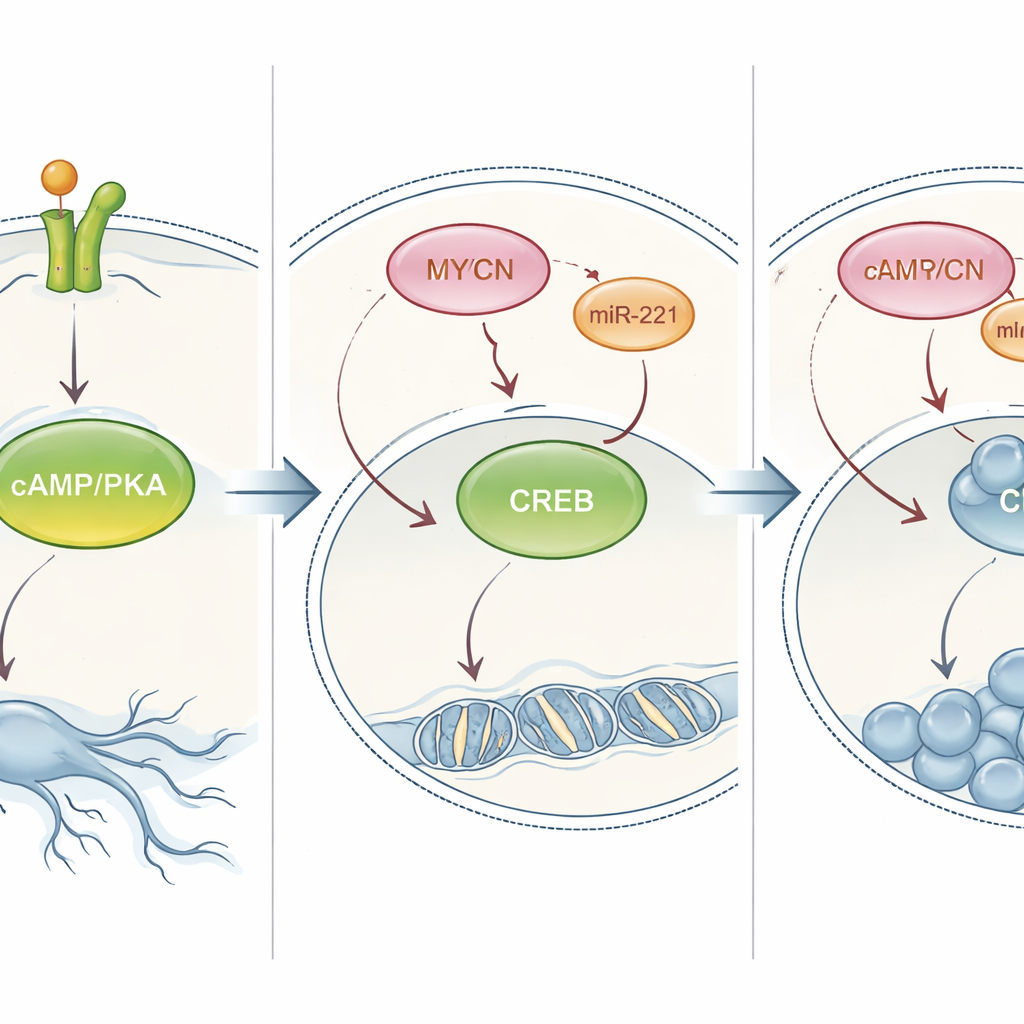
Inverser l’interrupteur PKA pour modifier le comportement tumoral
Les chercheurs ont ensuite testé si cette voie PKA contrôlait véritablement le choix de la cellule entre maturation et prolifération. Dans les cellules qui se différenciaient normalement en réponse à NT‑3, le blocage chimique de la PKA a réduit leurs prolongements de type nerveux et augmenté le nombre de cellules. Dans les cellules amplifiées en MYCN qui proliféraient habituellement, l’activation artificielle de la PKA — soit par un médicament mimant un messager naturel, soit en forçant l’expression de formes toujours actives de PKA ou de CREB — a inversé leur comportement : les cellules ont ralenti leur division et développé de longs prolongements semblables à des neurones. Cet effet s’est observé non seulement en culture cellulaire mais aussi dans un modèle de poisson zèbre, où l’activation de la PKA a entraîné la réduction de tumeurs humaines de neuroblastome implantées. Ensemble, ces expériences montrent que la signalisation PKA/CREB est un levier central pouvant orienter des cellules de neuroblastome à haut risque vers un état plus mature et moins dangereux.
Comment MYCN et un microARN grippent le circuit de différenciation
L’étude a ensuite examiné comment MYCN éteint cette voie bénéfique. Lorsque les niveaux de MYCN ont été réduits dans des cellules amplifiées, les protéines PKA et CREB ont augmenté, et NT‑3 a de nouveau favorisé la différenciation plutôt que la croissance. L’analyse des données tumorales de patients a révélé que les gènes codant pour des composants de la PKA sont exprimés à des niveaux plus faibles dans les tumeurs amplifiées en MYCN que dans les autres cas, suggérant que MYCN atténue largement cette voie chez les enfants atteints de formes à haut risque. Les auteurs ont également mis au jour un rôle pour un petit ARN régulateur, miR‑221, fortement associé à MYCN et à de mauvais pronostics. Des niveaux élevés de miR‑221 corrélaient avec l’expression de MYCN tant dans les tumeurs que dans les lignées cellulaires. Lorsque miR‑221 a été bloqué dans des cellules amplifiées en MYCN, les niveaux de CREB ont augmenté et NT‑3 a pu à nouveau induire la maturation neuronale. Cela indique que MYCN supprime le circuit PKA/CREB à la fois en réprimant des gènes clés et en élevant miR‑221, qui abaisse encore CREB.
Implications pour les traitements futurs
Globalement, ce travail dresse un tableau net : dans le neuroblastome à faible risque, NT‑3 agissant via TrkC et une voie PKA/CREB active aide les cellules tumorales immatures à mûrir en cellules nerveuses bénignes. Dans les tumeurs à haut risque avec amplification de MYCN, cette voie de maturation est bloquée et le même signal est réacheminé pour alimenter une croissance incontrôlée, aidé en partie par le microARN miR‑221. En restaurant l’activité PKA/CREB — par des médicaments qui stimulent cette voie ou en atténuant les inhibiteurs induits par MYCN — les cliniciens pourraient un jour convertir des neuroblastomes agressifs en tumeurs plus différenciées et plus traitables. Cette stratégie s’inscrit dans un objectif thérapeutique plus large en oncologie pédiatrique : ne pas seulement tuer les cellules cancéreuses, mais les ramener sur une voie de développement normale.
Citation: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Mots-clés: neuroblastome, MYCN, TrkC, voie PKA CREB, différenciation tumorale