Clear Sky Science · de
MYCN hemmt TrkC-vermittelte Differenzierung in Neuroblastomzellen durch Störung des PKA-Signalwegs
Warum diese Studie zu kindlichem Krebs wichtig ist
Neuroblastom ist ein kindlicher Krebs, der sich sehr unterschiedlich verhalten kann: Manche Tumoren reifen still und schrumpfen, andere breiten sich aggressiv aus und sind therapieresistent. Diese Studie stellt eine auf den ersten Blick einfache Frage mit großen klinischen Folgen: Warum treiben bestimmte Signale einige Neuroblastomzellen dazu, zu harmlosen, nervenähnlichen Zellen heranzuwachsen, während dieselben Signale andere Zellen zur Vermehrung als Krebszellen anregen? Indem die Autoren aufdecken, wie ein starkes Krebsgen namens MYCN ein natürliches Reifungssignal blockiert, zeigen sie einen möglichen neuen Weg, Hochrisiko-Tumoren in einen sichereren, besser behandelbaren Zustand zu lenken.
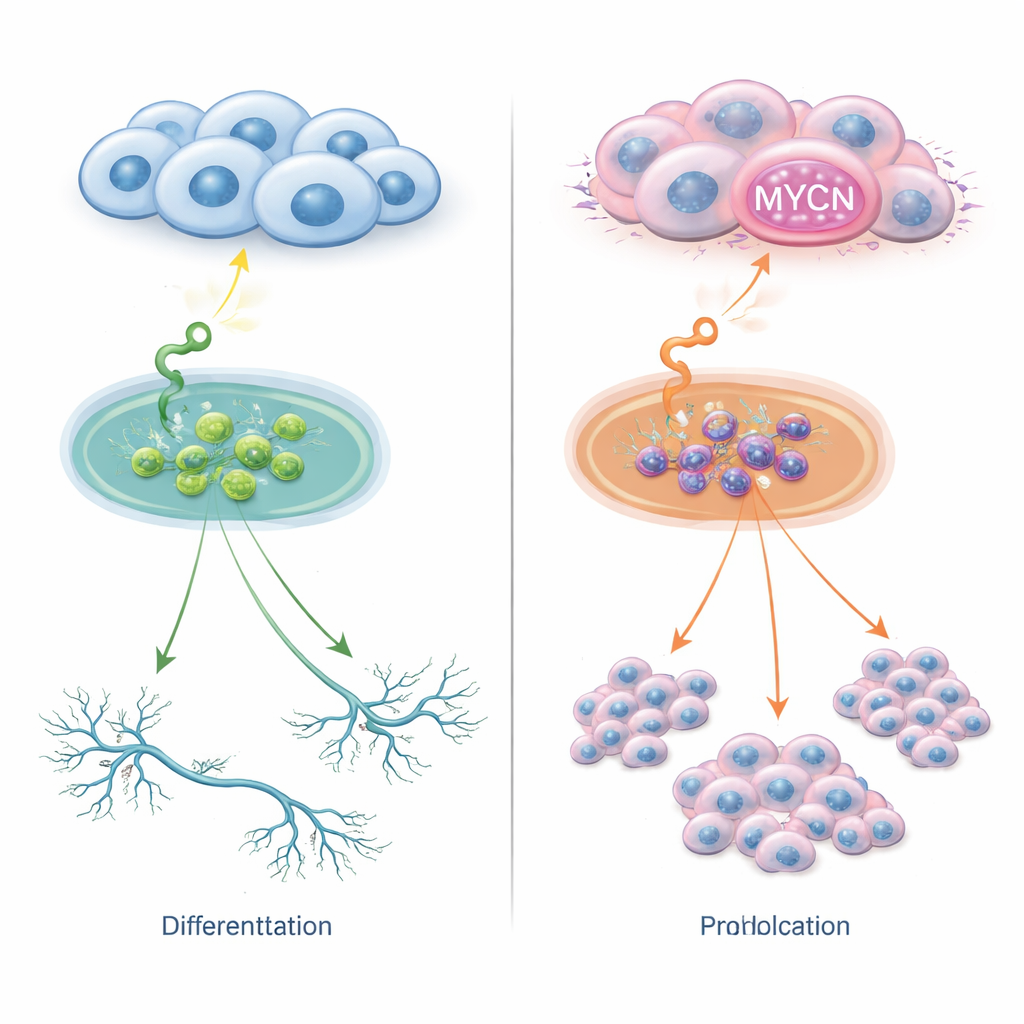
Zwei Wege für dasselbe Signal
Neuroblastomzellen tragen Rezeptoren auf ihrer Oberfläche, die Wachstumsfaktoren in ihrer Umgebung wahrnehmen. Einer dieser Rezeptoren, TrkC genannt, erkennt ein Molekül namens NT‑3. Unter normalen Bedingungen kann diese Partnerschaft junge Nervenzellen zur weiteren Reifung anregen. Die Forscher statteten mehrere Neuroblastomzelllinien mit TrkC aus und stimulierten sie mit NT‑3. In Zellen ohne zusätzliche Kopien des MYCN-Gens veranlasste NT‑3 die Zellen, lange, nervenähnliche Fortsätze auszubilden und ein reiferes Erscheinungsbild anzunehmen, bei kaum veränderter Zellzahl. Im krassen Gegensatz dazu führte dasselbe NT‑3-Signal in Zellen mit zu viel MYCN — durch Überexpression oder Genamplifikation — nicht zur Reifung, sondern förderte stattdessen schnelle Zellteilung. Ein einziges externes Signal kann also entweder Differenzierung oder aggressives Wachstum auslösen, abhängig davon, wie viel MYCN die Zellen enthalten.
Den Signaturspuren im Inneren der Zelle folgen
Um zu verstehen, wie diese Verhaltensaufspaltung entsteht, kartierte das Team chemische "An/Aus"-Schalter in den Zellen über die Zeit mithilfe einer Technik namens Phosphoproteomik. Sie verglichen Tausende modifizierter Proteine nach NT‑3-Stimulation in den verschiedenen Zelllinien. Zellen ohne MYCN-Amplifikation zeigten ein starkes und spezifisches Aktivierungsmuster, während MYCN-reiche Zellen eine abgeschwächtere Antwort aufwiesen. Als die Autoren sich darauf konzentrierten, welche Signalkinasen am aktivsten waren, stach in den differenzierenden Zellen ein wiederkehrender Akteur hervor: der Protein-Kinase-A-(PKA)-Weg und sein Partner CREB, ein Regulator im Zellkern, der Gene für die Reifung anschaltet. Die Pfadanalyse bestätigte, dass Prozesse, die mit Nerventwicklung und strukturellem Umbau zu tun haben — etwa Achslenkung und Veränderungen des Zytoskeletts — speziell angereichert waren, wenn PKA/CREB-Aktivität zunahm.
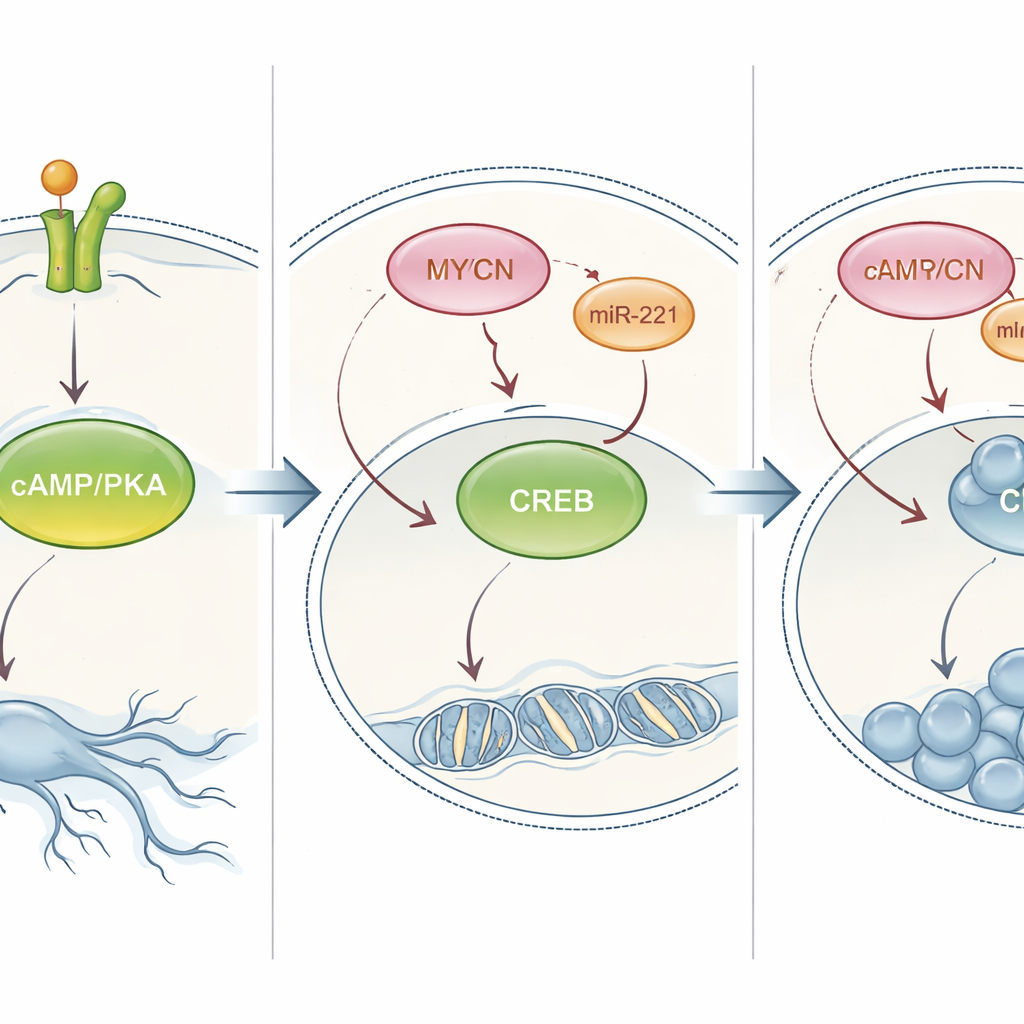
Den PKA-Schalter umlegen, um das Tumorverhalten zu ändern
Die Forscher prüften anschließend, ob dieser PKA-Weg tatsächlich die Entscheidung der Zelle zwischen Reifung und Vermehrung steuert. In Zellen, die normalerweise als Reaktion auf NT‑3 differenzierten, verringerte das chemische Blockieren von PKA ihre nervenähnlichen Auswüchse und erhöhte die Zellzahlen. In MYCN-amplifizierten Zellen, die normalerweise nur proliferieren, kehrte ein künstliches Anheben von PKA — entweder mit einem Wirkstoff, der einen natürlichen Botenstoff nachahmt, oder durch das Erzeugen ständig aktiver Formen von PKA oder CREB — ihr Verhalten um: Die Zellen teilten sich langsamer und bildeten lange Fortsätze, die Neuronen ähnelten. Dieser Effekt zeigte sich nicht nur in Zellkulturen, sondern auch in einem Zebrafischmodell, wo die Aktivierung von PKA implantierte menschliche Neuroblastomtumoren schrumpfen ließ. Zusammengenommen zeigen diese Experimente, dass PKA/CREB-Signale ein zentraler Hebel sind, mit dem sich Hochrisiko-Neuroblastomzellen in einen reiferen, weniger gefährlichen Zustand umleiten lassen.
Wie MYCN und ein microRNA den Differenzierungsweg blockieren
Die Studie untersuchte anschließend, wie MYCN diesen vorteilhaften Weg abschaltet. Wenn MYCN-Spiegel in amplifizierten Zellen reduziert wurden, stiegen PKA- und CREB-Proteine an, und NT‑3 förderte wieder Differenzierung statt Wachstum. Analysen von Patiententumordaten zeigten, dass Gene, die PKA-Komponenten kodieren, in MYCN-amplifizierten Tumoren niedriger exprimiert sind als in anderen Fällen, was darauf hindeutet, dass MYCN diesen Weg bei Kindern mit Hochrisiko-Erkrankung allgemein dämpft. Die Autoren entdeckten außerdem eine Rolle für eine kleine regulatorische RNA, miR‑221, die stark mit MYCN und schlechter Prognose assoziiert ist. Hohe miR‑221-Spiegel korrelierten mit MYCN-Expression in Tumoren und Zelllinien. Wenn miR‑221 in MYCN-amplifizierten Zellen blockiert wurde, stiegen CREB-Spiegel an und NT‑3 konnte erneut die neuronale Reifung antreiben. Das deutet darauf hin, dass MYCN die PKA/CREB-Schaltung sowohl durch das Herunterregulieren wichtiger Gene als auch durch Anheben von miR‑221 unterdrückt, was CREB weiter reduziert.
Was das für zukünftige Behandlungen bedeutet
Insgesamt zeichnet die Arbeit ein klares Bild: Im Niedrigrisiko-Neuroblastom hilft NT‑3 über TrkC und einen aktiven PKA/CREB-Weg unreifen Tumorzellen, zu gutartigen, nervenähnlichen Zellen heranzuwachsen. In Hochrisiko-Tumoren mit zusätzlichem MYCN ist dieser Reifungsweg blockiert, und dasselbe Signal wird umgeleitet, um unkontrolliertes Wachstum zu fördern, teils vermittelt durch die microRNA miR‑221. Durch Wiederherstellen der PKA/CREB-Aktivität — etwa mit Wirkstoffen, die diesen Weg stärken, oder durch Abschwächen von MYCN-vermittelten Blockaden — könnten Kliniker eines Tages aggressive Neuroblastome in stärker differenzierte, besser behandelbare Tumoren umwandeln. Diese Strategie fügt sich in ein breiteres therapeutisches Ziel bei kindlichem Krebs ein: nicht nur Krebszellen abzutöten, sondern sie wieder auf einen normalen Entwicklungsweg zu lenken.
Zitation: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Schlüsselwörter: Neuroblastom, MYCN, TrkC, PKA-CREB-Signalweg, Tumor-Differenzierung