Clear Sky Science · es
MYCN inhibe la diferenciación mediada por TrkC en células de neuroblastoma mediante la interrupción de la vía de señalización PKA
Por qué importa este estudio sobre el cáncer infantil
El neuroblastoma es un cáncer infantil que puede comportarse de maneras muy distintas: algunos tumores maduran silenciosamente y se reducen, mientras que otros se diseminan agresivamente y resisten el tratamiento. Este estudio plantea una pregunta aparentemente simple con grandes consecuencias clínicas: ¿por qué ciertas señales inducen a algunas células de neuroblastoma a madurar en células inofensivas similares a neuronas, pero empujan a otras a multiplicarse como cáncer? Al descubrir cómo un potente gen canceroso llamado MYCN bloquea una señal natural de maduración, los autores revelan una posible vía para inducir a tumores de alto riesgo a un estado más seguro y tratable.
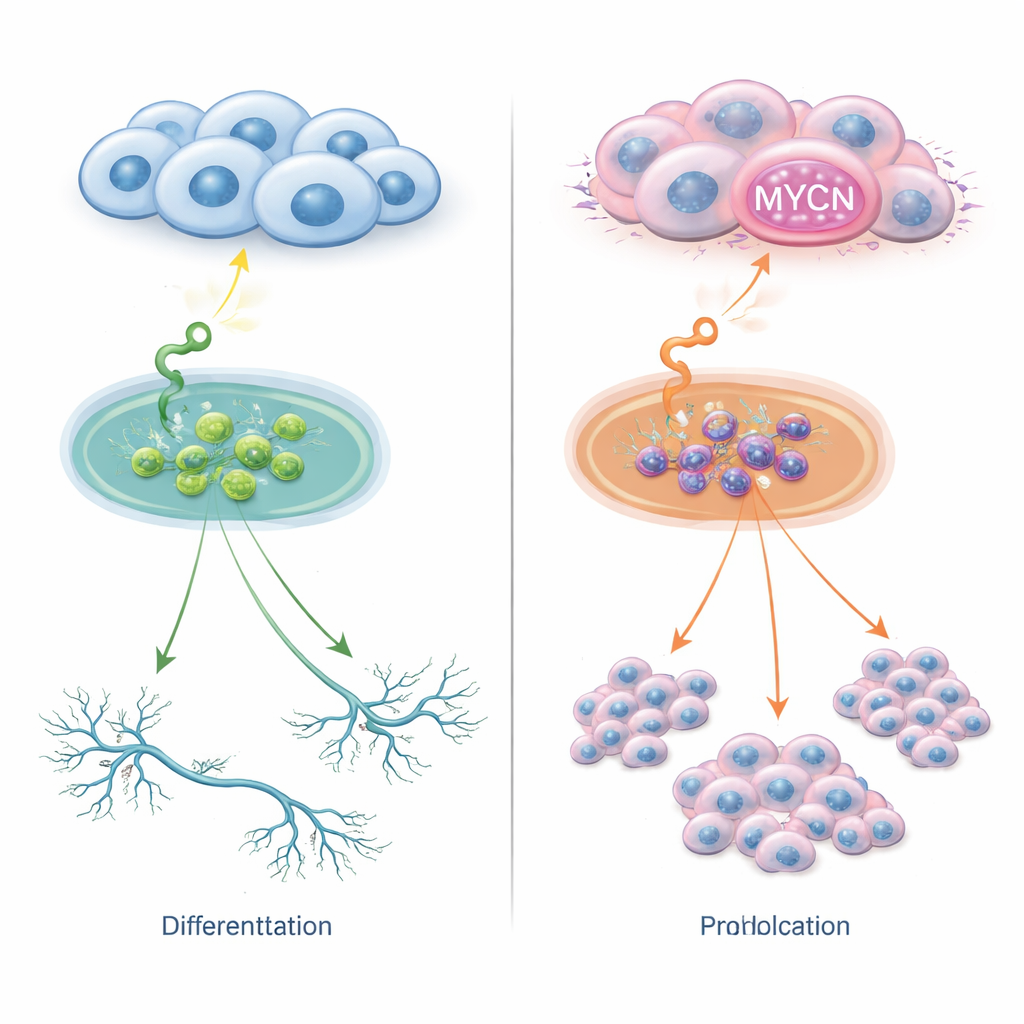
Dos caminos para la misma señal
Las células de neuroblastoma tienen receptores en su superficie que detectan factores de crecimiento en su entorno. Uno de esos receptores, llamado TrkC, percibe una molécula denominada NT‑3. En condiciones habituales, esta pareja puede favorecer que las células nerviosas jóvenes se desarrollen hacia formas más maduras. Los investigadores diseñaron varias líneas celulares de neuroblastoma para expresar TrkC y luego las estimularon con NT‑3. En células sin copias adicionales del gen MYCN, NT‑3 impulsó a las células a extender largas ramas tipo nervio y a adoptar una apariencia más madura, con poco cambio en el número de células. En marcado contraste, en células con exceso de MYCN —ya sea por sobreexpresión o por amplificación completa del gen— la misma señal de NT‑3 dejó de inducir la maduración y, en cambio, alimentó una rápida división celular. Así, una sola señal externa puede conducir tanto a la diferenciación como al crecimiento agresivo, según la cantidad de MYCN que contengan las células.
Siguiendo las huellas de señalización dentro de la célula
Para entender cómo surge esta bifurcación de comportamientos, el equipo cartografió los interruptores químicos de “encendido/apagado” dentro de las células a lo largo del tiempo mediante una técnica llamada fosfoproteómica. Compararon miles de proteínas modificadas tras la estimulación con NT‑3 en las distintas líneas celulares. Las células sin amplificación de MYCN mostraron un patrón de activación fuerte y característico, mientras que las células ricas en MYCN tuvieron una respuesta más atenuada. Cuando los autores se centraron en qué enzimas de señalización estaban más activas, destacó un actor recurrente en las células que diferenciaban: la vía de la proteína quinasa A (PKA) y su socia CREB, un regulador nuclear que activa genes necesarios para la maduración. El análisis de vías confirmó que los procesos relacionados con el desarrollo nervioso y la remodelación estructural —como la orientación axonal y los cambios del citoesqueleto— se enriquecieron específicamente cuando aumentó la actividad PKA/CREB.
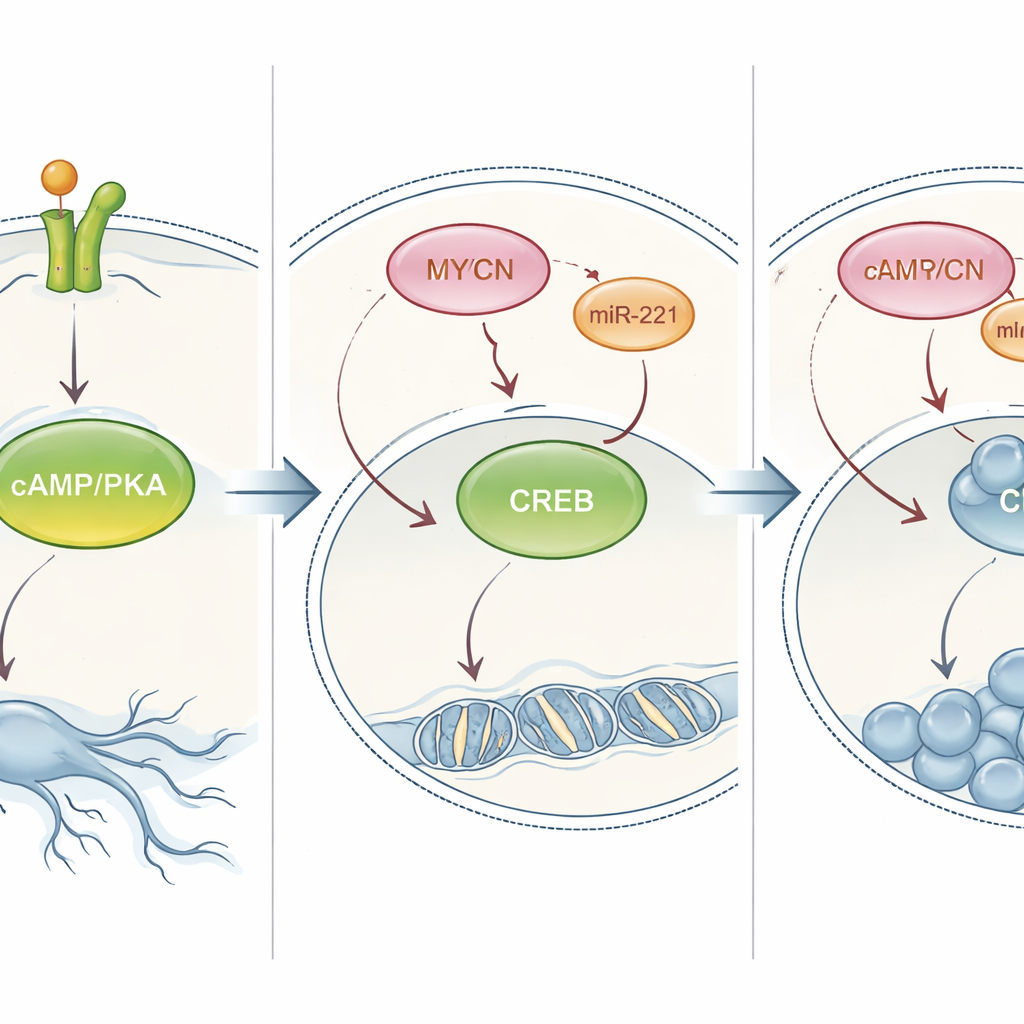
Accionar el interruptor PKA para cambiar el comportamiento tumoral
Los investigadores probaron a continuación si esta vía PKA controla realmente la elección celular entre madurar o multiplicarse. En células que normalmente se diferenciaban en respuesta a NT‑3, bloquear químicamente la PKA redujo sus extensiones tipo nervio e incrementó el número de células. En células con amplificación de MYCN que normalmente sólo proliferan, aumentar artificialmente la PKA —ya sea con un fármaco que imita un mensajero natural o forzando a las células a producir versiones siempre activas de PKA o de CREB— revirtió su comportamiento: las células ralentizaron la división y crecieron largos procesos similares a neuronas. Este efecto se mantuvo no solo en placas de cultivo sino también en un modelo de pez cebra, donde la activación de PKA causó la reducción de tumores humanos de neuroblastoma implantados. En conjunto, estos experimentos muestran que la señalización PKA/CREB es una palanca central que puede redirigir células de neuroblastoma de alto riesgo hacia un estado más maduro y menos peligroso.
Cómo MYCN y un microARN bloquean el circuito de diferenciación
El estudio examinó luego cómo MYCN apaga esta vía beneficiosa. Cuando se redujeron los niveles de MYCN en células amplificadas, aumentaron las proteínas PKA y CREB, y NT‑3 volvió a promover la diferenciación en lugar del crecimiento. El análisis de datos de tumores de pacientes reveló que los genes que codifican componentes de PKA se expresan a niveles más bajos en tumores con amplificación de MYCN que en otros casos, lo que sugiere que MYCN amortigua en general esta vía en niños con enfermedad de alto riesgo. Los autores también identificaron un papel para un pequeño ARN regulador, miR‑221, que se asocia fuertemente con MYCN y con peores desenlaces. Los niveles altos de miR‑221 se correlacionaron con la expresión de MYCN tanto en tumores como en líneas celulares. Cuando se bloqueó miR‑221 en células con amplificación de MYCN, aumentaron los niveles de CREB y NT‑3 pudo de nuevo impulsar la maduración neuronal. Esto indica que MYCN suprime el circuito PKA/CREB tanto al reducir genes clave como al elevar miR‑221, que a su vez disminuye aún más CREB.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo dibuja una imagen clara: en el neuroblastoma de bajo riesgo, NT‑3 actuando a través de TrkC y una vía PKA/CREB activa ayuda a que las células tumorales inmaduras maduren hacia células benignas similares a neuronas. En tumores de alto riesgo con exceso de MYCN, esta ruta de maduración está bloqueada y la misma señal se reconduce para alimentar el crecimiento incontrolado, en parte facilitado por el microARN miR‑221. Al restaurar la actividad PKA/CREB —mediante fármacos que estimulen esta vía o atenuando los bloqueadores impulsados por MYCN— los clínicos podrían algún día convertir neuroblastomas agresivos en tumores más diferenciados y tratables. Esta estrategia encaja con un objetivo terapéutico más amplio en el cáncer infantil: no solo matar células cancerosas, sino empujarlas de nuevo hacia una trayectoria de desarrollo normal.
Cita: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Palabras clave: neuroblastoma, MYCN, TrkC, vía PKA CREB, diferenciación tumoral