Clear Sky Science · it
MYCN inibisce la differenziazione mediata da TrkC nelle cellule di neuroblastoma tramite l’interruzione della via di segnalazione PKA
Perché questo studio sul cancro infantile è importante
Il neuroblastoma è un tumore dell’infanzia che può comportarsi in modi molto diversi: alcuni tumori maturano silenziosamente e si riducono, mentre altri si diffondono in modo aggressivo e resistono alle terapie. Questo studio pone una domanda all’apparenza semplice ma dalle grandi implicazioni cliniche: perché certi segnali spingono alcune cellule di neuroblastoma a maturare in cellule nervose innocue, mentre in altre gli stessi segnali inducono proliferazione cancerosa? Scoprendo come un potente oncogene chiamato MYCN blocca un segnale naturale di maturazione, gli autori rivelano una possibile nuova strategia per spingere i tumori ad alto rischio verso uno stato più sicuro e trattabile.
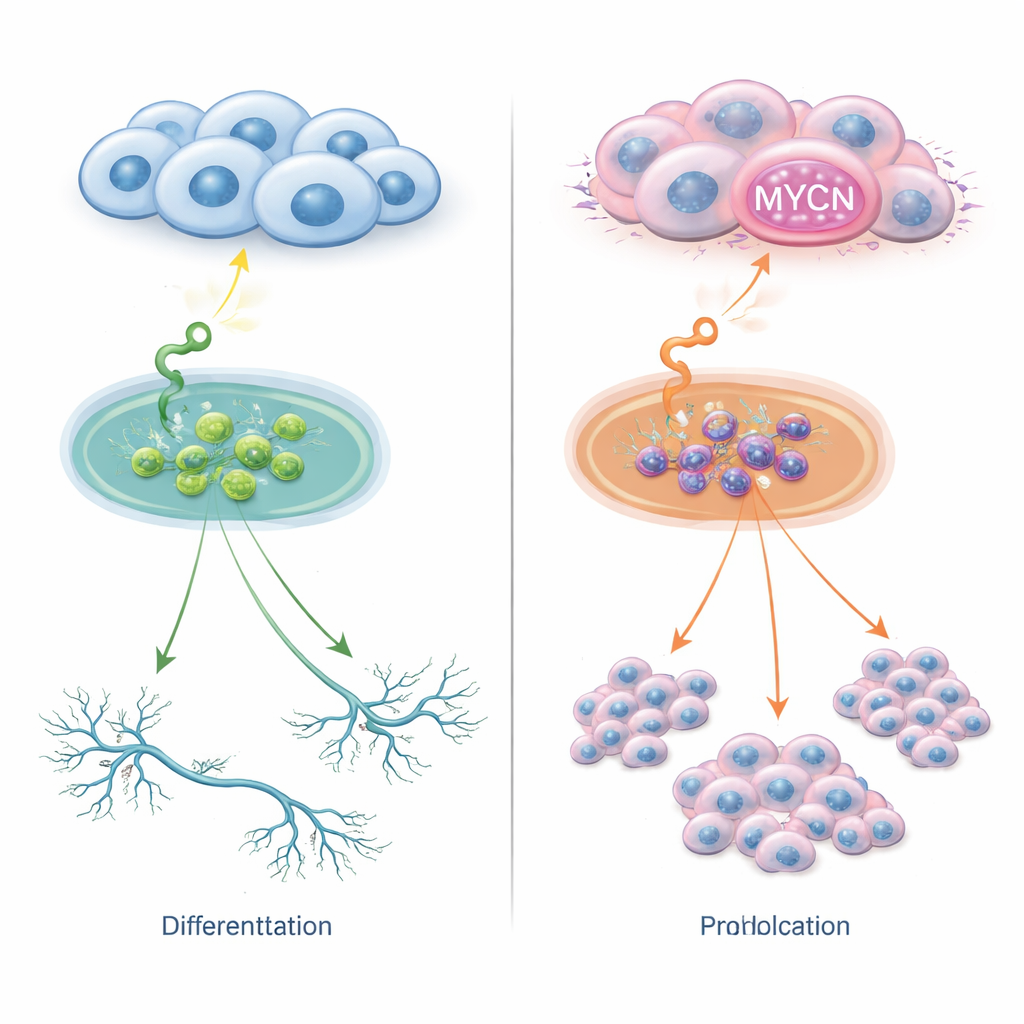
Due percorsi per lo stesso segnale
Le cellule di neuroblastoma hanno recettori sulla loro superficie che rilevano fattori di crescita nell’ambiente. Uno di questi recettori, chiamato TrkC, riconosce una molecola denominata NT‑3. In condizioni normali questa coppia può favorire lo sviluppo delle cellule nervose immature verso forme più mature. I ricercatori hanno ingegnerizzato varie linee cellulari di neuroblastoma per esprimere TrkC e poi le hanno stimolate con NT‑3. Nelle cellule senza copie aggiuntive del gene MYCN, NT‑3 ha spinto le cellule ad estendere lunghi prolungamenti simili a neuriti e ad assumere un aspetto più maturo, con pochi cambiamenti nel numero di cellule. In netto contrasto, nelle cellule con eccesso di MYCN—sia per sovraespressione sia per amplificazione genica completa—lo stesso segnale NT‑3 non ha più indotto la maturazione ma ha invece alimentato una rapida divisione cellulare. Così, un singolo segnale esterno può portare o alla differenziazione o a una crescita aggressiva, a seconda della quantità di MYCN presente nelle cellule.
Seguire le tracce della segnalazione all’interno della cellula
Per capire come si genera questa biforcazione comportamentale, il gruppo ha mappato gli interruttori chimici di “on/off” nelle cellule nel tempo usando una tecnica chiamata fosfoproteomica. Hanno confrontato migliaia di proteine modificate dopo la stimolazione con NT‑3 nelle diverse linee cellulari. Le cellule senza amplificazione di MYCN hanno mostrato un pattern di attivazione forte e distintivo, mentre le cellule ricche di MYCN hanno avuto una risposta più attenuata. Quando gli autori si sono concentrati su quali enzimi di segnalazione erano più attivi, è emerso un protagonista ricorrente nelle cellule in differenziazione: la via della proteina chinasi A (PKA) e il suo partner CREB, un regolatore nucleare che attiva geni necessari per la maturazione. L’analisi delle vie di segnalazione ha confermato che i processi legati allo sviluppo nervoso e al rimodellamento strutturale—come la guida degli assoni e i cambiamenti del citoscheletro—erano arricchiti specificamente quando l’attività PKA/CREB aumentava.
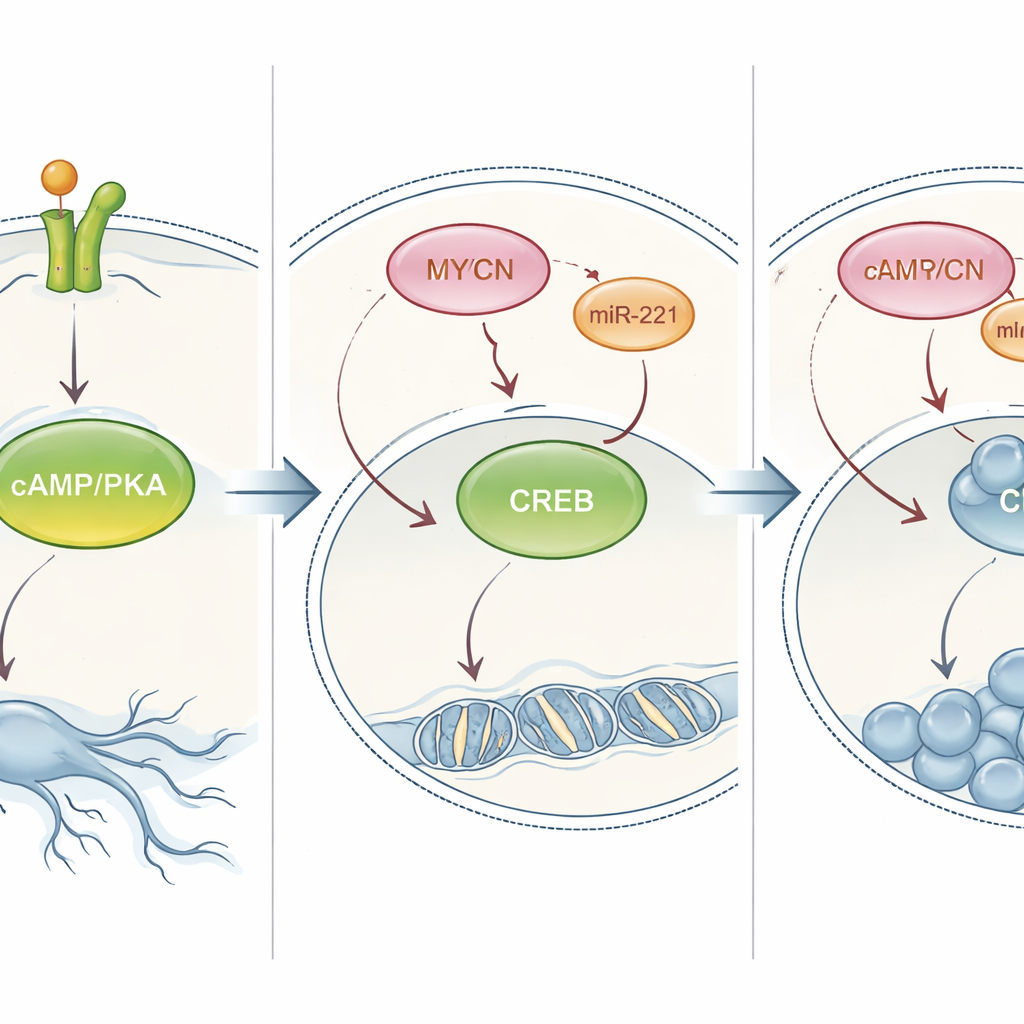
Invertire l’interruttore PKA per modificare il comportamento tumorale
I ricercatori hanno quindi testato se questa via PKA controlla davvero la scelta della cellula tra maturazione e proliferazione. Nelle cellule che normalmente si differenziavano in risposta a NT‑3, il blocco chimico della PKA ha ridotto l’emergere di prolungamenti nervosi e aumentato il numero di cellule. Nelle cellule con amplificazione di MYCN che solitamente proliferano, l’attivazione artificiale della PKA—sia con un farmaco che imita un messaggero naturale sia costringendo le cellule a produrre forme sempre attive di PKA o CREB—ha invertito il comportamento: le cellule hanno rallentato la divisione e sviluppato lunghi processi simili a neuriti. Questo effetto si è osservato non solo in colture cellulari ma anche in un modello di pesce zebra, dove l’attivazione della PKA ha fatto regredire i tumori umani di neuroblastoma impiantati. Complessivamente, questi esperimenti dimostrano che la segnalazione PKA/CREB è una leva centrale capace di riportare le cellule di neuroblastoma ad alto rischio verso uno stato più maturo e meno pericoloso.
Come MYCN e un microRNA bloccano il circuito di differenziazione
Lo studio ha poi esaminato come MYCN spenga questa via benefica. Quando i livelli di MYCN sono stati ridotti nelle cellule amplificate, le proteine PKA e CREB sono aumentate e NT‑3 ha nuovamente promosso la differenziazione anziché la crescita. Le analisi dei dati provenienti da tumori di pazienti hanno rivelato che i geni che codificano componenti della PKA sono espressi a livelli più bassi nei tumori con amplificazione di MYCN rispetto ad altri casi, suggerendo che MYCN inibisce ampiamente questa via nei bambini con malattia ad alto rischio. Gli autori hanno inoltre individuato un ruolo per un piccolo RNA regolatorio, miR‑221, fortemente associato a MYCN e a prognosi sfavorevole. Alti livelli di miR‑221 correlavano con l’espressione di MYCN sia nei tumori sia nelle linee cellulari. Quando miR‑221 è stato bloccato nelle cellule con amplificazione di MYCN, i livelli di CREB sono aumentati e NT‑3 ha potuto nuovamente stimolare la maturazione neuronale. Ciò indica che MYCN sopprime il circuito PKA/CREB sia reprimendo geni chiave sia aumentando miR‑221, che a sua volta riduce ulteriormente CREB.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro dipinge un quadro chiaro: nel neuroblastoma a basso rischio, NT‑3 che agisce tramite TrkC e una via PKA/CREB attiva aiuta le cellule tumorali immature a maturare in cellule benigne simili a neuroni. Nei tumori ad alto rischio con eccesso di MYCN, questa via di maturazione è bloccata e lo stesso segnale viene reindirizzato a sostenere la crescita incontrollata, favorita in parte dal microRNA miR‑221. Ripristinando l’attività PKA/CREB—con farmaci che potenziano questa via o attenuando i fattori inibitori indotti da MYCN—i clinici potrebbero un giorno convertire neuroblastomi aggressivi in tumori più differenziati e trattabili. Questa strategia si inserisce in un obiettivo terapeutico più ampio nel cancro infantile: non solo eliminare le cellule tumorali, ma indurle a percorrere nuovamente una via di sviluppo normale.
Citazione: Maher, S., Roe, A., Wynne, K. et al. MYCN inhibits TrkC-mediated differentiation in neuroblastoma cells via disruption of the PKA signalling pathway. Cell Death Discov. 12, 176 (2026). https://doi.org/10.1038/s41420-026-03024-y
Parole chiave: neuroblastoma, MYCN, TrkC, via PKA CREB, differenziazione tumorale