Clear Sky Science · zh
血管疾病中平滑肌细胞的铁死亡:从基本原理到临床转化
血管细胞死亡为何关乎心脑健康
心肌梗死、中风、动脉瘤和高血压等疾病都有一个共同的舞台:血管。本文综述探讨了一种新识别的血管壁平滑肌细胞死亡方式——铁死亡,这种细胞死亡与铁代谢和脂质氧化密切相关。通过整理数十项近期研究,作者展示了这种死亡形式如何既削弱血管,又在某些情况下抑制有害的细胞过度增生。理解这一双刃效应或将为预防和治疗多种血管疾病开辟新途径。
铁驱动的细胞死亡如何发生
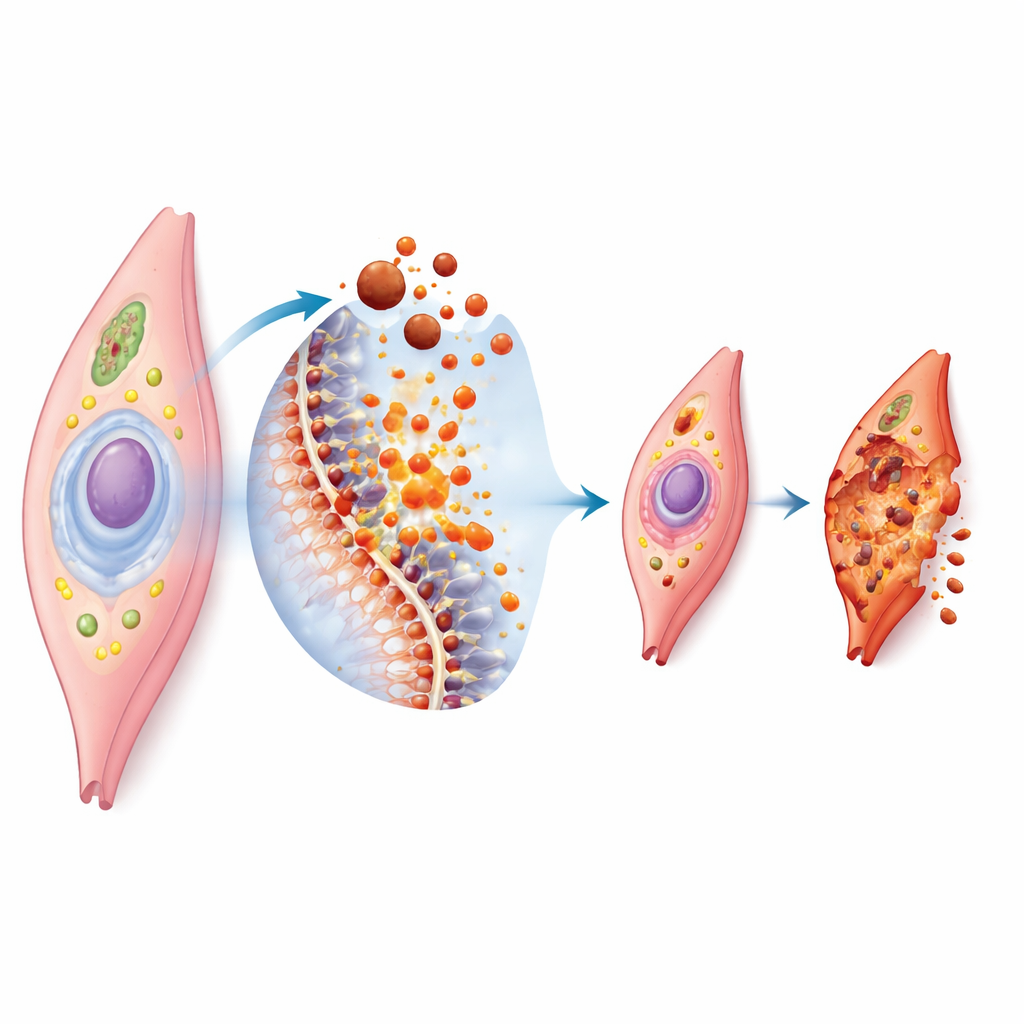
铁死亡是一种依赖铁和膜脂质过氧化的程序性细胞死亡。当细胞内铁过量时,会促进高活性分子的产生,攻击细胞膜的脂类成分。如果细胞自身的防御系统——如抗氧化酶和保护性小分子——被压倒,膜结构将受损,细胞崩解。在显微镜下,这类细胞可见能量工厂(线粒体)萎缩变形以及细胞膜破裂。由于血管平滑肌细胞富含特定脂类并长期承受机械和化学应激,当铁与氧化失衡时,它们尤其脆弱。
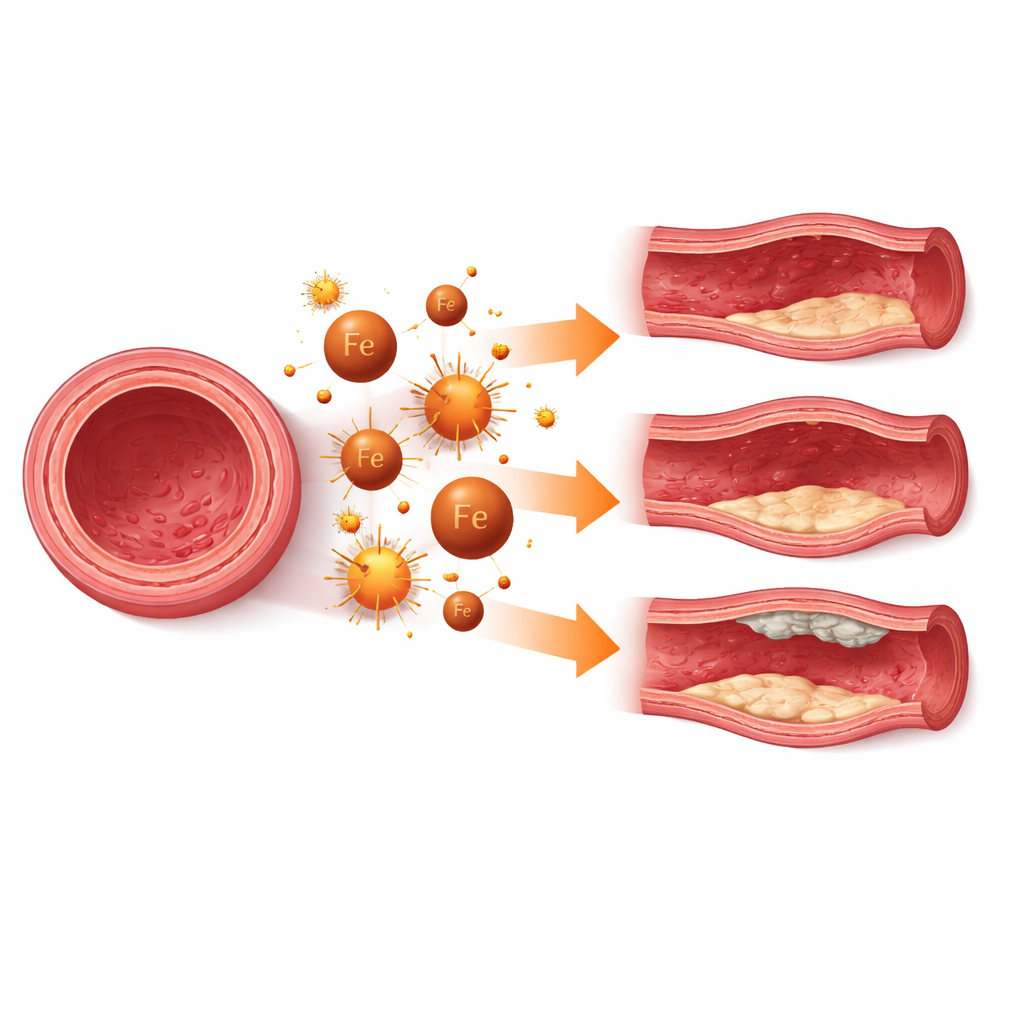
当细胞死亡削弱血管壁
在许多疾病中,血管平滑肌细胞的铁死亡像一把缓慢的破坏锤,损蚀血管壁。在被称为动脉瘤的动脉囊状膨出处,这些肌细胞的丧失使血管壁变薄、易于破裂。细胞、动物和人类组织研究均在动脉瘤区域发现铁堆积、脂质损伤和铁死亡标志。用实验性药物抑制铁死亡或增强天然防御可以减缓动脉瘤进展并维持细胞的收缩型状态。颅内动脉瘤也显示出相似模式,保护脑血管平滑肌细胞免受铁死亡可能有助于保持供脑细小动脉的强度。
铁、钙化斑块与血管硬化
铁死亡还影响动脉的老化与堵塞。在引发大多数心肌梗死和中风的动脉粥样硬化中,不稳定的斑块常含有死亡或濒死的平滑肌细胞、受损脂质和强烈的炎症活动。综述强调,平滑肌细胞的铁死亡可以使稳定斑块的纤维帽变薄,从而增加破裂风险。在慢性肾病和糖尿病常见的血管钙化中,铁驱动的脂质损伤促使平滑肌细胞向类骨表型转变并促进钙盐在血管壁沉积。在这两种情形中,减少铁过载、恢复抗氧化能力或直接抑制铁死亡的实验性治疗在动物模型中都能减轻钙化并增强斑块稳定性。
何时诱导细胞死亡有益
令人注目的是,同一过程在平滑肌细胞过度增生时反而有利。在支架置入后的新生内膜增生或肺动脉高压等病症中,这些细胞向高度增殖、合成型迁移,导致血管壁增厚和血流通道狭窄。这里的问题不是细胞丧失而是细胞过剩。综述描述了若干研究,表明在过度活跃的平滑肌细胞中温和促进铁死亡或恢复其对铁死亡的敏感性,可以抑制异常增生并限制瘢痕样组织堆积。相反,当铁死亡在这些疾病中过度被抑制时,血管会以更不利的方式重塑,恶化血流并推动血压升高。
多层调控与新兴疗法
文章强调,血管平滑肌细胞中的铁死亡受一个复杂调控网络支配。RNA的化学修饰、基因表达开关、蛋白质翻译后修饰,以及来自相邻免疫细胞和干细胞的信号,都会促使体系向或远离铁死亡倾斜。这些层次最终汇聚于三大核心功能:铁的摄入与储存、膜脂质的易氧化性以及抗氧化防御的强度。许多实验性疗法正针对这些调节杆,从小分子与天然化合物,到基于RNA的工具、工程化纳米颗粒以及将保护性货物递送至血管壁的外泌体。
对患者意味着什么
总体而言,综述得出结论:铁死亡是血管疾病中的一个核心但情境依赖的驱动因素。当其失控时,会破坏赋予血管强度和弹性的平滑肌细胞,助长动脉瘤、斑块不稳定和钙化;当其被过度抑制时,则助长细胞失控增殖和血管壁增厚,如某些形式的高血压和术后瘢痕化。未来医学的挑战在于判断何时抑制铁死亡、何时利用它,并以一种靶向正确细胞类型和疾病阶段的方式施行。如果能够实现这种平衡,针对这一与铁相关的细胞死亡通路的疗法或可成为维护血管健康、减轻心脑肺血管疾病负担的有力工具。
引用: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
关键词: 铁死亡, 血管平滑肌细胞, 动脉瘤, 动脉粥样硬化, 血管钙化