Clear Sky Science · de
Ferroptose glatter Muskelzellen bei Gefäßerkrankungen: von den Grundprinzipien zur klinischen Translation
Warum sterbende Gefäßzellen für Herz- und Hirngesundheit wichtig sind
Herzinfarkte, Schlaganfälle, Aneurysmen und Bluthochdruck haben alle eine gemeinsame Bühne: unsere Blutgefäße. Dieser Übersichtsartikel beleuchtet eine neu erkannte Form des Zelltods glatter Muskelzellen der Gefäßwand, die Ferroptose genannt wird und eng mit Eisen und Fettoxidation verknüpft ist. Anhand zahlreicher aktueller Studien zeigen die Autorinnen und Autoren, wie diese Art des Zelltods Gefäße schwächen, in manchen Fällen aber auch schädliches Zellwachstum eindämmen kann. Das Verständnis dieses zweischneidigen Prozesses könnte neue Wege eröffnen, eine breite Palette von Gefäßerkrankungen zu verhindern oder zu behandeln.
Wie eisengetriebener Zelltod funktioniert
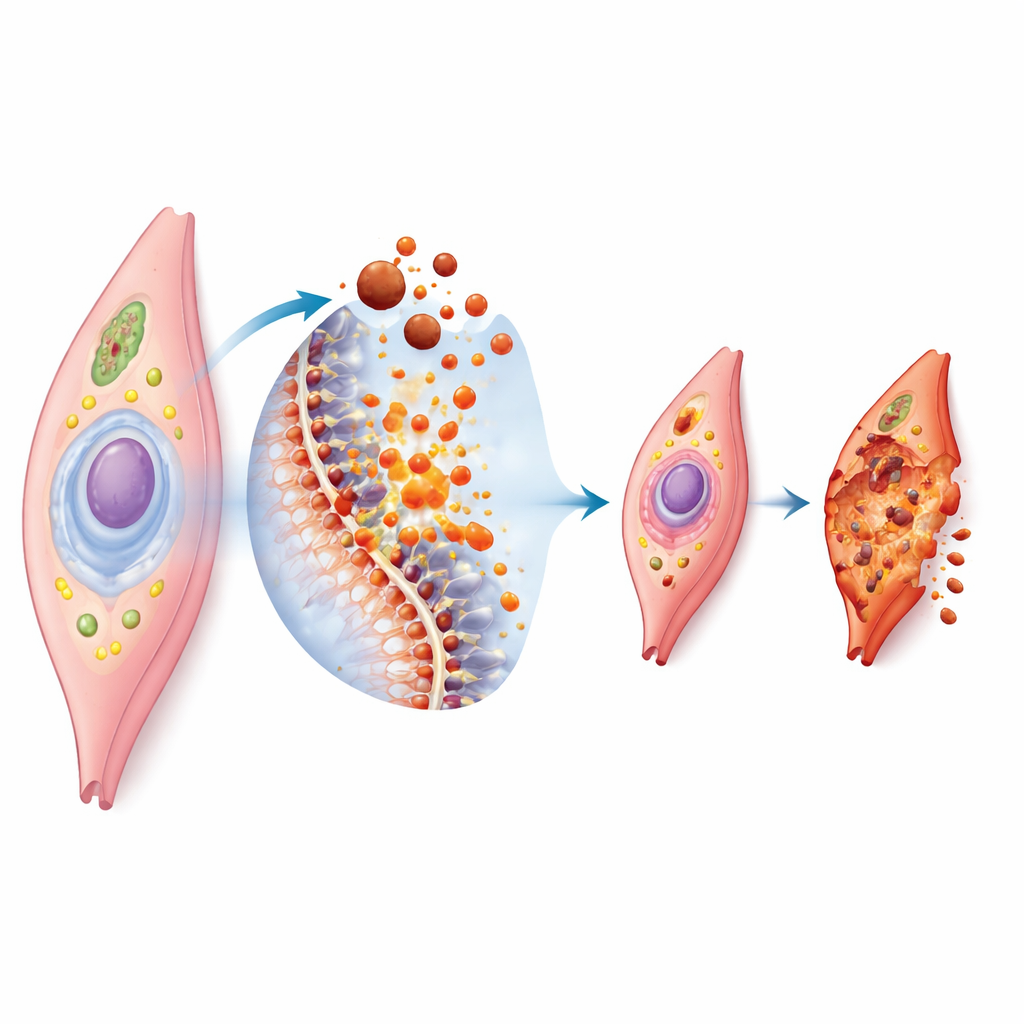
Ferroptose ist eine Form des kontrollierten Zelltods, die von Eisen und dem Abbau von Fetten in Zellmembranen abhängt. Wenn sich zu viel Eisen in einer Zelle ansammelt, fördert es die Bildung hochreaktiver Moleküle, die die fettigen Bestandteile der Zellhülle angreifen. Sind die körpereigenen Abwehrsysteme der Zelle, wie antioxidative Enzyme und schützende kleine Moleküle, überfordert, wird die Membran beschädigt und die Zelle bricht zusammen. Unter dem Mikroskop zeigen sich verkleinerte, deformierte „Energiefabriken“ und aufgerissene äußere Membranen. Da Gefäßmuskelzellen reich an bestimmten Fetten sind und ständig mechanischen sowie chemischen Stress aushalten müssen, sind sie besonders verwundbar, wenn Eisen und Oxidation aus dem Gleichgewicht geraten.
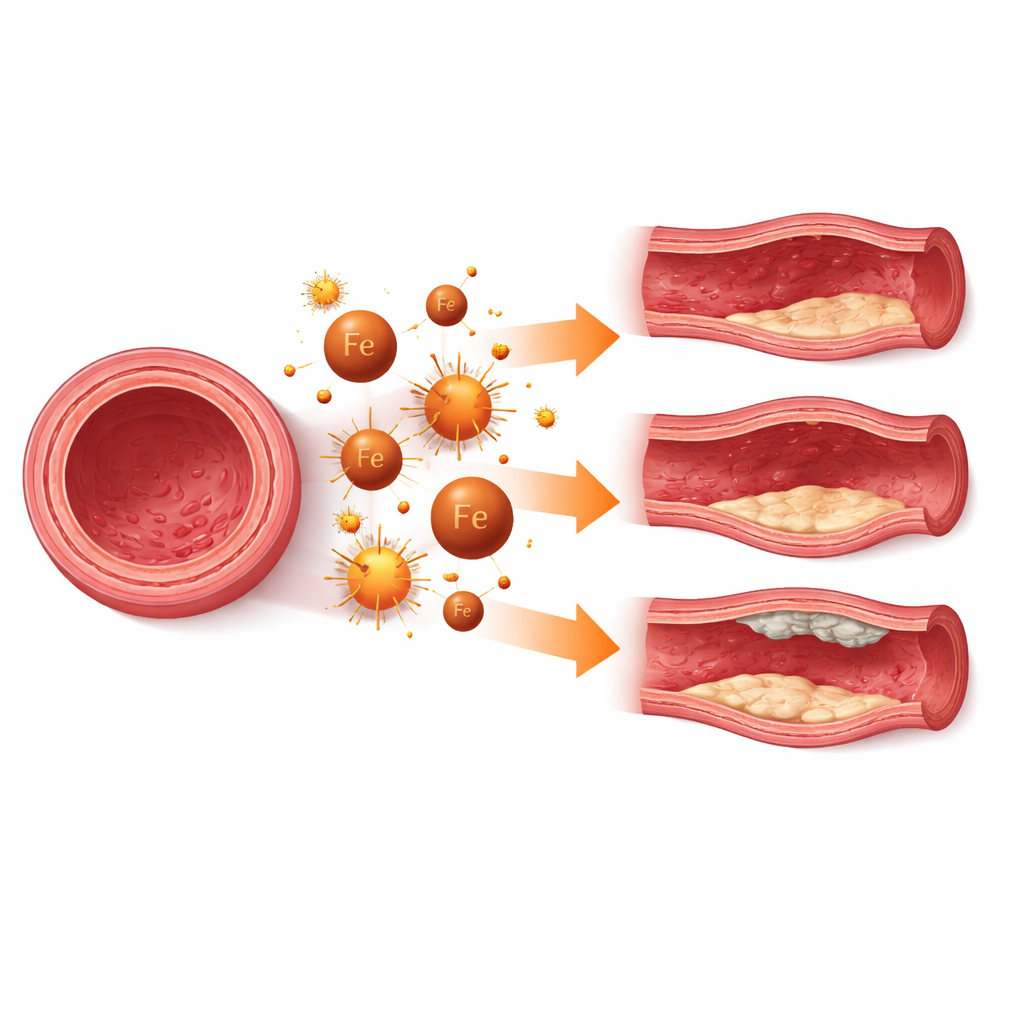
Wenn Zelltod die Gefäßwand schwächt
Bei vielen Erkrankungen wirkt Ferroptose in vaskulären glatten Muskelzellen wie ein langsamer Abrisskran an der Gefäßwand. Bei ballonartigen Aussackungen großer Arterien, den Aneurysmen, führt der Verlust dieser Muskelzellen zu einer Ausdünnung der Wand und erhöht so die Gefahr eines Risses. Zellkultur-, Tier- und humane Gewebestudien zeigen in Aneurysmenbereichen Hinweise auf Eisenansammlung, Fettverletzungen und Marker der Ferroptose. Das Blockieren der Ferroptose mit experimentellen Wirkstoffen oder das Stärken natürlicher Schutzmechanismen kann das Wachstum von Aneurysmen verlangsamen und den normalen, kontraktilen Zustand dieser Zellen erhalten. Ähnliche Muster finden sich bei intrakraniellen Aneurysmen, wo der Schutz der Hirngefäßmuskelzellen vor Ferroptose helfen könnte, die Stabilität empfindlicher Hirnarterien zu bewahren.
Eisen, alternde Plaques und verhärtete Arterien
Ferroptose prägt auch, wie Arterien altern und verstopfen. Bei der Atherosklerose, der häufigsten Ursache von Herzinfarkten und Schlaganfällen, enthalten instabile Plaques oft sterbende oder abgestorbene glatte Muskelzellen, beschädigte Fette und ausgeprägte Entzündungsreaktionen. Die Übersichtsarbeit hebt Studien hervor, die zeigen, dass Ferroptose dieser Zellen die fibröse Kappe, die einen Plaque stabilisiert, ausdünnen kann und damit das Rupturrisiko erhöht. Bei der Gefäßverkalkung, häufig bei chronischer Nierenerkrankung und Diabetes, fördert eisengetriebene Fettoxidation die Umwandlung von Muskelzellen in einen knochenähnlichen Zustand und begünstigt Kalziumablagerungen in der Gefäßwand. In beiden Fällen können experimentelle Behandlungen, die Eisenüberladung reduzieren, die antioxidative Kapazität wiederherstellen oder Ferroptose direkt hemmen, in Tiermodellen Verkalkung verringern und Plaques stärken.
Wenn das Auslösen von Zelltod nützlich ist
Bemerkenswerterweise kann derselbe Prozess hilfreich sein, wenn glatte Muskelzellen übermäßig wachsen. Bei Zuständen wie neointimaler Hyperplasie nach Stent-Implantation oder pulmonaler arterieller Hypertonie in der Lunge treten diese Zellen in einen hochproliferativen, synthetischen Zustand, der die Gefäßwand verdickt und den Blutfluss einengt. Hier besteht das Problem nicht im Zellverlust, sondern im Zellenüberschuss. Die Übersichtsarbeit beschreibt Studien, in denen eine gezielte Förderung der Ferroptose in überaktiven Muskelzellen oder die Wiederherstellung ihrer Empfindlichkeit gegenüber Ferroptose abnormales Wachstum dämpfen und die Bildung narbenähnlichen Gewebes begrenzen kann. Umgekehrt führt eine übermäßige Unterdrückung der Ferroptose in diesen Erkrankungen zu Gefäßumbau, der den Blutfluss verschlechtert und den Druck erhöht.
Regulationsebenen und aufkommende Therapien
Der Artikel betont, dass Ferroptose in Gefäßmuskelzellen durch ein dichtes Netzwerk von Kontrollmechanismen gesteuert wird. Chemische Markierungen auf RNA, Schalter in der Genaktivität, Feinabstimmungen von Proteinen nach deren Synthese sowie Signale benachbarter Immun- und Stammzellen verschieben das Gleichgewicht hin zu oder weg von Ferroptose. Diese Ebenen laufen auf drei Kernfunktionen hinaus: wie viel Eisen ein- und gespeichert wird, wie leicht Membranlipide oxidiert werden und wie stark die antioxidativen Abwehrsysteme bleiben. Viele experimentelle Therapien greifen inzwischen diese Hebel an — von Kleinstmolekülen und Naturstoffen über RNA-basierte Werkzeuge bis hin zu konstruierten Nanopartikeln und Exosomen, die schützende Ladung gezielt an die Gefäßwand bringen.
Was das für Patientinnen und Patienten bedeutet
Insgesamt kommt die Übersichtsarbeit zu dem Schluss, dass Ferroptose ein zentraler, aber kontextabhängiger Treiber vaskulärer Erkrankungen ist. Läuft sie unkontrolliert ab, zerstört sie die glatten Muskelzellen, die Gefäßen Kraft und Beweglichkeit verleihen, und trägt so zu Aneurysmen, Plaqueinstabilität und Verkalkung bei. Wird sie hingegen zu stark blockiert, ermöglicht das ungebremstes Zellwachstum und eine Verdickung der Gefäßwand, wie bei bestimmten Formen von Bluthochdruck und nach chirurgischen Eingriffen. Die Herausforderung der zukünftigen Medizin besteht darin zu lernen, wann Ferroptose gedämpft und wann sie genutzt werden sollte — und dies gezielt für die richtigen Zelltypen im passenden Krankheitsstadium. Gelingt dieses Gleichgewicht, könnten Therapien, die auf diesen eisenverknüpften Zelltodweg abzielen, mächtige Werkzeuge werden, um die Gefäßgesundheit zu erhalten und die Belastung durch Herz-, Hirn- und Lungengefäßerkrankungen zu reduzieren.
Zitation: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Schlüsselwörter: Ferroptose, gefäße glatte Muskelzellen, Aneurysma, Atherosklerose, Gefäßverkalkung