Clear Sky Science · es
Ferroptosis de las células musculares lisas en las enfermedades vasculares: desde los principios básicos hasta la traducción clínica
Por qué la muerte de las células de los vasos importa para la salud del corazón y el cerebro
Los infartos, los accidentes cerebrovasculares, los aneurismas y la hipertensión comparten un escenario común: nuestros vasos sanguíneos. Este artículo de revisión explora una forma recién reconocida de muerte celular en las células musculares de la pared vascular, llamada ferroptosis, estrechamente ligada al hierro y al daño lipídico. Al integrar docenas de estudios recientes, los autores muestran cómo este tipo de muerte celular puede tanto debilitar los vasos como, en algunos casos, ayudar a frenar el crecimiento celular nocivo. Comprender este proceso de doble filo podría abrir nuevos caminos para prevenir o tratar un amplio espectro de enfermedades vasculares.
Cómo funciona la muerte celular impulsada por el hierro
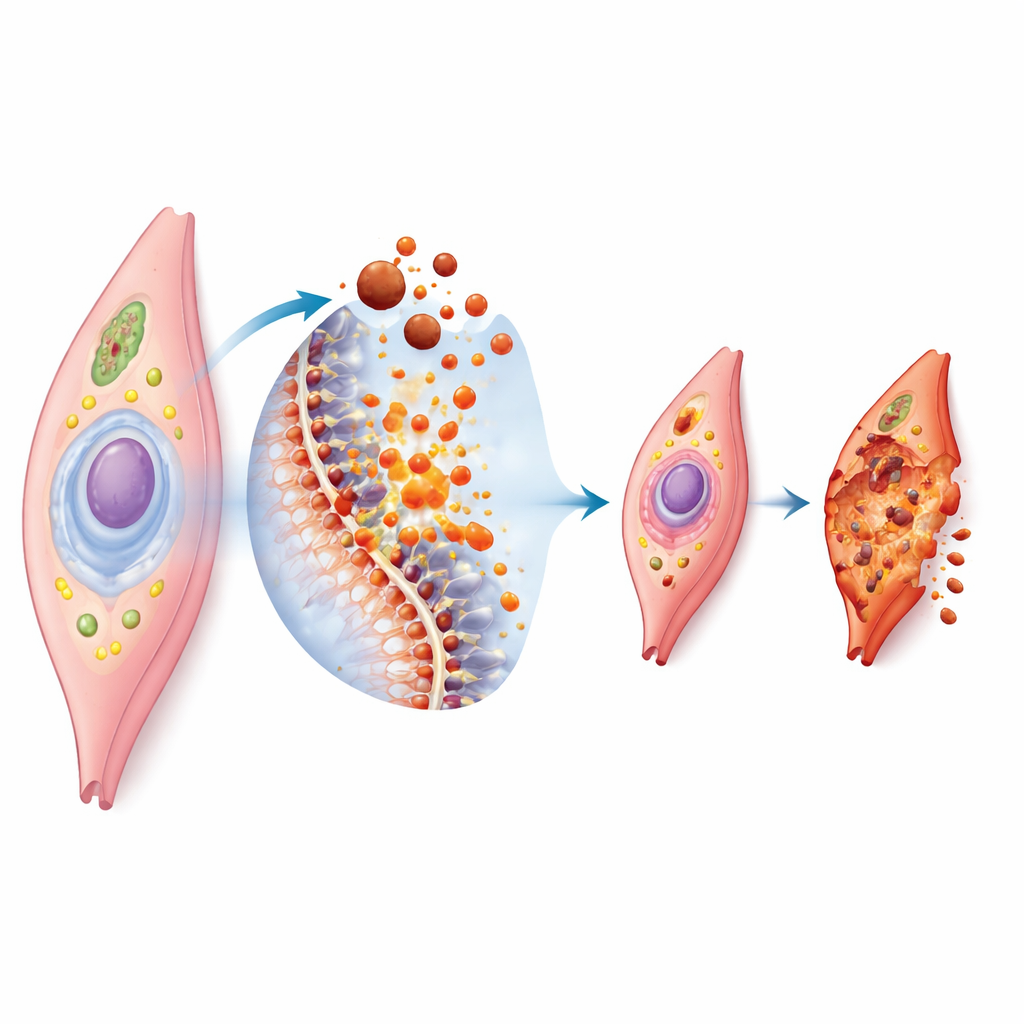
La ferroptosis es una forma de muerte celular regulada que depende del hierro y de la peroxidación de los lípidos de las membranas. Cuando se acumula demasiado hierro dentro de una célula, favorece la generación de moléculas altamente reactivas que atacan los componentes grasos de la envoltura celular. Si los sistemas de defensa de la célula, como enzimas antioxidantes y pequeñas moléculas protectoras, se ven desbordados, la membrana resulta dañada y la célula colapsa. Al microscopio, estas células muestran orgánulos energéticos reducidos y deformados y membranas externas rotas. Dado que las células musculares vasculares son ricas en ciertos lípidos y soportan de forma constante estrés mecánico y químico, son especialmente vulnerables cuando el equilibrio entre hierro y oxidación se altera.
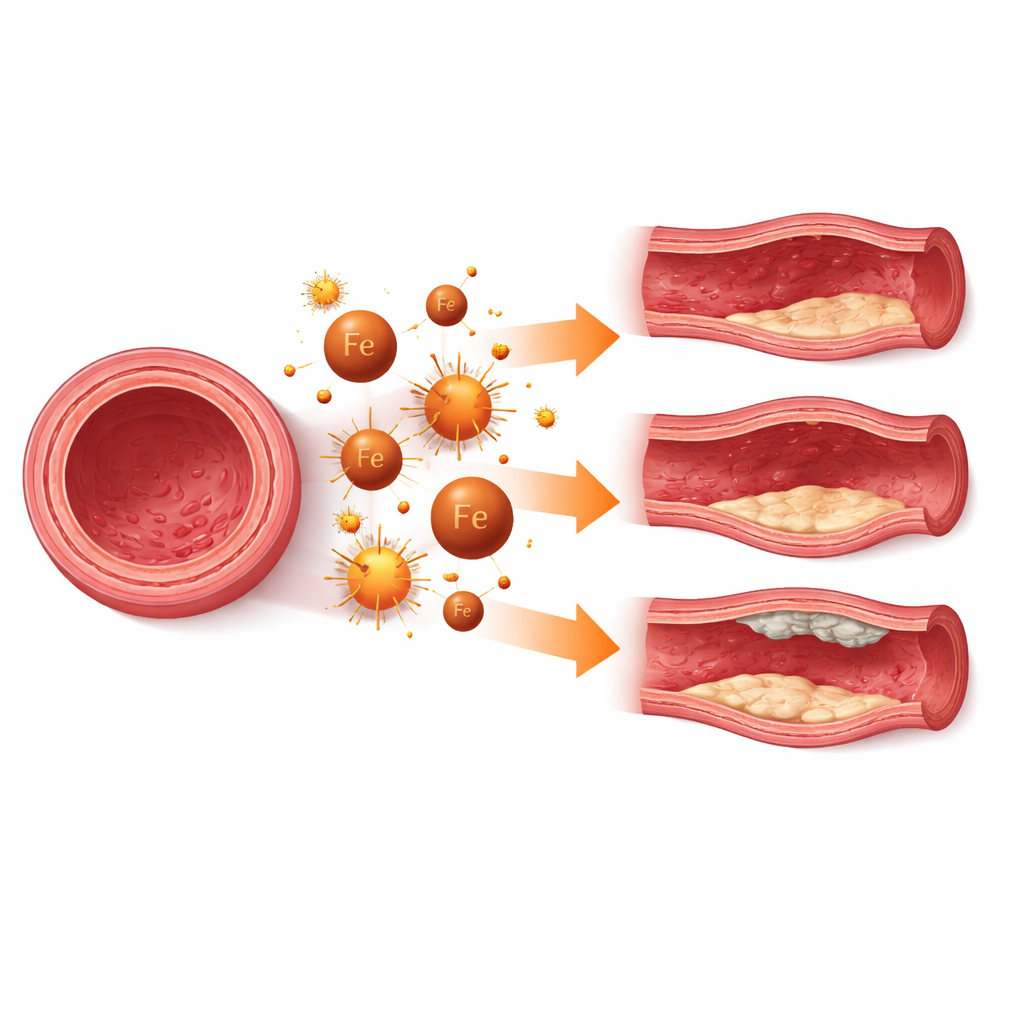
Cuando la muerte celular debilita la pared vascular
En muchas enfermedades, la ferroptosis en las células musculares lisas vasculares actúa como una demolición paulatina de la pared del vaso. En las dilataciones en forma de balón de las arterias principales, conocidas como aneurismas, la pérdida de estas células musculares adelgaza la pared y facilita su rotura. Estudios en células, animales y tejido humano muestran signos de acumulación de hierro, daño lipídico y marcadores de ferroptosis en las regiones aneurismáticas. Bloquear la ferroptosis con fármacos experimentales o reforzando las defensas naturales puede frenar el crecimiento del aneurisma y preservar el estado contráctil normal de estas células. Patrones similares aparecen en aneurismas intracraneales, donde proteger a las células musculares de los vasos cerebrales frente a la ferroptosis puede ayudar a mantener la resistencia de las arterias delicadas que irrigan el cerebro.
Hierro, placas envejecidas y endurecimiento arterial
La ferroptosis también condiciona cómo las arterias envejecen y se obstruyen. En la aterosclerosis, la enfermedad detrás de la mayoría de los infartos y los ictus, las placas inestables suelen contener células musculares lisas moribundas o muertas, lípidos dañados y una intensa actividad inflamatoria. La revisión destaca trabajos que muestran que la ferroptosis en estas células puede adelgazar la capa fibrosa que estabiliza la placa, haciéndola más propensa a romperse. En la calcificación vascular, común en la enfermedad renal crónica y la diabetes, el daño lipídico impulsado por el hierro empuja a las células musculares hacia un estado similar al óseo y fomenta los depósitos de calcio en la pared vascular. En ambos contextos, tratamientos experimentales que reducen la sobrecarga de hierro, restauran la capacidad antioxidante o inhiben directamente la ferroptosis pueden disminuir la calcificación y fortalecer las placas en modelos animales.
Cuando inducir la muerte celular resulta útil
De manera llamativa, el mismo proceso puede ser beneficioso cuando las células musculares lisas proliferan en exceso. En afecciones como la hiperplasia neointimal tras la colocación de stents, o la hipertensión arterial pulmonar en los pulmones, estas células pasan a un estado sintético y altamente proliferativo que engrosa la pared vascular y estrecha el paso de la sangre. Aquí, el problema no es la pérdida celular sino el exceso de células. La revisión describe estudios en los que promover moderadamente la ferroptosis en células musculares hiperactivas, o restaurar su sensibilidad a ella, puede frenar el crecimiento anormal y limitar la acumulación de tejido fibrótico. Por el contrario, cuando la ferroptosis está excesivamente suprimida en estas enfermedades, los vasos se remodelan de maneras que empeoran el flujo sanguíneo y aumentan la presión.
Capas de control y tratamientos emergentes
El artículo subraya que la ferroptosis en las células musculares vasculares está gobernada por una densa red de control. Marcas químicas en el ARN, cambios en la actividad génica, ajustes finos de las proteínas tras su síntesis y señales de células inmunes y progenitoras vecinas empujan el equilibrio hacia o lejos de la ferroptosis. Estas capas convergen en tres funciones centrales: cuánto hierro entra y se almacena, con qué facilidad se oxidan los lípidos de membrana y cuán robustas permanecen las defensas antioxidantes. Muchas terapias experimentales dirigen ahora estos puntos de palanca, desde pequeñas moléculas y compuestos naturales hasta herramientas basadas en ARN, nanopartículas diseñadas y exosomas que llevan carga protectora directamente a la pared vascular.
Qué significa esto para los pacientes
En conjunto, la revisión concluye que la ferroptosis es un motor central, aunque dependiente del contexto, de la enfermedad vascular. Cuando se descontrola, destruye las células musculares lisas que proporcionan fuerza y flexibilidad a los vasos, contribuyendo a aneurismas, inestabilidad de las placas y calcificación. Cuando está bloqueada en exceso, facilita el crecimiento celular desbocado y el engrosamiento de las paredes vasculares, como en ciertas formas de hipertensión y en la cicatrización postoperatoria. El reto para la medicina futura es aprender cuándo atenuar la ferroptosis y cuándo aprovecharla, y hacerlo de forma que se dirija a los tipos celulares adecuados en la fase correcta de la enfermedad. Si se logra ese equilibrio, las terapias que apunten a esta vía de muerte celular ligada al hierro podrían convertirse en herramientas poderosas para preservar la salud vascular y reducir la carga de los trastornos vasculares del corazón, el cerebro y los pulmones.
Cita: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Palabras clave: ferroptosis, células musculares lisas vasculares, aneurisma, aterosclerosis, calcificación vascular