Clear Sky Science · ru
Ферроптоз гладкомышечных клеток сосудов при сосудистых заболеваниях: от основных принципов до клинической трансляции
Почему гибель клеток сосудов важна для здоровья сердца и мозга
Инфаркты, инсульты, аневризмы и повышенное артериальное давление — все они имеют общую арену: наши кровеносные сосуды. В этом обзоре рассматривается недавно признанный путь гибели мышечных клеток стенки сосудов, называемый ферроптозом, который тесно связан с железом и повреждением липидов. Проанализировав десятки недавних исследований, авторы показывают, как этот тип гибели клеток может как ослаблять сосуды, так и, в некоторых случаях, помогать сдерживать вредный избыточный рост клеток. Понимание этого двустороннего процесса может открыть новые пути для профилактики и лечения широкого круга сосудистых заболеваний.
Как работает управляемая гибель, зависящая от железа
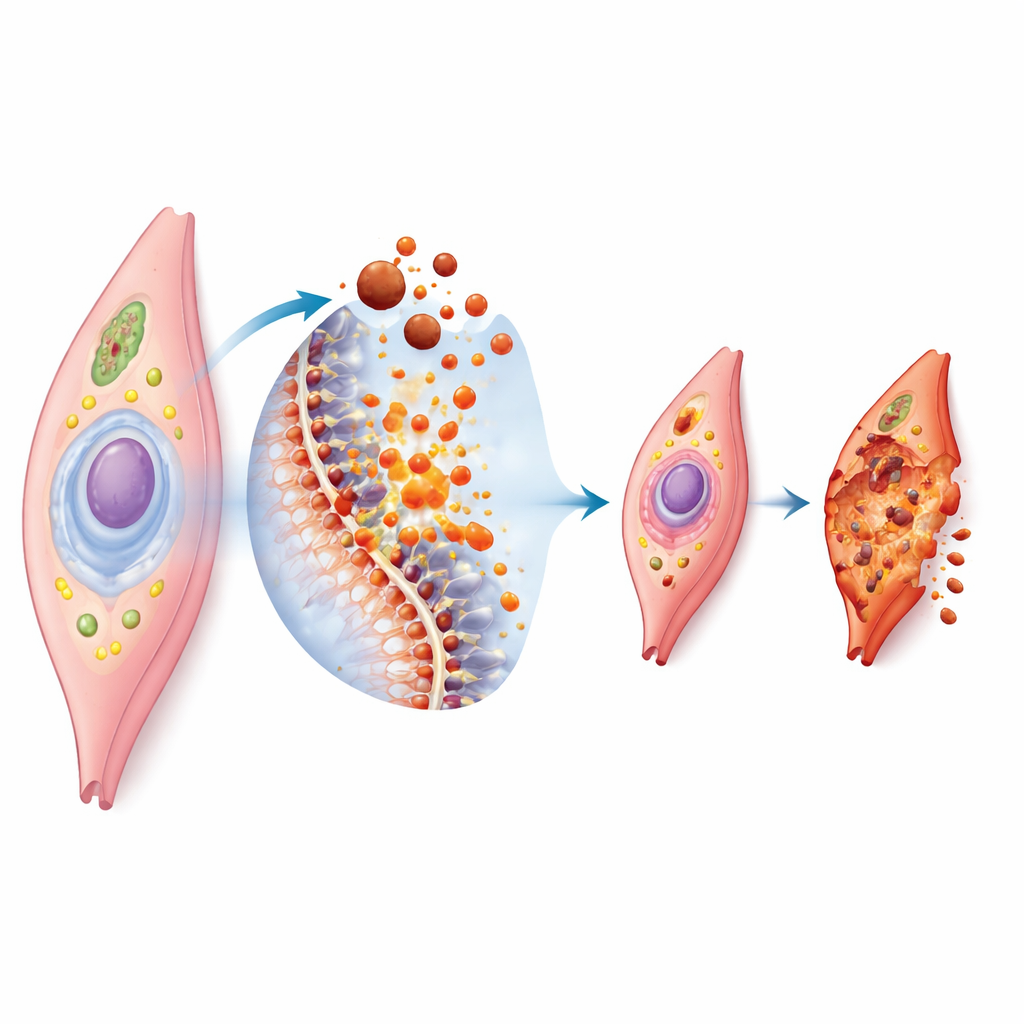
Ферроптоз — это форма регулируемой гибели клеток, зависящая от железа и пероксидации липидов в мембранах. Когда в клетке накапливается избыточное железо, оно способствует образованию высокореактивных молекул, атакующих жирные компоненты клеточной оболочки. Если собственные защитные системы клетки, такие как антиоксидантные ферменты и защитные малые молекулы, перегружаются, мембрана повреждается, и клетка разрушается. Под микроскопом такие клетки показывают уменьшенные, деформированные «энергетические фабрики» и разорванные наружные мембраны. Поскольку гладкомышечные клетки сосудов богаты определёнными липидами и постоянно испытывают механические и химические нагрузки, они особенно уязвимы при нарушении баланса железа и окисления.
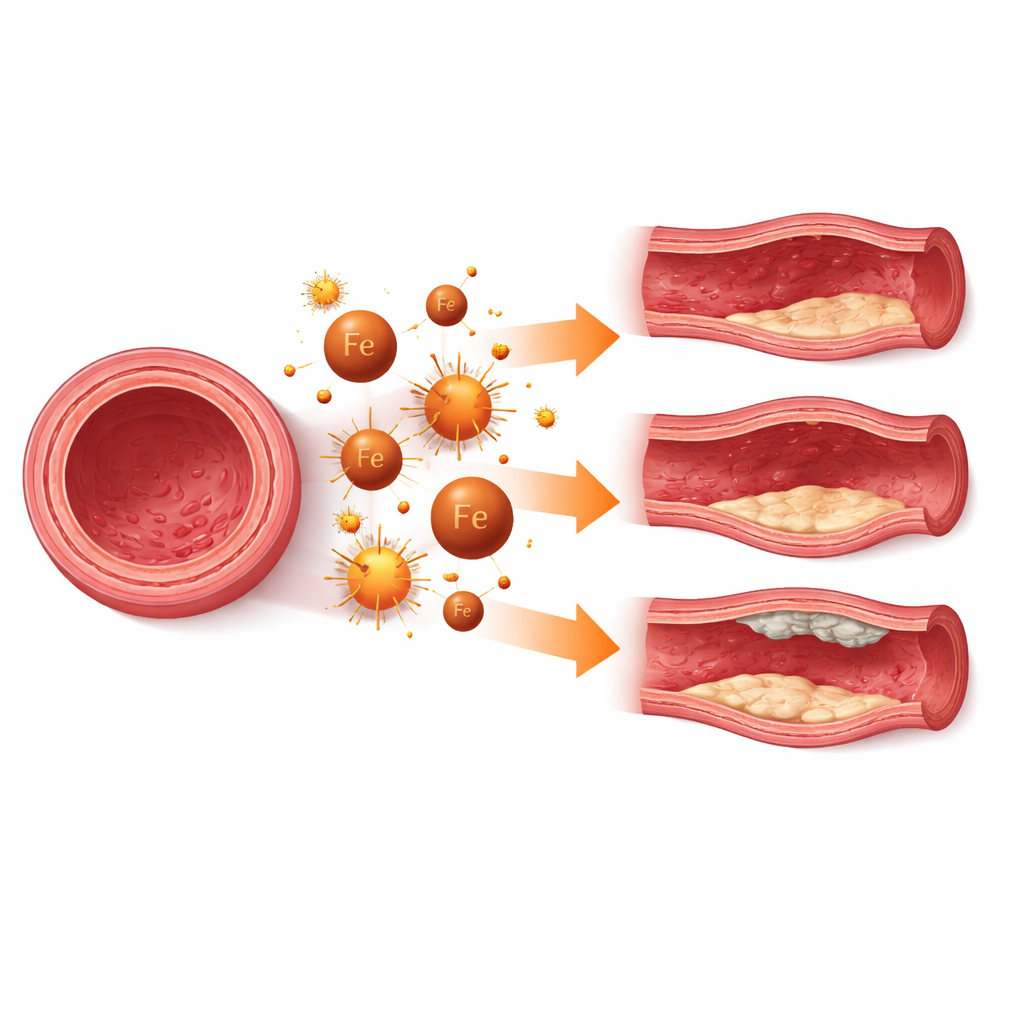
Когда гибель клеток ослабляет стенку сосуда
При многих заболеваниях ферроптоз в гладкомышечных клетках сосудов действует как медленный разрушительный фактор для стенки сосуда. При выпячиваниях крупных артерий, известных как аневризмы, потеря этих мышечных клеток истончает стенку и делает её более склонной к разрыву. Исследования in vitro, на животных моделях и в человеческих тканях показывают признаки накопления железа, повреждения липидов и маркеры ферроптоза в участках аневризм. Блокирование ферроптоза экспериментальными препаратами или усиление естественной защиты может замедлить рост аневризмы и сохранить нормальное, сократительное состояние этих клеток. Подобные закономерности наблюдаются при внутричерепных аневризмах, где защита мышечных клеток сосудов мозга от ферроптоза может помочь сохранить прочность тонких артерий, питающих мозг.
Железо, стареющие бляшки и окаменение артерий
Ферроптоз также влияет на старение и закупорку артерий. При атеросклерозе, болезни, лежащей в основе большинства инфарктов и инсультов, нестабильные бляшки часто содержат умирающие или погибшие гладкомышечные клетки, повреждённые липиды и выраженное воспаление. В обзоре подчёркиваются работы, показывающие, что ферроптоз в этих клетках может истончать фиброзную «шапку», стабилизирующую бляшку, делая её более склонной к разрыву. При сосудистой кальцификации, распространённой при хронической болезни почек и диабете, повреждение липидов под влиянием железа направляет гладкомышечные клетки в остеоподобное состояние и способствует отложению кальция в стенке сосуда. В обоих случаях экспериментальные вмешательства, уменьшающие перегрузку железом, восстанавливающие антиоксидантный потенциал или непосредственно ингибирующие ферроптоз, в моделях на животных снижают кальцификацию и укрепляют бляшки.
Когда запуск гибели клеток бывает полезен
Парадоксально, тот же процесс может быть полезен при избыточном росте гладкомышечных клеток. При таких состояниях, как неоинтимальная гиперплазия после установки стента или лёгочная артериальная гипертензия, эти клетки переходят в высокопролиферативное, синтетическое состояние, что утолщает стенки сосудов и сужает просвет для крови. Здесь проблема не в потере клеток, а в их избытке. В обзоре описаны исследования, где умеренное стимулирование ферроптоза в чрезмерно активных мышечных клетках или восстановление их чувствительности к нему способно сдерживать аномальный рост и ограничивать накопление рубцоподобной ткани. И напротив, чрезмерное подавление ферроптоза в этих заболеваниях приводит к ремоделированию сосудов, ухудшающему кровоток и повышающему давление.
Уровни регуляции и перспективные методы лечения
Статья подчёркивает, что ферроптоз в мышечных клетках сосудов находится под контролем сложной сети регуляции. Химические метки на РНК, переключатели активности генов, тонкая настройка белков после их синтеза и сигналы от соседних иммунных и стволовых клеток — всё это сдвигает баланс в сторону или против ферроптоза. Эти уровни сходятся в трёх ключевых функциях: сколько железа поступает и хранится, насколько легко окисляются мембранные липиды и насколько сильна антиоксидантная защита. Многие экспериментальные подходы нацелены на эти рычаги — от малых молекул и природных соединений до РНК-инструментов, модифицированных наночастиц и экзосом, доставляющих защитный груз прямо к стенке сосуда.
Что это означает для пациентов
В целом обзор делает вывод, что ферроптоз является центральным, но контекст-зависимым фактором сосудистых заболеваний. Когда он выходит из-под контроля, он уничтожает гладкомышечные клетки, дающие сосудам прочность и эластичность, способствуя развитию аневризм, нестабильности бляшек и кальцификации. Когда же ферроптоз слишком сильно подавлен, это позволяет неконтролируемому росту клеток и утолщению стенок сосудов, как при некоторых формах повышенного давления и послеопераческих рубцеваний. Задача будущей медицины — научиться, когда ослаблять ферроптоз, а когда его использовать, и делать это так, чтобы попадать в нужные типы клеток на нужной стадии болезни. Если удастся найти этот баланс, терапии, направленные на путь клеточной гибели, связанный с железом, могут стать мощным инструментом для сохранения здоровья сосудов и снижения бремени сердечно-сосудистых, цереброваскулярных и лёгочных сосудистых расстройств.
Цитирование: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Ключевые слова: ферроптоз, гладкомышечные клетки сосудов, аневризма, атеросклероз, васкулярная кальцификация