Clear Sky Science · fr
Ferroptose des cellules musculaires lisses dans les maladies vasculaires : des principes fondamentaux à la traduction clinique
Pourquoi la mort des cellules vasculaires compte pour la santé du cœur et du cerveau
Les infarctus, les AVC, les anévrismes et l’hypertension partagent une scène commune : nos vaisseaux sanguins. Cet article de synthèse explore une voie nouvellement reconnue de mort des cellules musculaires de la paroi vasculaire, appelée ferroptose, étroitement liée au fer et à l’oxydation des lipides. En rassemblant des dizaines d’études récentes, les auteurs montrent comment ce type de mort cellulaire peut à la fois fragiliser les vaisseaux et, dans certains cas, freiner une prolifération cellulaire nuisible. Comprendre ce processus à double tranchant pourrait ouvrir de nouvelles pistes pour prévenir ou traiter un large éventail de maladies vasculaires.
Comment fonctionne la mort cellulaire pilotée par le fer
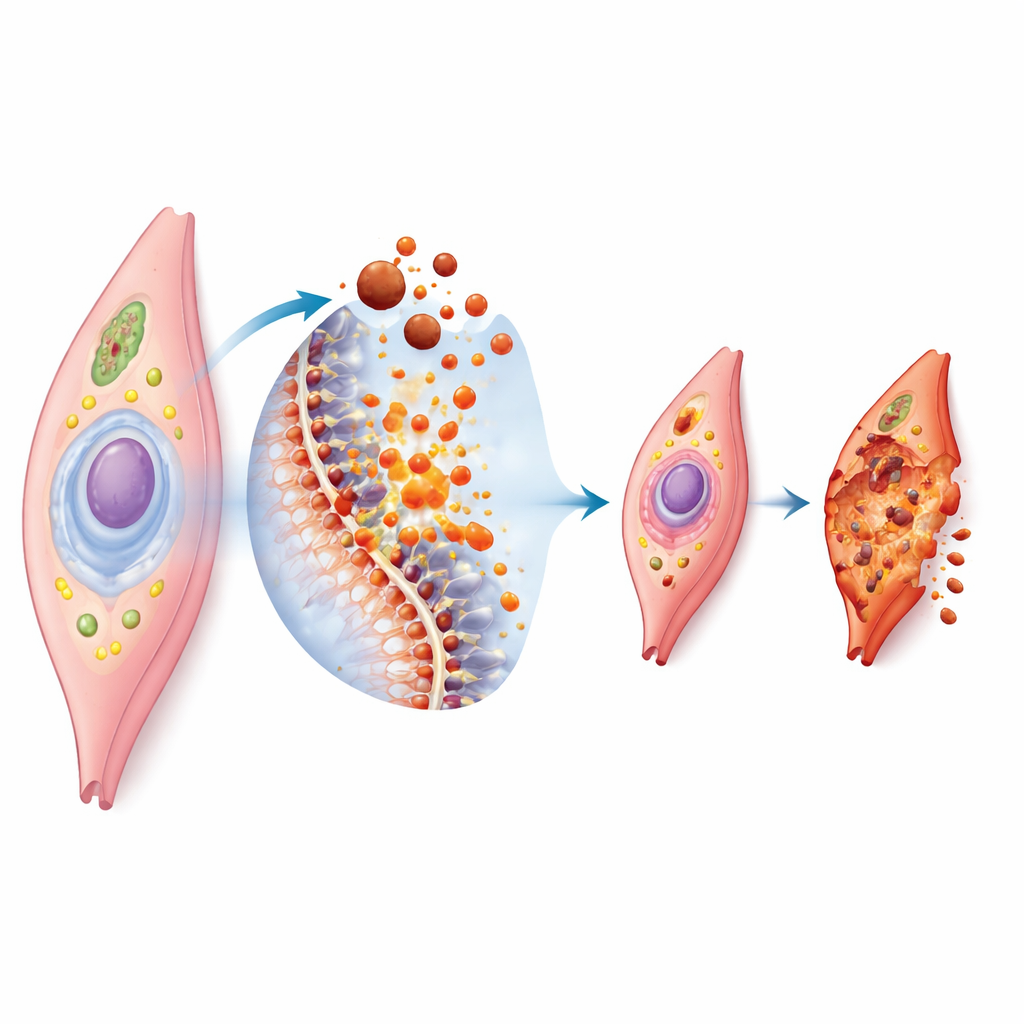
La ferroptose est une forme de mort cellulaire régulée qui dépend du fer et de la peroxydation des lipides membranaires. Quand un excès de fer s’accumule dans une cellule, il favorise la génération de molécules hautement réactives qui attaquent les composants lipidiques de l’enveloppe cellulaire. Si les systèmes de défense de la cellule, tels que les enzymes antioxydantes et les petites molécules protectrices, sont dépassés, la membrane est endommagée et la cellule s’effondre. Au microscope, ces cellules présentent des mitochondries rétrécies et déformées et des membranes externes rompues. Parce que les cellules musculaires vasculaires sont riches en certains lipides et subissent en permanence des contraintes mécaniques et chimiques, elles sont particulièrement vulnérables lorsque l’équilibre entre fer et oxydation est perturbé.
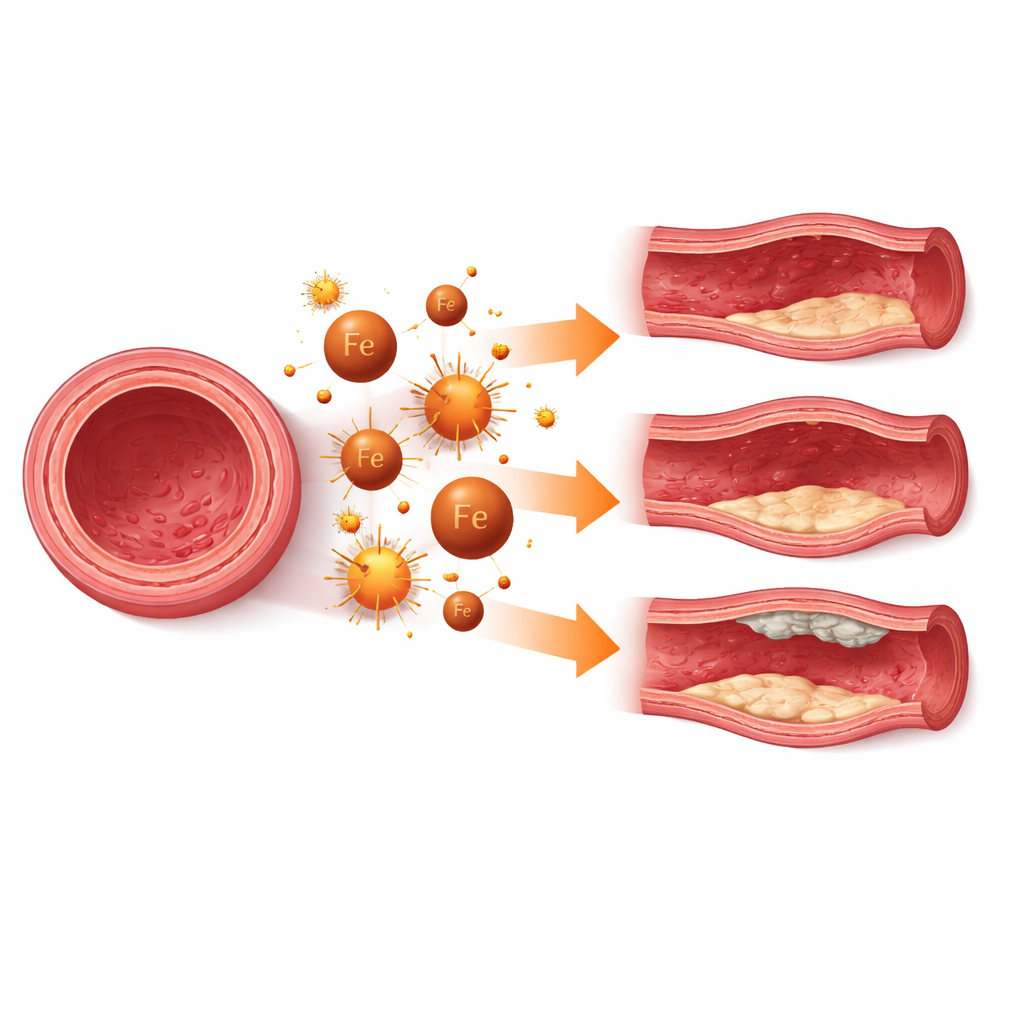
Quand la mort cellulaire affaiblit la paroi vasculaire
Dans de nombreuses maladies, la ferroptose des cellules musculaires lisses vasculaires agit comme un bourreau lent de la paroi vasculaire. Dans les renflements en forme de ballon des artères principales, appelés anévrismes, la perte de ces cellules rend la paroi plus mince et plus susceptible de se rompre. Des études in vitro, chez l’animal et sur des tissus humains montrent des signes d’accumulation de fer, de dommages lipidiques et de marqueurs de ferroptose dans les régions anévrismales. Bloquer la ferroptose avec des composés expérimentaux ou en renforçant les défenses naturelles peut ralentir la croissance des anévrismes et préserver l’état contractile normal de ces cellules. Des schémas similaires apparaissent dans les anévrismes intracrâniens : protéger les cellules musculaires des vaisseaux cérébraux de la ferroptose pourrait aider à maintenir la résistance des artères délicates qui irriguent le cerveau.
Fer, plaques vieillissantes et durcissement des artères
La ferroptose influence également le vieillissement et l’occlusion des artères. Dans l’athérosclérose, la maladie à l’origine de la plupart des infarctus et AVC, les plaques instables contiennent souvent des cellules musculaires lisses mourantes ou mortes, des lipides endommagés et une forte activité inflammatoire. La revue souligne des travaux montrant que la ferroptose de ces cellules peut amincir le cap fibreux qui stabilise la plaque, la rendant plus susceptible de se rompre. Dans la calcification vasculaire, fréquente dans l’insuffisance rénale chronique et le diabète, les dommages lipidiques liés au fer poussent les cellules musculaires vers un phénotype ostéomimétique et favorisent les dépôts calciques dans la paroi. Dans les deux contextes, des traitements expérimentaux qui réduisent la surcharge en fer, restaurent la capacité antioxydante ou inhibent directement la ferroptose peuvent diminuer la calcification et renforcer les plaques dans des modèles animaux.
Quand déclencher la mort cellulaire est utile
Fait remarquable, le même processus peut être bénéfique lorsque les cellules musculaires lisses prolifèrent excessivement. Dans des affections comme l’hyperplasie néointimale après la pose d’un stent, ou l’hypertension artérielle pulmonaire, ces cellules basculent vers un état synthétique hautement prolifératif qui épaissit la paroi vasculaire et rétrécit le calibre des vaisseaux. Ici, le problème n’est pas la perte cellulaire mais l’excès de cellules. La revue décrit des études où promouvoir modérément la ferroptose dans des cellules musculaires hyperactives, ou restaurer leur sensibilité à celle-ci, peut freiner la croissance anormale et limiter l’accumulation de tissu cicatriciel. À l’inverse, lorsque la ferroptose est excessivement inhibée dans ces maladies, la remodelation vasculaire s’aggrave, détériorant le flux sanguin et augmentant la pression.
Couches de régulation et traitements émergents
L’article insiste sur le fait que la ferroptose dans les cellules musculaires vasculaires est gouvernée par un réseau de contrôle dense. Les marques chimiques sur les ARN, les commutateurs d’activité génique, le réglage post‑traductionnel des protéines et les signaux émis par les cellules immunitaires et souches voisines orientent tous l’équilibre vers ou contre la ferroptose. Ces couches convergent sur trois fonctions centrales : la quantité de fer qui entre et est stockée, la susceptibilité des lipides membranaires à l’oxydation et la solidité des défenses antioxydantes. De nombreuses approches expérimentales ciblent aujourd’hui ces leviers, allant de petites molécules et composés naturels à des outils basés sur l’ARN, des nanoparticules conçues et des exosomes apportant des charges protectrices directement à la paroi vasculaire.
Ce que cela signifie pour les patients
Globalement, la revue conclut que la ferroptose est un moteur central, mais dépendant du contexte, des maladies vasculaires. Lorsqu’elle est débridée, elle détruit les cellules musculaires lisses qui confèrent force et souplesse aux vaisseaux, contribuant aux anévrismes, à l’instabilité des plaques et à la calcification. Lorsqu’elle est trop fortement bloquée, elle permet une prolifération cellulaire incontrôlée et un épaississement de la paroi vasculaire, comme dans certaines formes d’hypertension et de fibrose post‑chirurgicale. Le défi pour la médecine future est d’apprendre quand atténuer la ferroptose et quand l’exploiter, et de le faire de façon ciblée sur les types cellulaires appropriés et au bon stade de la maladie. Si cet équilibre peut être atteint, des thérapies visant cette voie de mort cellulaire liée au fer pourraient devenir des outils puissants pour préserver la santé des vaisseaux sanguins et réduire le fardeau des maladies vasculaires du cœur, du cerveau et des poumons.
Citation: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Mots-clés: ferroptose, cellules musculaires lisses vasculaires, anévrisme, athérosclérose, calcification vasculaire