Clear Sky Science · ar
التحلل الحديدي لخلايا العضلات الملساء في الأمراض الوعائية: من المبادئ الأساسية إلى الترجمة السريرية
لماذا تهم وفاة خلايا الأوعية لصحة القلب والدماغ
النوبات القلبية والسكتات وتمدد الأوعية وارتفاع ضغط الدم تشترك جميعها في مسرح واحد: أوعيتنا الدموية. تستعرض هذه المقالة طريقة جديدة معروفة لموت خلايا العضلات في جدران الأوعية تُعرف بالتحلل الحديدي، وهي مرتبطة بشكل وثيق بالحديد وتلف الدهون. من خلال تجميع عدة دراسات حديثة، يبيّن المؤلفون كيف يمكن لهذا النوع من موت الخلايا أن يضعف الأوعية الدموية وفي بعض الحالات يساعد في كبح فرط نمو الخلايا الضار. فهم هذه الظاهرة ذات الحدين قد يفتح طرقاً جديدة للوقاية أو علاج مجموعة واسعة من الأمراض الوعائية.
كيف يعمل موت الخلايا المدفوع بالحديد
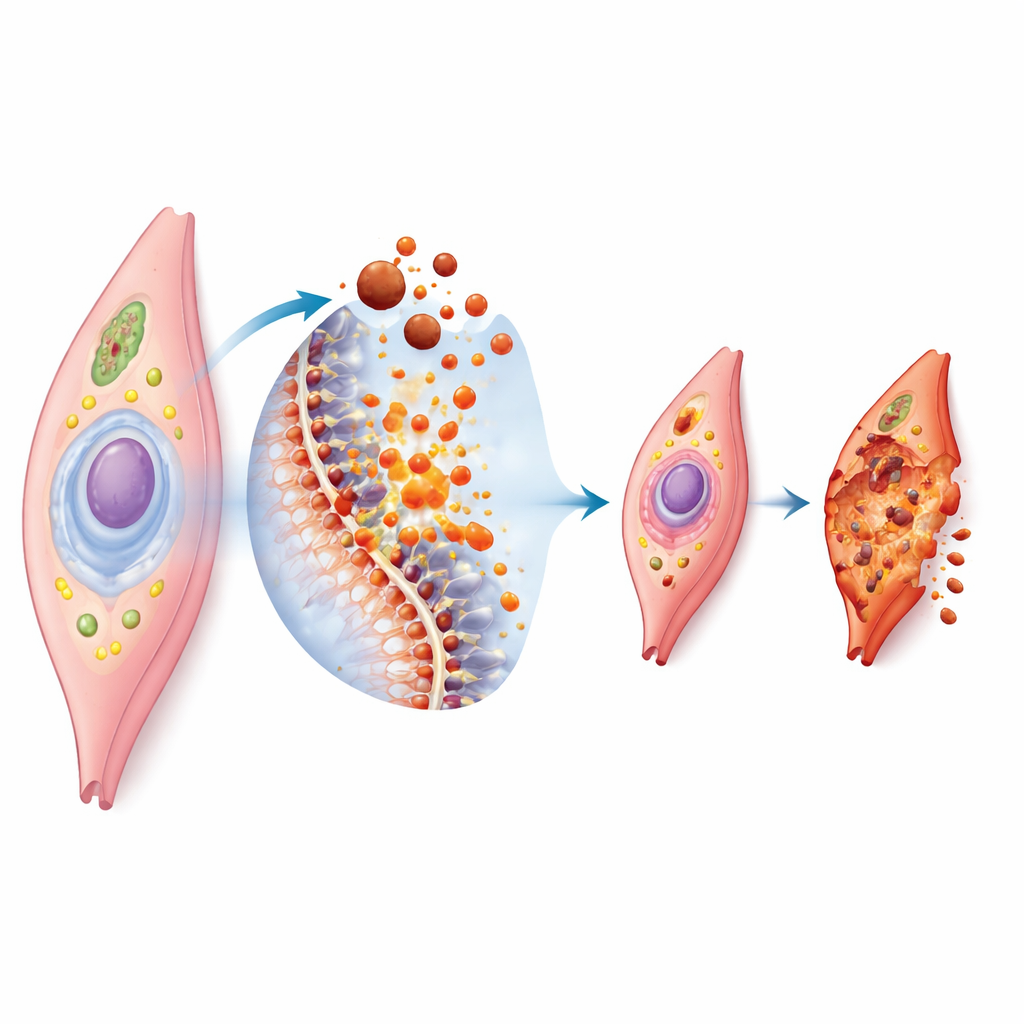
التحلل الحديدي هو شكل من أشكال موت الخلايا المبرمج يعتمد على الحديد وتكسير الدهون في أغشية الخلايا. عندما يتراكم الحديد داخل الخلية بشكل مفرط، يساهم في توليد جزيئات شديدة التفاعل تهاجم المكونات الدهنية في الغشاء الخارجي للخلية. إذا انهارت أنظمة الدفاع الخلوية مثل الإنزيمات المضادة للأكسدة والجزيئات الواقية الصغيرة، يتلف الغشاء وتنهار الخلية. تحت الميكروسكوب تبدو هذه الخلايا مع تقزم وتشوه في مصانع الطاقة وتهتك الأغشية الخارجية. ونظراً لأن خلايا العضلات في الأوعية غنية بأنواع معينة من الدهون وتتعرض باستمرار لإجهاد ميكانيكي وكيميائي، فهي عرضة بشكل خاص عندما يختل توازن الحديد والأكسدة.
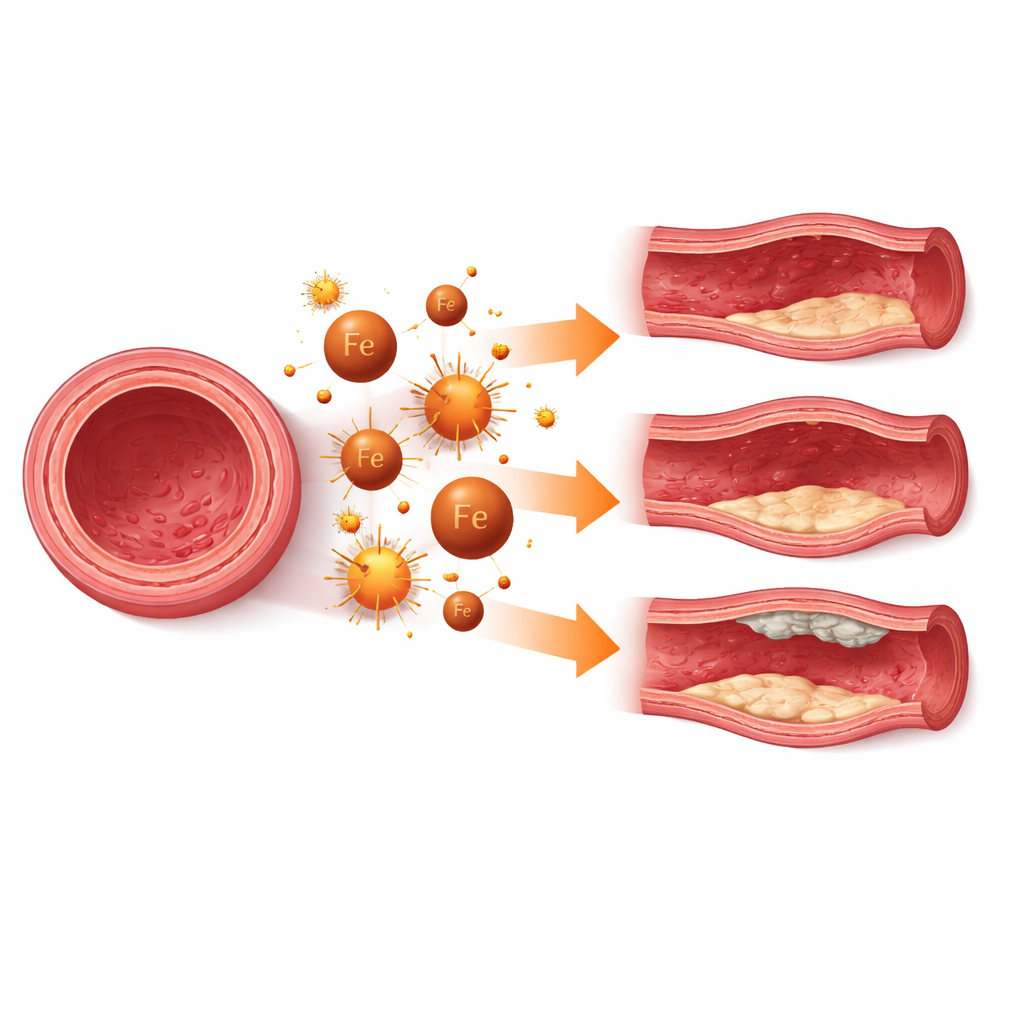
عندما يضعف موت الخلايا جدار الوعاء
في العديد من الأمراض، يعمل التحلل الحديدي في خلايا العضلات الملساء الوعائية ككرة هدم بطيئة لجدار الوعاء. في البروزات الشبه البالونية للشرايين الكبرى والمعروفة بالتمدد الوعائي، يؤدي فقدان هذه الخلايا إلى ترقق الجدار وزيادة احتمالية التمزق. تُظهر دراسات خلوية وحيوانية ونسيج بشري علامات تراكم الحديد، وتلف الدهون، ومؤشرات التحلل الحديدي في مناطق التمدد. إيقاف التحلل الحديدي بأدوية تجريبية أو عن طريق تعزيز الدفاعات الطبيعية يمكن أن يبطئ نمو التمدد ويحافظ على الحالة الانقباضية الطبيعية لهذه الخلايا. تظهر أنماط مماثلة في التمددات داخل الجمجمة، حيث قد يساعد حماية خلايا العضلات الوعائية في الدماغ من التحلل الحديدي في الحفاظ على قوة الشرايين الرقيقة الموردة للدماغ.
الحديد واللويحات المتقدمة وتصلب الشرايين
يشكل التحلل الحديدي أيضاً كيفية شيخوخة وانسداد الشرايين. في تصلب الشرايين، المرض الذي يقف وراء معظم النوبات القلبية والسكتات، غالباً ما تحتوي اللويحات غير المستقرة على خلايا عضلات ملساء ميتة أو في طور الموت، ودهون تالفة، ونشاط التهابي عالي. تسلط المراجعة الضوء على أعمال تُظهر أن التحلل الحديدي في هذه الخلايا يمكن أن يرشح الغطاء الليفي الذي يثبّت اللوحة، مما يجعلها أكثر عرضة للتمزق. في تكلس الأوعية، الشائع في مرضى الفشل الكلوي المزمن والسكري، يدفع تلف الدهون المعتمد على الحديد الخلايا العضلية نحو حالة تشبه العظام ويشجع ترسُّب الكالسيوم في جدار الوعاء. في كلتا الحالتين، يمكن للعلاجات التجريبية التي تقلل فرط التحميل بالحديد، أو تستعيد القدرة المضادة للأكسدة، أو تثبط التحلل الحديدي مباشرة أن تقلل التكلس وتقوّي اللويحات في نماذج حيوانية.
عندما يكون تحفيز موت الخلايا مفيداً
ومن اللافت أن نفس العملية قد تكون مفيدة عندما تنمو خلايا العضلات الملساء بشكل مفرط. في حالات مثل فرط تنسج النسيج الداخلي بعد وضع الدعامات، أو ارتفاع ضغط الشريان الرئوي في الرئتين، تتحول هذه الخلايا إلى حالة اصطناعية عالية التكاثر تضخم جدران الأوعية وتضيق مجرى الدم. هنا المشكلة ليست فقدان الخلايا بل فرطها. تصف المراجعة دراسات حيث أن تحفيز التحلل الحديدي بلطف في الخلايا العضلية المفرطة النشاط، أو استعادة حساسيتها له، يمكن أن يحد من النمو غير الطبيعي ويقلل تراكم النسيج الشبيهي بالندبة. وبالمقابل، عندما يُثبط التحلل الحديدي بشكل مفرط في هذه الأمراض، تعيد الأوعية تشكيل نفسها بطرق تفاقم تدفق الدم وتزيد الضغط.
طبقات الضبط والعلاجات الناشئة
تؤكد المقالة أن التحلل الحديدي في خلايا العضلات الوعائية تحكمه شبكة ضابطة معقدة. العلامات الكيميائية على الحمض النووي الريبوزي، مفاتيح نشاط الجينات، التعديلات اللاحقة للبروتينات، والإشارات من الخلايا المناعية وجذعية المجاورة كلها تدفع التوازن نحو أو بعيدا عن التحلل الحديدي. تتقاطع هذه الطبقات على ثلاث وظائف جوهرية: كمية الحديد الداخل والمخزن، سهولة أكسدة دهون الغشاء، وقوة الدفاعات المضادة للأكسدة. العديد من العلاجات التجريبية تستهدف الآن هذه الروافع، من جزيئات صغيرة ومركبات طبيعية إلى أدوات تعتمد على الحمض النووي الريبوزي، جسيمات نانوية مصممة، وإكسوسومات تحمل حمولة وقائية مباشرة إلى جدار الوعاء.
ماذا يعني هذا للمرضى
تستخلص المراجعة بشكل عام أن التحلل الحديدي هو عامل مركزي، ولكن معتمد على السياق، للأمراض الوعائية. عندما يخرج عن السيطرة، يدمر خلايا العضلات الملساء التي تمنح الأوعية قوتها ومرونتها، مساهمًا في التمدد الوعائي، وعدم استقرار اللويحات، والتكلس. وعندما يُثبط بقوة مفرطة، يتيح فرط نمو الخلايا وتثخن جدران الأوعية، كما في أشكال معينة من ارتفاع ضغط الدم والتندب بعد العمليات الجراحية. التحدي أمام الطب المستقبلي هو معرفة متى نخفف التحلل الحديدي ومتى نستخدمه، وأن يتم ذلك بحيث يستهدف الأنواع الخلوية الصحيحة وفي مرحلة المرض المناسبة. إذا أمكن تحقيق ذلك التوازن، فقد تصبح العلاجات الموجهة إلى مسار موت الخلايا المرتبط بالحديد أدوات فعالة لحفظ صحة الأوعية الدموية وتقليل عبء اضطرابات الأوعية القلبية والدماغية والرئوية.
الاستشهاد: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
الكلمات المفتاحية: التحلل الحديدي, خلايا العضلات الملساء الوعائية, تمدد الأوعية, تصلب الشرايين, تكلس الأوعية الدموية