Clear Sky Science · pl
Ferroptoza komórek mięśni gładkich naczyń w chorobach naczyniowych: od zasad podstawowych do translacji klinicznej
Dlaczego umierające komórki naczyniowe mają znaczenie dla zdrowia serca i mózgu
Zawały serca, udary, tętniaki i nadciśnienie mają wspólny etap: nasze naczynia krwionośne. Ten przegląd bada nowo rozpoznany sposób obumierania komórek mięśniowych w ścianach naczyń, zwany ferroptozą, ściśle powiązany z żelazem i uszkodzeniem tłuszczów. Składając razem dziesiątki ostatnich badań, autorzy pokazują, jak ten rodzaj śmierci komórkowej może osłabiać naczynia, a w niektórych przypadkach pomagać w powstrzymywaniu szkodliwego nadmiernego wzrostu komórek. Zrozumienie tego obosiecznego procesu może otworzyć nowe drogi zapobiegania i leczenia wielu chorób naczyniowych.
Jak działa śmierć komórki napędzana przez żelazo
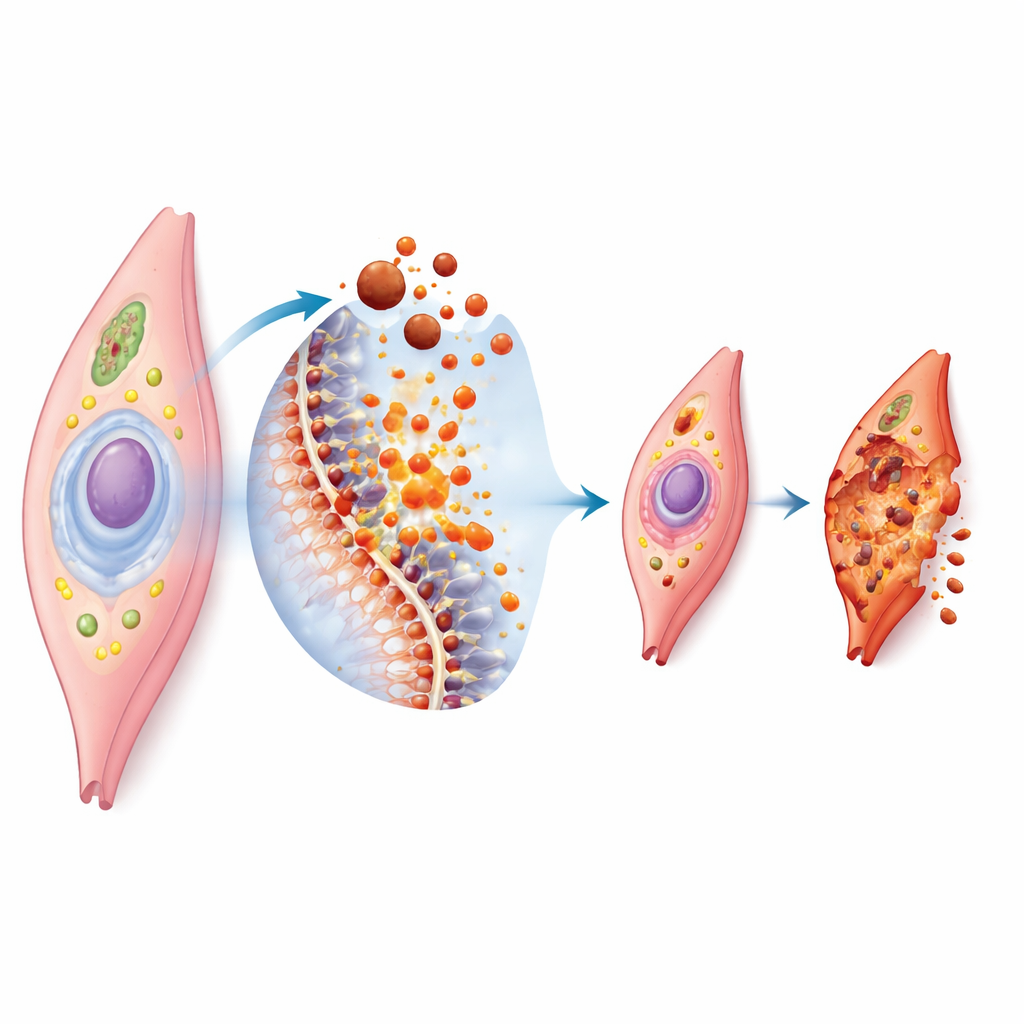
Ferroptoza to forma kontrolowanej śmierci komórki zależna od żelaza i utleniania lipidów w błonach komórkowych. Gdy w komórce gromadzi się zbyt dużo żelaza, sprzyja to powstawaniu wysoce reaktywnych cząsteczek, które atakują lipidowe składniki powłoki komórkowej. Jeśli mechanizmy obronne komórki, takie jak enzymy antyoksydacyjne i ochronne małe cząsteczki, zostaną przytłoczone, błona ulega uszkodzeniu i komórka zapada się. Pod mikroskopem komórki te wykazują skurczone, zdeformowane „elektrownie” energetyczne i przerwane błony zewnętrzne. Ponieważ komórki mięśniowe naczyń są bogate w określone tłuszcze i stale poddawane naprężeniom mechanicznym i chemicznym, są szczególnie wrażliwe, gdy równowaga żelaza i utleniania zostaje zachwiana.
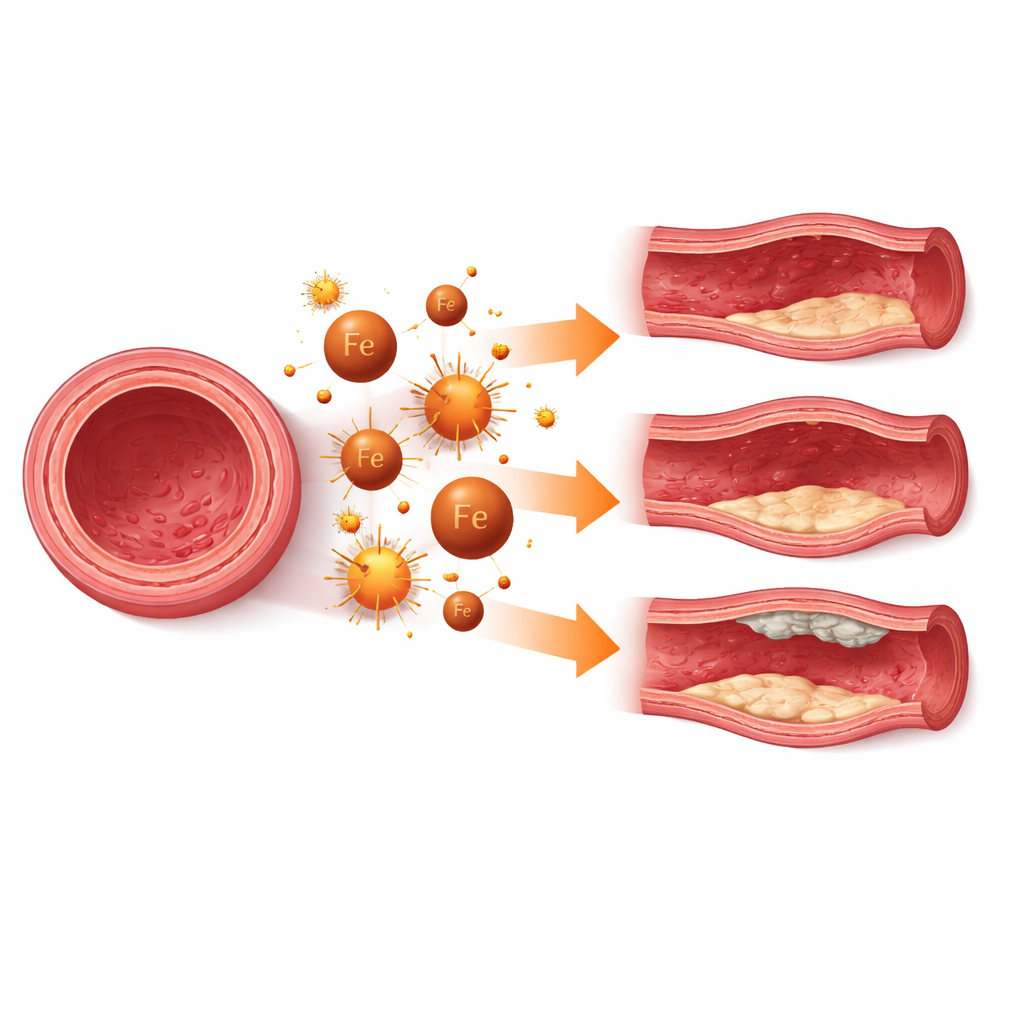
Kiedy śmierć komórek osłabia ścianę naczynia
W wielu chorobach ferroptoza w komórkach mięśni gładkich naczyń działa jak powolny młot niszczący ścianę naczynia. W balonowatych uwypukleniach dużych tętnic, zwanych tętniakami, utrata tych komórek powoduje, że ściana staje się cieńsza i bardziej podatna na pęknięcie. Badania in vitro, na modelach zwierzęcych i w tkankach ludzkich wykazują obecność nagromadzenia żelaza, uszkodzeń lipidów i markerów ferroptozy w obszarach tętniaków. Blokowanie ferroptozy za pomocą eksperymentalnych leków lub wzmacnianie naturalnych mechanizmów obronnych może spowolnić wzrost tętniaka i zachować normalny, kurczliwy stan tych komórek. Podobne wzorce obserwuje się w tętniakach wewnątrzczaszkowych, gdzie ochrona komórek mięśni naczyniowych mózgu przed ferroptozą może pomóc w utrzymaniu wytrzymałości delikatnych tętnic zaopatrujących mózg.
Żelazo, starzejące się blaszki i usztywnianie tętnic
Ferroptoza kształtuje też procesy starzenia i zatykania tętnic. W miażdżycy, chorobie leżącej u podstaw większości zawałów i udarów, niestabilne blaszki często zawierają obumierające lub martwe komórki mięśniowe, uszkodzone lipidy i silną aktywność zapalną. Przegląd podkreśla badania pokazujące, że ferroptoza w tych komórkach może przerzedzać włóknistą czapeczkę stabilizującą blaszkę, zwiększając ryzyko jej pęknięcia. W wapnieniu naczyniowym, częstym przy przewlekłej chorobie nerek i cukrzycy, uszkodzenie lipidów napędzane żelazem skierowuje komórki mięśniowe w stronę fenotypu kostnego i sprzyja odkładaniu się wapnia w ścianie naczynia. W obu przypadkach terapie eksperymentalne, które zmniejszają przeciążenie żelazem, przywracają zdolność antyoksydacyjną lub bezpośrednio hamują ferroptozę, mogą zmniejszać wapnienie i wzmacniać blaszki w modelach zwierzęcych.
Kiedy wywołanie śmierci komórek jest korzystne
Zadziwiająco, ten sam proces może być korzystny, gdy komórki mięśniowe nadmiernie się rozmnażają. W stanach takich jak neointimalna hiperplazja po wszczepieniu stentu czy nadciśnienie płucne w krążeniu płucnym, komórki te przechodzą w wysoce proliferacyjny, syntetyczny stan, który pogrubia ściany naczyń i zwęża światło naczynia. Tutaj problemem nie jest utrata komórek, lecz ich nadmiar. Przegląd opisuje badania, w których łagodne promowanie ferroptozy w nadaktywnych komórkach mięśniowych lub przywrócenie ich wrażliwości na nią może powstrzymać nieprawidłowy wzrost i ograniczyć odkładanie się tkanki bliznowatej. Odwrotnie, gdy ferroptoza jest nadmiernie zahamowana w tych chorobach, przebudowa naczyń pogarsza przepływ krwi i podnosi ciśnienie.
Warstwy kontroli i pojawiające się terapie
Artykuł podkreśla, że ferroptoza w komórkach mięśniowych naczyń jest regulowana przez gęstą sieć kontroli. Chemiczne modyfikacje RNA, przełączniki aktywności genów, dopracowywanie białek po ich syntezie oraz sygnały od sąsiednich komórek immunologicznych i macierzystych przesuwają równowagę w stronę lub przeciwko ferroptozie. Te warstwy zbieżają się wokół trzech podstawowych funkcji: ile żelaza wnika i jest magazynowane, jak łatwo ulegają utlenieniu lipidy błonowe oraz jaka jest siła mechanizmów antyoksydacyjnych. Wiele eksperymentalnych terapii celuje teraz w te dźwignie — od małych cząsteczek i związków naturalnych po narzędzia oparte na RNA, zaprojektowane nanocząstki i egzosomy dostarczające ochronne ładunki bezpośrednio do ściany naczynia.
Co to oznacza dla pacjentów
Podsumowując, przegląd dochodzi do wniosku, że ferroptoza jest centralnym, lecz zależnym od kontekstu, czynnikiem chorób naczyniowych. Gdy wymyka się spod kontroli, niszczy komórki mięśni gładkich, które nadają naczyniom siłę i elastyczność, przyczyniając się do tętniaków, niestabilności blaszek i wapnienia. Gdy jest zbyt silnie blokowana, umożliwia niekontrolowany wzrost komórek i pogrubianie ścian naczyń, jak w niektórych postaciach nadciśnienia i pooperacyjnego bliznowacenia. Wyzwanie dla przyszłej medycyny polega na tym, by nauczyć się, kiedy tłumić ferroptozę, a kiedy ją wykorzystać, i robić to w sposób ukierunkowany na właściwe typy komórek na odpowiednim etapie choroby. Jeśli uda się osiągnąć tę równowagę, terapie wymierzone w ten powiązany z żelazem szlak śmierci komórkowej mogą stać się potężnym narzędziem do zachowania zdrowia naczyń i zmniejszenia obciążenia chorobami naczyniowymi serca, mózgu i płuc.
Cytowanie: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Słowa kluczowe: ferroptoza, komórki mięśni gładkich naczyń, tętniak, miażdżyca, zwapnienie naczyń