Clear Sky Science · it
Ferroptosi delle cellule muscolari lisce nelle malattie vascolari: dai principi di base alla traduzione clinica
Perché la morte delle cellule vascolari conta per la salute di cuore e cervello
Infarti, ictus, aneurismi e ipertensione condividono un palcoscenico comune: i nostri vasi sanguigni. Questa review esplora un modo recentemente riconosciuto in cui le cellule muscolari delle pareti vascolari possono morire, chiamato ferroptosi, strettamente legato al ferro e al danno lipidico. Ricomponendo dozzine di studi recenti, gli autori mostrano come questo tipo di morte cellulare possa sia indebolire i vasi sia, in alcuni casi, contribuire a contenere una crescita cellulare nociva. Comprendere questo processo a doppio taglio potrebbe aprire nuove strade per prevenire o trattare una vasta gamma di malattie vascolari.
Come funziona la morte cellulare guidata dal ferro
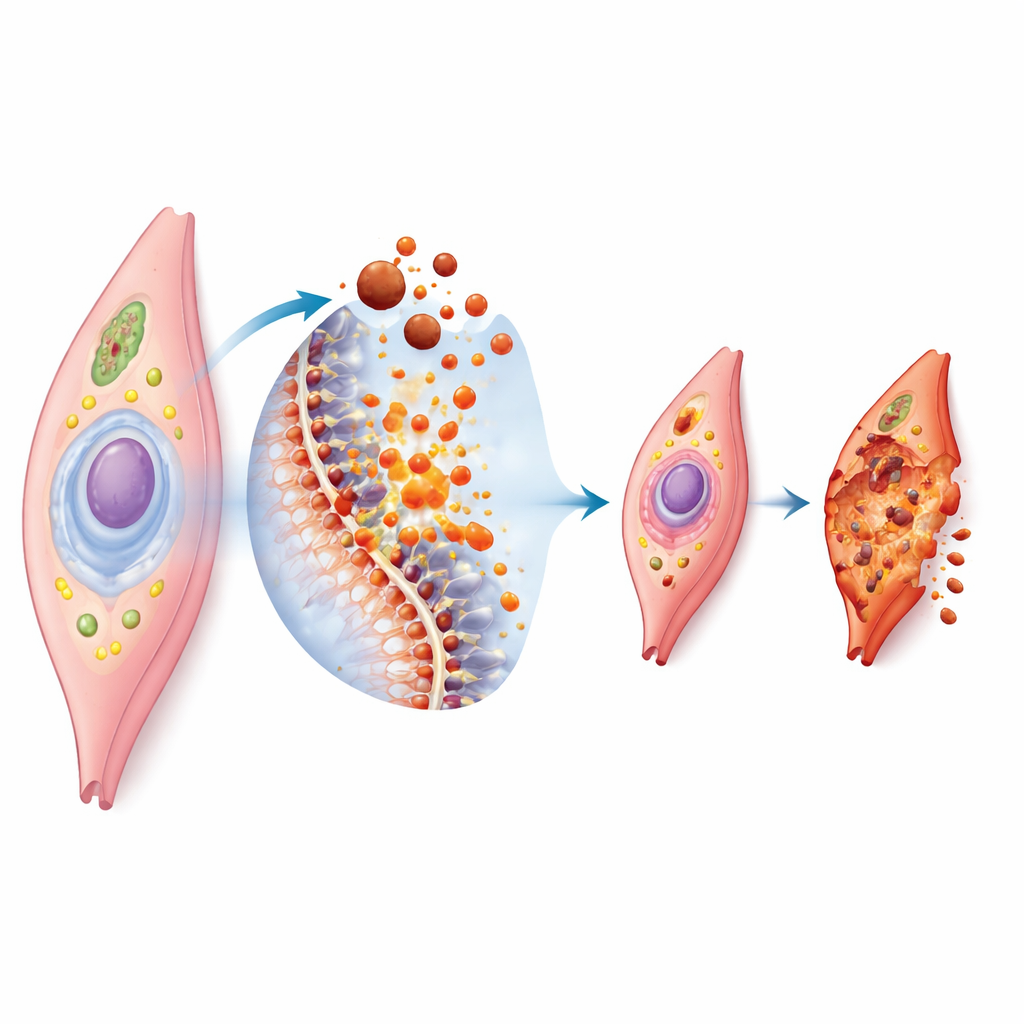
La ferroptosi è una forma di morte cellulare regolata che dipende dal ferro e dalla degradazione dei lipidi nelle membrane cellulari. Quando troppo ferro si accumula all’interno di una cellula, favorisce la formazione di molecole altamente reattive che attaccano i componenti grassi della membrana cellulare. Se i sistemi di difesa della cellula, come enzimi antiossidanti e piccole molecole protettive, vengono sopraffatti, la membrana si danneggia e la cellula collassa. Al microscopio queste cellule mostrano organelli energetici rimpiccioliti e deformati e membrane esterne rotte. Poiché le cellule muscolari vascolari sono ricche di certi lipidi e sopportano costantemente stress meccanici e chimici, risultano particolarmente vulnerabili quando ferro e ossidazione perdono l’equilibrio.
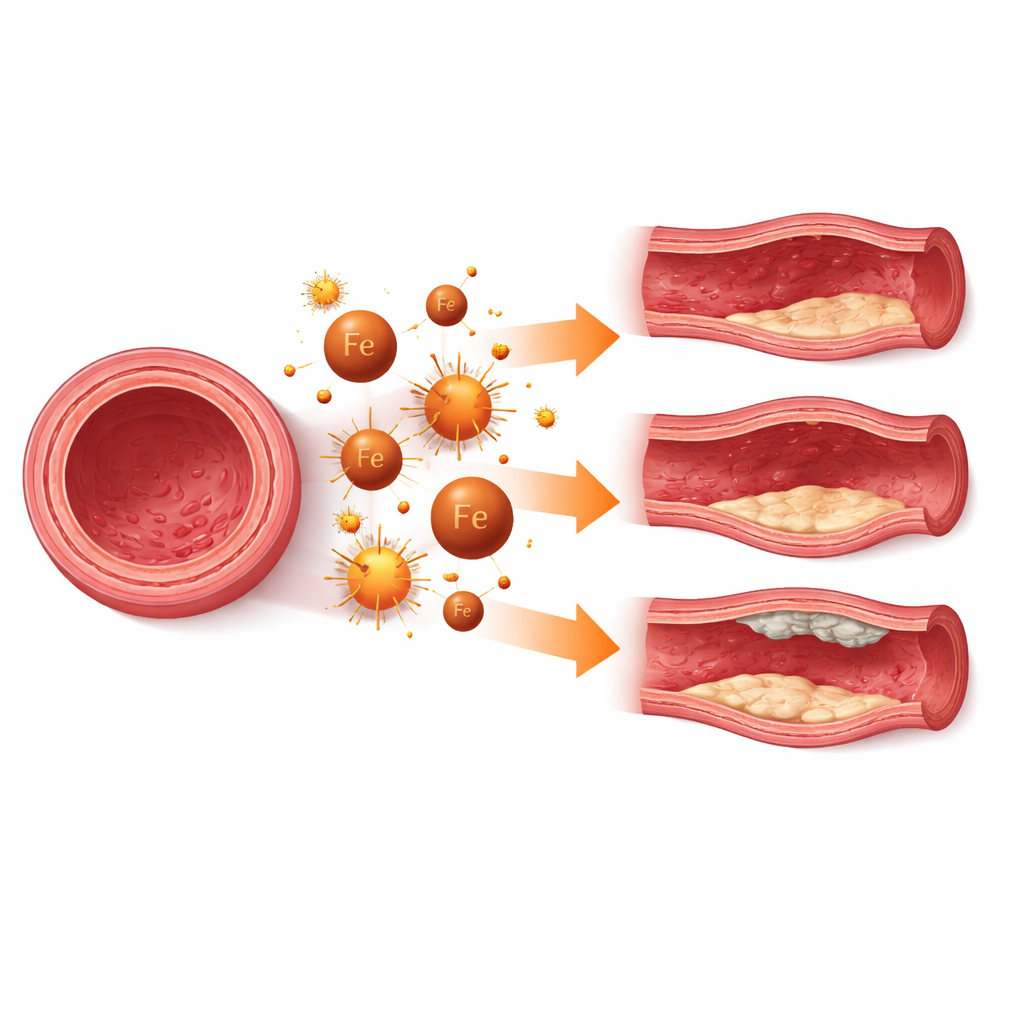
Quando la morte cellulare indebolisce la parete del vaso
In molte malattie, la ferroptosi nelle cellule muscolari lisce vascolari agisce come una lenta palla demolitrice sulla parete del vaso. In rigonfiamenti a forma di pallone delle arterie principali, noti come aneurismi, la perdita di queste cellule muscolari rende la parete più sottile e più facile da lacerare. Studi su cellule, modelli animali e tessuto umano mostrano segni di accumulo di ferro, danno lipidico e marker di ferroptosi nelle regioni aneurismatiche. Bloccare la ferroptosi con farmaci sperimentali o potenziando le difese naturali può rallentare la crescita dell’aneurisma e preservare lo stato contrattile normale di queste cellule. Pattern simili si osservano negli aneurismi intracranici, dove proteggere le cellule muscolari dei vasi cerebrali dalla ferroptosi potrebbe aiutare a mantenere la resistenza delle delicate arterie che irrorano il cervello.
Ferro, placche senescenti e indurimento delle arterie
La ferroptosi influisce anche su come le arterie invecchiano e si ostruiscono. Nell’aterosclerosi, la patologia alla base della maggior parte degli infarti e degli ictus, le placche instabili spesso contengono cellule muscolari lisce morenti o morte, lipidi danneggiati e intensa attività infiammatoria. La review mette in evidenza lavori che dimostrano come la ferroptosi in queste cellule possa assottigliare la cuffia fibrosa che stabilizza la placca, rendendola più suscettibile a rompersi. Nella calcificazione vascolare, comune nella malattia renale cronica e nel diabete, il danno lipidico alimentato dal ferro spinge le cellule muscolari verso uno stato simile all’osso e favorisce depositi di calcio nella parete vascolare. In entrambi i casi, trattamenti sperimentali che riducono il sovraccarico di ferro, ripristinano la capacità antiossidante o inibiscono direttamente la ferroptosi possono attenuare la calcificazione e rafforzare le placche in modelli animali.
Quando indurre la morte cellulare è utile
In modo sorprendente, lo stesso processo può essere benefico quando le cellule muscolari lisce proliferano eccessivamente. In condizioni come l’iperplasia neointimale dopo l’impianto di uno stent, o l’ipertensione arteriosa polmonare, queste cellule passano a uno stato altamente proliferativo e sintetico che ispessisce le pareti vascolari e restringe il lume per il flusso sanguigno. Qui il problema non è la perdita di cellule ma l’eccesso cellulare. La review descrive studi in cui promuovere moderatamente la ferroptosi nelle cellule muscolari iperattive, o ripristinarne la sensibilità, può contenere la crescita anomala e limitare l’accumulo di tessuto cicatriziale. Al contrario, quando la ferroptosi è eccessivamente soppressa in queste patologie, i vasi si rimodellano in modi che peggiorano il flusso sanguigno e aumentano la pressione.
Strati di controllo e terapie emergenti
L’articolo sottolinea che la ferroptosi nelle cellule muscolari vascolari è governata da una fitta rete di controllo. Marchi chimici sull’RNA, interruttori nell’attività genica, modulazioni post-traduzionali delle proteine e segnali da cellule immunitarie e staminali vicine spingono tutti l’equilibrio verso o lontano dalla ferroptosi. Questi livelli convergono su tre funzioni chiave: quanto ferro entra e viene immagazzinato, quanto facilmente i lipidi di membrana vengono ossidati e quanto robuste restano le difese antiossidanti. Molte terapie sperimentali mirano oggi a queste leve, da piccole molecole e composti naturali a strumenti basati su RNA, nanoparticelle ingegnerizzate ed esosomi che trasportano carichi protettivi direttamente alla parete vascolare.
Cosa significa per i pazienti
Nel complesso, la review conclude che la ferroptosi è un fattore centrale, ma dipendente dal contesto, nelle malattie vascolari. Quando sfugge al controllo, distrugge le cellule muscolari lisce che conferiscono ai vasi forza e flessibilità, contribuendo ad aneurismi, instabilità delle placche e calcificazione. Quando è troppo bloccata, permette una crescita cellulare incontrollata e l’ispessimento delle pareti vascolari, come in alcune forme di ipertensione e nella cicatrizzazione post-operatoria. La sfida per la medicina futura è capire quando attenuare la ferroptosi e quando sfruttarla, e farlo in modo da colpire i tipi cellulari giusti nello stadio di malattia appropriato. Se questo equilibrio potrà essere raggiunto, terapie mirate a questa via di morte cellulare legata al ferro potrebbero diventare strumenti potenti per preservare la salute dei vasi sanguigni e ridurre il carico di malattie vascolari di cuore, cervello e polmoni.
Citazione: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Parole chiave: ferroptosi, cellule muscolari lisce vascolari, aneurisma, aterosclerosi, calcificazione vascolare