Clear Sky Science · sv
Ferroptos hos glattmuskelceller i vaskulära sjukdomar: från grundprinciper till klinisk translation
Varför döende kärlceller spelar roll för hjärta och hjärna
Hjärtinfarkter, stroke, aneurysm och högt blodtryck har alla ett gemensamt skede: våra blodkärl. Denna översiktsartikel utforskar en nyligen erkänd väg för hur muskelceller i kärlväggen kan dö — ferroptos — som är starkt kopplad till järn och lipidskador. Genom att sammanföra dussintals nyare studier visar författarna hur denna typ av celldöd både kan försvaga blodkärl och, i vissa fall, hjälpa till att begränsa skadlig cellöverväxt. Att förstå denna tvåeggade process kan öppna nya vägar för att förebygga eller behandla en rad vaskulära sjukdomar.
Hur järndriven celldöd fungerar
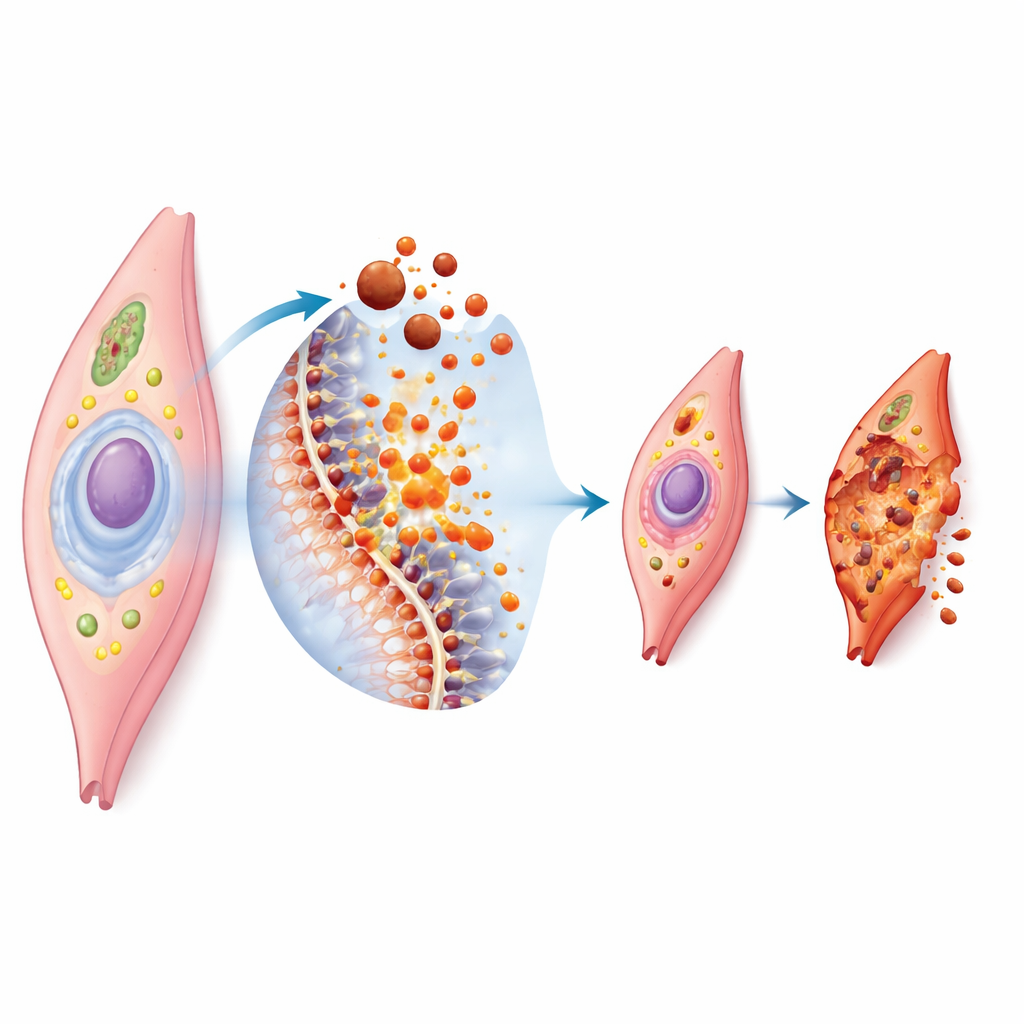
Ferroptos är en form av reglerad celldöd som är beroende av järn och nedbrytning av lipider i cellmembran. När för mycket järn ansamlas i en cell bidrar det till bildning av mycket reaktiva molekyler som angriper de fettkomponenter som utgör cellens yttre skikt. Om cellens egna försvarssystem, såsom antioxidantenzym och skyddande små molekyler, överväldigas blir membranet skadat och cellen kollapsar. Under mikroskop visar dessa celler krympta, förvrängda energiverk och brustna yttre membran. Eftersom blodkärlens muskelceller är rika på vissa fetter och ständigt utsätts för mekanisk och kemisk stress, är de särskilt känsliga när järn och oxidation hamnar ur balans.
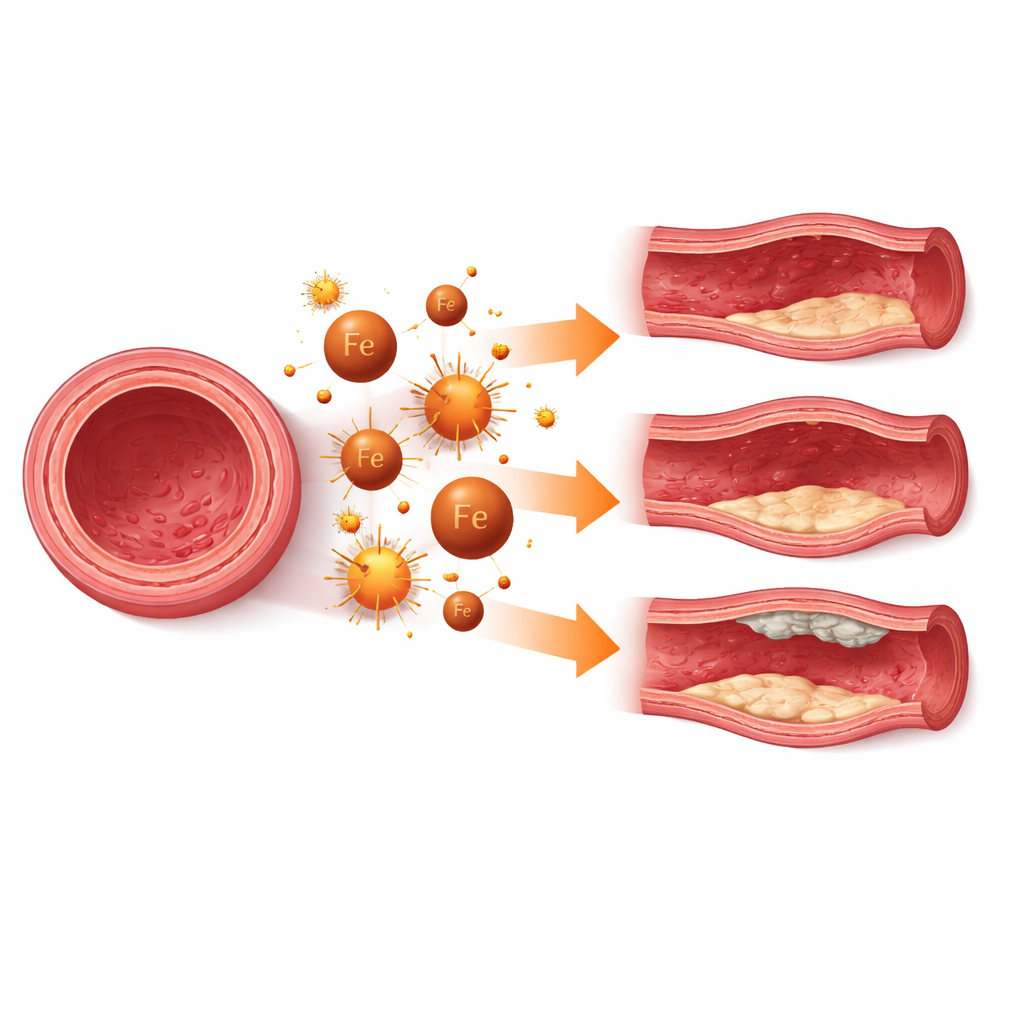
När celldöd försvagar kärlväggen
I många sjukdomar fungerar ferroptos i vaskulära glattmuskelceller som en långsam förstörare av kärlväggen. I ballongliknande utbuktningar av stora artärer, kända som aneurysm, gör förlusten av dessa muskelceller väggen tunnare och mer benägen att brista. Studier i celler, djur och mänsklig vävnad visar alla tecken på järnansamling, lipidskador och markörer för ferroptos i aneurysmområden. Att blockera ferroptos med experimentella läkemedel eller genom att stärka naturliga försvar kan bromsa aneurysmväxt och bevara cellernas normala kontraktila tillstånd. Liknande mönster ses i intrakraniella aneurysm, där skydd av hjärnans kärlmuskelceller mot ferroptos kan bidra till att upprätthålla styrkan i de känsliga artärer som förser hjärnan.
Järn, åldrande plack och förhårdnande artärer
Ferroptos påverkar också hur artärer åldras och täpps till. I ateroskleros, sjukdomen bakom de flesta hjärtinfarkter och strokefall, innehåller instabila plack ofta döende eller döda glattmuskelceller, skadade lipider och stark inflammatorisk aktivitet. Översikten lyfter fram arbete som visar att ferroptos i dessa celler kan tunna ut den fibrösa mössan som stabiliserar ett plack, vilket gör det mer benäget att spricka. Vid vaskulär förkalkning, vanligt vid kronisk njursjukdom och diabetes, driver järninducerad lipidskada muskelceller mot ett benlikt tillstånd och främjar kalciumavlagringar i kärlväggen. I båda sammanhang kan experimentella behandlingar som minskar järnöverskott, återställer antioxidantkapacitet eller direkt hämmar ferroptos minska förkalkning och stärka plack i djurmodeller.
När det är fördelaktigt att utlösa celldöd
Anmärkningsvärt nog kan samma process vara fördelaktig när glattmuskelceller växer för mycket. Vid tillstånd som neointimal hyperplasi efter stentinsättning eller pulmonell arteriell hypertension i lungorna skiftar dessa celler till ett högproliferativt, syntetiskt tillstånd som förtjockar kärlväggarna och förtränger blodflödet. Här är problemet inte cellförlust utan cellexcess. Översikten beskriver studier där mild aktivering av ferroptos i överaktiva muskelceller, eller att återställa deras känslighet för ferroptos, kan dämpa onormal tillväxt och begränsa ackumulering av ärrlik vävnad. Omvänt, när ferroptos är alltför hämmat i dessa sjukdomar omformas kärlen på sätt som försämrar blodflödet och ökar trycket.
Kontrolllager och framväxande behandlingar
Artikeln betonar att ferroptos i kärlmuskelceller styrs av ett tätt nätverk av kontrollmekanismer. Kemiska märkningar på RNA, växlar i genaktivitet, finjustering av proteiner efter translation och signaler från närliggande immunceller och stamceller skjuter alla balansen mot eller bort från ferroptos. Dessa lager sammanstrålar kring tre centrala funktioner: hur mycket järn som kommer in och lagras, hur lätt membranlipider oxideras och hur starka antioxidantförsvaren är. Många experimentella terapier riktar sig nu mot dessa reglage, från små molekyler och naturprodukter till RNA-baserade verktyg, designade nanopartiklar och exosomer som levererar skyddande last direkt till kärlväggen.
Vad detta betyder för patienter
Sammantaget drar översikten slutsatsen att ferroptos är en central, men kontextberoende, drivkraft i vaskulära sjukdomar. När den löper fritt förstörs de glattmuskelceller som ger kärlen styrka och flexibilitet, vilket bidrar till aneurysm, plackinstabilitet och förkalkning. När den är för starkt blockerad möjliggörs okontrollerad celltillväxt och förtjockning av kärlväggar, som i vissa former av högt blodtryck och postoperative ärrbildningar. Utmaningen för framtida medicin är att lära sig när ferroptos ska dämpas och när den ska utnyttjas — och att göra det på ett sätt som riktar in sig på rätt celltyper i rätt sjukdomsstadium. Om den balansen kan uppnås kan terapier som riktar sig mot denna järnkopplade celldödssignal bli kraftfulla verktyg för att bevara kärlhälsa och minska bördan av hjärta-, hjärna- och lungbaserade kärlsjukdomar.
Citering: Yang, Y., Nawabi, A.Q., Yao, Y. et al. Ferroptosis of smooth muscle cells in vascular diseases: from basic principles to clinical translation. Cell Death Discov. 12, 140 (2026). https://doi.org/10.1038/s41420-026-02950-1
Nyckelord: ferroptos, vaskulära glattmuskelceller, aneurysm, ateroskleros, vaskulär förkalkning