Clear Sky Science · zh
乳酸通过细胞内酸化驱动NLRP3炎症小体激活和类半胱天冬酶‑1样细胞因子切割
当一种“运动分子”反过来伤害我们
乳酸以在剧烈跑步后肌肉产生的灼痛感而闻名,但它在严重感染如脓毒症中也会积累。该研究揭示,乳酸不仅仅是简单的代谢废物:在免疫细胞内,它有助于开启强烈的炎症机制,甚至能够独立化学性地切割关键的免疫信使分子。理解乳酸的这种二重性可能会重塑我们对脓毒症、癌症及其他严重疾病中炎症机制的认识。 
免疫细胞如何感知危险
我们对感染的第一道防线依赖固有免疫细胞,如巨噬细胞,它们能快速感知危险并释放警报信号。这些细胞内的一个中心控制枢纽,被称为NLRP3炎症小体,对多种威胁作出反应并激活一种酶,将不活跃的细胞因子前体切割成活性形式。这些活性片段,尤其是IL‑1β和IL‑18,随后被分泌以召集其他免疫细胞。尽管这种反应有助于清除感染,但当其过度激活时,会促成如脓毒性休克等危及生命的状况。
燃料利用、细胞酸度与免疫开关
为了驱动这一快速的警报系统,巨噬细胞会将代谢转向糖酵解——一种快速分解糖并产生乳酸的途径。研究者表明,当NLRP3被触发时,免疫细胞迅速增加乳酸产生并在细胞内滞留更多乳酸。这种累积使细胞内环境酸化,反过来强烈促进炎症小体的组装、酶的激活和IL‑1β的释放。细胞外的酸性条件阻碍乳酸外排,进一步加深细胞内部的酸性转变并放大反应。将周围液体提升到略碱性的pH可以阻止这种酸化并几乎完全抑制炎症小体活性,而不会阻止乳酸本身的产生。
细胞内部:通向炎症的连锁反应
深入研究显示,乳酸驱动的酸化破坏线粒体——细胞的能量工厂,并增加活性氧(ROS),这是一类化学应激信号。与此同时,它激活一种名为PKR的应激感应酶并促进其与NLRP3装置的物理相互作用。线粒体应激和PKR激活被证明都是实现完整炎症小体功能所必需的。阻断乳酸产生或使环境更碱性可降低这些应激信号,削弱PKR–NLRP3的相互作用,并抑制炎症小体复合物的形成。 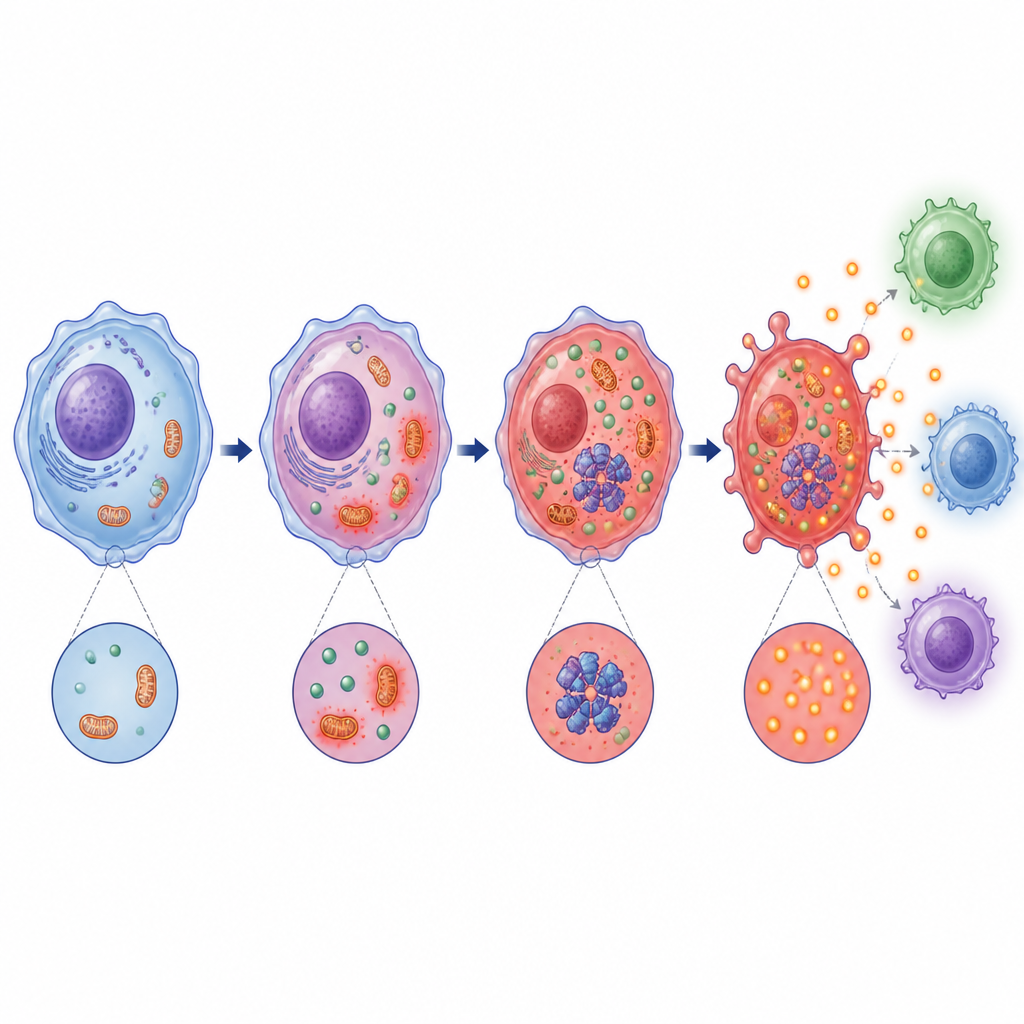
乳酸作为化学“外科刀”
令人意外的是,乳酸还发挥着第二种独立作用。在缺乏完整炎症小体装置的细胞提取物中,仅加入乳酸就足以将IL‑1β和IL‑18前体切割成与通常酶产生的成熟片段相匹配的大小。这种化学性切割需要乳酸的酸性、不解离形式,并依赖于IL‑1β内的特定位点——与酶通常切割的位置相同。具有相似化学基团的其他有机酸在较小程度上也能做到这一点,而单独的强矿质酸效果要差得多,这提示乳酸本身的结构在非常酸性条件下有助于驱动这种精确的切割反应。
这对脓毒症及其他疾病意味着什么
为在活体系统中检验这些想法,研究者使用了多菌种脓毒症的小鼠模型,这是一种严重的全身性感染。在脓毒症小鼠中提高血乳酸水平会增加血液和腹腔中的IL‑1β,吸引更多中性粒细胞到感染部位,降低体温并恶化存活率。用一种阻断NLRP3的药物处理小鼠大体上逆转了这些有害效应,强调了乳酸激增主要通过该通路助长炎症。综合来看,这些发现表明乳酸是促炎症的双重驱动者:既通过重塑细胞代谢以促进炎症小体激活,又在极端酸性条件下直接加工关键细胞因子。
这些发现为何重要
对非专业读者而言,核心信息是乳酸并非仅仅是运动或疾病后的无害副产物。在受应激的免疫细胞内,它会变成一种“把火调大”的信号,使炎症更强且更难控制。在乳酸和酸度同时升高的疾病如脓毒症中,这可能将防御性反应推向有害的全身性破坏。通过揭示乳酸如何将免疫细胞推入这种过度活化状态,以及它在极端酸性下如何直接影响炎性信使,这项工作指向了通过靶向细胞酸处理和NLRP3系统来抑制有害炎症的新策略。
引用: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
关键词: 乳酸, 炎症小体, IL-1β, 脓毒症, 免疫代谢