Clear Sky Science · nl
Melkzuur zorgt voor activatie van het NLRP3-inflammasoom en caspase-1–achtige cytokineknip via intracellulaire acidificatie
Wanneer een trainingsmolecuul zich tegen ons keert
Melkzuur is bekend van de brandende sensatie in je spieren na een zware loop, maar het hoopt zich ook op tijdens ernstige infecties zoals sepsis. Deze studie laat zien dat melkzuur meer is dan een eenvoudig afvalproduct: binnen immuuncellen helpt het krachtige ontstekingsmechanismen aan te zetten en kan het zelfs zelfstandig sleutelboodschappers van het immuunsysteem chemisch splijten. Begrijpen dat melkzuur zo’n dubbele rol heeft kan onze kijk op ontsteking bij sepsis, kanker en andere ernstige ziekten veranderen. 
Hoe immuuncellen gevaar waarnemen
Onze eerste verdedigingslinie tegen infecties berust op het aangeboren immuunsysteem, met cellen zoals macrofagen die snel gevaar detecteren en alarmstoffen vrijgeven. Een centraal regelpunt in deze cellen, het NLRP3-inflammasoom, reageert op een breed scala aan bedreigingen en activeert een enzym dat inactieve cytokinevoormolesculen in hun actieve vormen knipt. Deze actieve fragmenten, vooral IL-1β en IL-18, worden vervolgens uitgescheiden om andere immuuncellen te mobiliseren. Hoewel deze respons kan helpen bij het opruimen van infecties, draagt ze bij aan levensbedreigende toestanden zoals septische shock wanneer ze te sterk wordt.
Brandstofgebruik, celzuurgraad en een immuunknop
Om dit snelle alarmsysteem van energie te voorzien schakelen macrofagen hun stofwisseling naar glycolyse, een snelle manier om suiker af te breken die melkzuur produceert. De onderzoekers toonden aan dat wanneer NLRP3 geactiveerd is, immuuncellen snel meer melkzuur produceren en meer daarvan binnenshuis vasthouden. Deze ophoping verzacht het celinterieur en versterkt op zijn beurt krachtig de assemblage van het inflammasoom, enzymactivatie en de afgifte van IL-1β. Zure omstandigheden buiten de cel belemmeren het verlaten van melkzuur, wat de interne verzuring verder verdiept en de respons versterkt. Het verhogen van de omringende vloeistof naar een licht basisch pH voorkwam deze verzuring en schakelde de inflammasoomactiviteit bijna volledig uit zonder zelf de melkzuurproductie te stoppen.
In de cel: een kettingreactie naar ontsteking
Dieper onderzoek toonde aan dat door melkzuur veroorzaakte verzuring de mitochondriën — de energiecentrales van de cel — verstoort en het aantal reactieve zuurstofsoorten verhoogt, een type chemisch stresssignaal. Tegelijkertijd activeert het een stress-sensorisch enzym genaamd PKR en bevordert het de fysieke interactie ervan met het NLRP3-machinery. Zowel de mitochondriale stress als PKR-activatie bleken nodig voor volledige inflammasoomfunctie. Het blokkeren van melkzuurproductie of het basisch maken van de omgeving verminderde deze stresssignalen, verzwakte het PKR–NLRP3-partnerschap en beperkte de vorming van het inflammasoomcomplex. 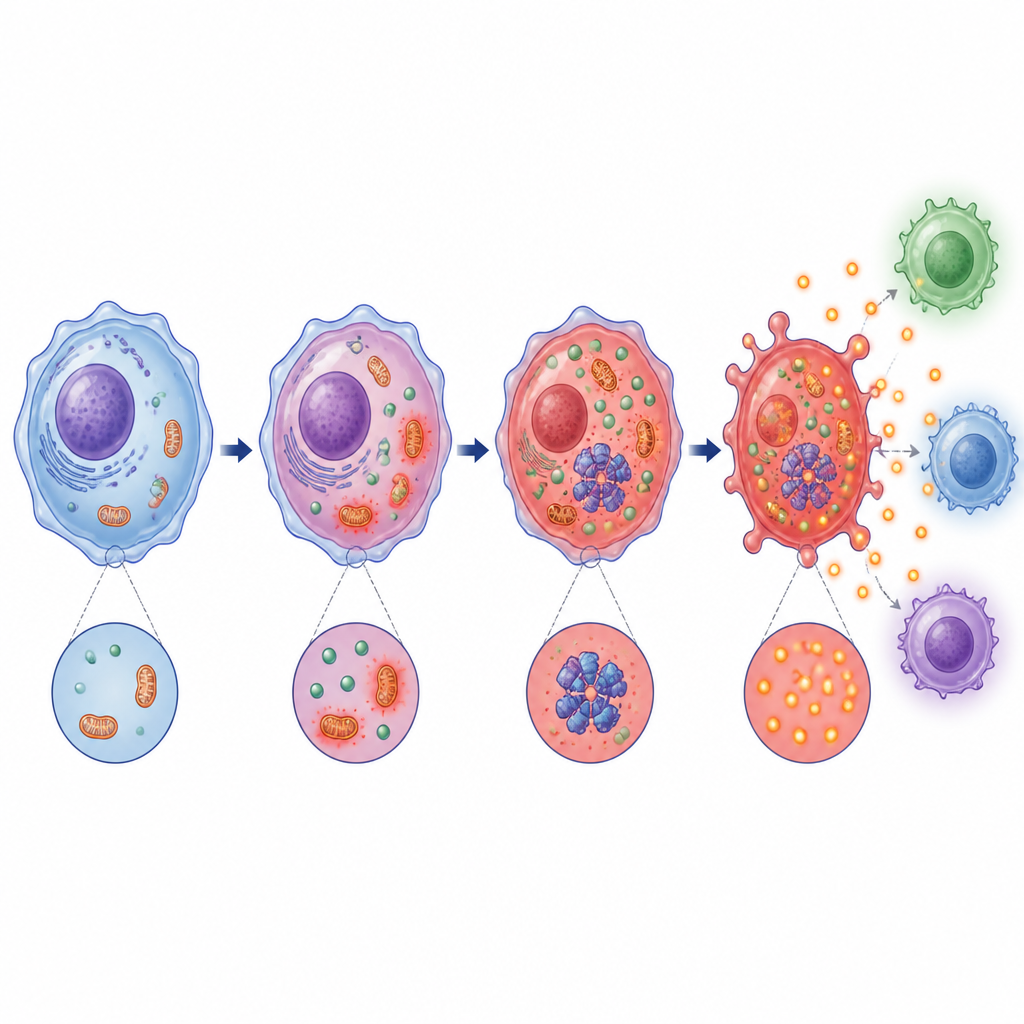
Melkzuur als chemisch “scalpel”
Verrassend genoeg speelde melkzuur ook een tweede, onafhankelijke rol. In celextracten zonder intacte inflammasoommachinerie was het al voldoende om simpelweg melkzuur toe te voegen om de IL-1β- en IL-18-voormoleculen in volwassen-grote fragmenten te splijten die overeenkwamen met die door het gebruikelijke enzym geproduceerd. Deze chemische knip vereiste de zure, niet-gedissocieerde vorm van melkzuur en was afhankelijk van een specifieke plaats binnen IL-1β, dezelfde plaats die normaal door het enzym wordt gebruikt. Andere organische zuren met vergelijkbare chemische groepen konden dit in mindere mate ook doen, terwijl sterke minerale zuren veel minder effectief waren, wat suggereert dat de eigen structuur van melkzuur bijdraagt aan deze nauwkeurige splijtingsreactie onder zeer zure omstandigheden.
Wat dit betekent voor sepsis en andere ziekten
Om deze ideeën in een levend systeem te testen gebruikten de onderzoekers een muismodel van polymicrobiële sepsis, een ernstige, lichaam-brede infectie. Het verhogen van het lactaatgehalte in bloed van zestigende muizen leidde tot meer IL-1β in bloed en buikholte, trok meer neutrofielen naar de infectieplaats, verlaagde de lichaamstemperatuur en verslechterde de overleving. Behandeling van de muizen met een medicijn dat NLRP3 blokkeert keerde deze schadelijke effecten grotendeels om, wat benadrukt dat de melkzuurpiekaanvoer ontsteking voornamelijk via dit pad voedt. Gezamenlijk suggereren de bevindingen dat melkzuur een tweesporige aanjager van ontsteking is: enerzijds door de celstofwisseling te verschuiven naar inflammasoomactivatie en anderzijds door sleutelcytokines direct te verwerken wanneer de zuurgraad extreem is.
Waarom deze bevindingen ertoe doen
Voor een niet-specialistische lezer is de kernboodschap dat melkzuur niet louter een onschadelijk bijproduct van inspanning of ziekte is. Binnen gestreste immuuncellen wordt het een signaal dat zegt “maak het vuur groter”, waardoor ontsteking krachtiger en moeilijker te beheersen wordt. In toestanden zoals sepsis, waarin zowel melkzuur als zuurgraad stijgen, kan dit het evenwicht verschuiven van een nuttige verdediging naar gevaarlijke, lichaam-brede schade. Door te onthullen hoe melkzuur immuuncellen in deze overactieve staat drijft, en hoe het ontstekingsboodschappers direct kan vormen, wijst dit werk op nieuwe strategieën om schadelijke ontsteking te temperen door de behandeling van cellulaire zuurgraad en het NLRP3-systeem te richten.
Bronvermelding: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Trefwoorden: melkzuur, inflammasoom, IL-1β, sepsis, immuunmetabolisme