Clear Sky Science · sv
Mjölksyra driver aktivering av NLRP3-inflammasomen och caspas-1–lik klyvning av cytokiner via intracellulär försurning
När en träningsmolekyl vänder sig mot oss
Mjölksyra är känd för den brännande känslan i musklerna efter ett hårt löpass, men den ackumuleras också vid allvarliga infektioner som sepsis. Denna studie visar att mjölksyra kan vara mer än en enkel avfallsprodukt: inne i immunceller hjälper den till att slå på kraftfulla inflammatoriska mekanismer och kan till och med kemiskt klyva viktiga immunkurirer på egen hand. Att förstå denna dubbla roll för mjölksyra kan förändra hur vi ser på inflammation vid sepsis, cancer och andra allvarliga sjukdomar. 
Hur immunceller känner igen fara
Vårt första försvar mot infektioner bygger på det medfödda immunsystemets celler, såsom makrofager, som snabbt känner av fara och släpper ut larm. En central kontrollpunkt i dessa celler, kallad NLRP3-inflammasomen, reagerar på en rad olika hot och aktiverar ett enzym som klyver inaktiva cytokinprekursorer till deras aktiva former. Dessa aktiva fragment, särskilt IL-1β och IL-18, sekreteras sedan för att samla andra immunceller. Medan detta svar kan hjälpa till att rensa infektioner, bidrar det – när det blir överdrivet – till livshotande tillstånd som septisk chock.
Bränsleanvändning, cellens surhetsgrad och en immunomkopplare
För att driva detta snabba larmsystem skiftar makrofager sin metabolism mot glykolys, ett snabbt sätt att bryta ner socker som producerar mjölksyra. Forskarna visade att när NLRP3 triggas ökar immunceller snabbt sin produktion av mjölksyra och fångar mer av den inuti. Denna uppbyggnad försurer cellens inre och förstärker i sin tur starkt inflammasomets montering, enzymaktivering och frisättning av IL-1β. Sur miljö utanför cellen hindrar dessutom mjölksyran från att lämna, vilket fördjupar den interna försurningen och förstärker svaret. Att höja omgivande vätskas pH till lätt basiskt förhindrade denna försurning och släckte nästan helt inflammasom-aktiviteten utan att stoppa själva mjölksyreproduktionen.
Inne i cellen: en kedjereaktion mot inflammation
Vid en närmare granskning fann teamet att mjölksyrainducerad försurning stör mitokondrierna, cellens kraftverk, och ökar reaktiva syreföreningar, en typ av kemisk stressignal. Samtidigt aktiverar den ett stresskännande enzym kallat PKR och främjar dess fysiska interaktion med NLRP3-komplexet. Både mitokondriell stress och PKR-aktivering visade sig vara nödvändiga för full inflammasomfunktion. Att blockera mjölksyreproduktionen eller göra miljön mer basisk minskade dessa stressignaler, försvagade PKR–NLRP3-samarbetet och dämpade bildandet av inflammasomkomplexet. 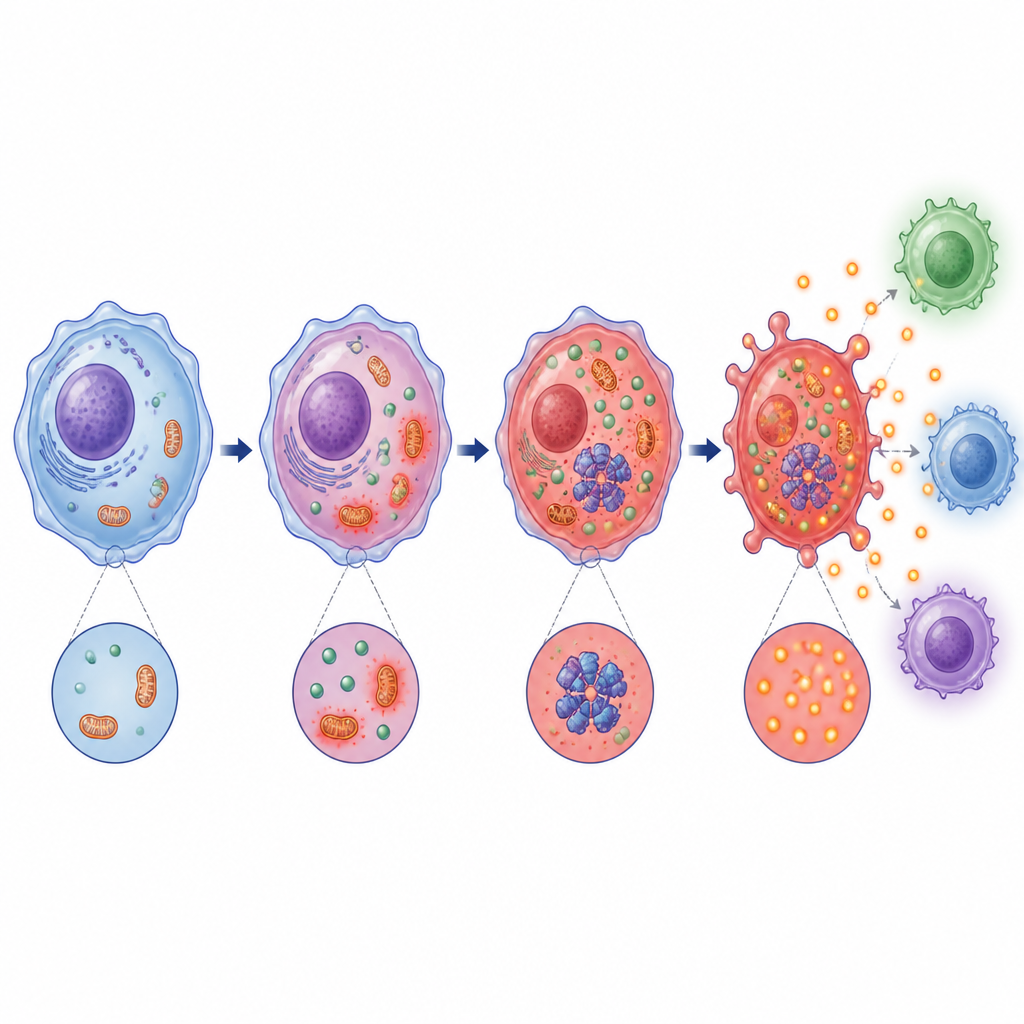
Mjölksyra som ett kemiskt "skalpell"
Överraskande nog spelade mjölksyra även en andra, oberoende roll. I cellextrakt som saknade intakt inflammasomutrustning var det tillräckligt att tillsätta mjölksyra för att klyva IL-1β- och IL-18-prekursorerna till mogna storlekar som matchade de bitar som det vanliga enzymet producerar. Denna kemiska klyvning krävde den sura, odissocierade formen av mjölksyra och var beroende av en specifik plats i IL-1β, samma plats som enzymet normalt använder. Andra organiska syror med liknande kemiska grupper kunde göra detta i mindre grad, medan stark mineralisk syra ensam var mycket mindre effektiv, vilket tyder på att mjölksyrans egen struktur hjälper till att driva denna precisa klyvningsreaktion under mycket sura förhållanden.
Vad detta innebär för sepsis och andra sjukdomar
För att testa dessa idéer i ett levande system använde forskarna en musmodell för polymikrobiell sepsis, en svår, kroppsomfattande infektion. Att öka blodets laktatnivåer hos septiska möss ökade IL-1β i blodet och i bukhålan, drog fler neutrofiler till infektionsstället, sänkte kroppstemperaturen och försämrade överlevnaden. Behandling av mössen med ett läkemedel som blockerar NLRP3 reverserade i stor utsträckning dessa skadliga effekter, vilket belyser att mjölksyrespurten driver inflammation främst via denna väg. Tillsammans tyder fynden på att mjölksyra är en tvådelad drivkraft för inflammation, både genom att omforma cellmetabolismen för att gynna inflammasomaktivering och genom att direkt processa nyckelcytokiner när syran blir extrem.
Varför dessa fynd är viktiga
För en lekmannaläsare är huvudbudskapet att mjölksyra inte bara är en ofarlig biprodukt av träning eller sjukdom. I stressade immunceller blir den en signal som säger "höj elden", vilket gör inflammationen starkare och svårare att kontrollera. Vid tillstånd som sepsis, där både mjölksyra och surhet ökar, kan detta välta balansen från ett hjälpsamt försvar till farlig, systemisk skada. Genom att visa hur mjölksyra driver immunceller in i detta överaktiva tillstånd, och hur den kan forma inflammatoriska budbärare direkt, pekar detta arbete mot nya strategier för att dämpa skadlig inflammation genom att rikta in sig på cellernas syrahantering och NLRP3-systemet.
Citering: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Nyckelord: mjölksyra, inflammasom, IL-1β, sepsis, immunmetabolism