Clear Sky Science · de
Milchsäure treibt die Aktivierung des NLRP3-Inflammasoms und die caspase-1‑ähnliche Zytokinschnittbildung durch intrazellulare Versauerung voran
Wenn ein Trainingsmolekül gegen uns arbeitet
Milchsäure ist bekannt für das Brennen in den Muskeln nach einem harten Lauf, sie reichert sich aber auch bei schweren Infektionen wie Sepsis an. Diese Studie zeigt, dass Milchsäure mehr ist als nur ein Abfallprodukt: In Immunzellen trägt sie zur Aktivierung mächtiger entzündlicher Mechanismen bei und kann sogar eigenständig wichtige Immunbotenstoffe chemisch zerschneiden. Das Verständnis dieses Doppellebens der Milchsäure könnte unsere Sicht auf Entzündungen bei Sepsis, Krebs und anderen schweren Erkrankungen verändern. 
Wie Immunzellen Gefahr wahrnehmen
Unsere erste Verteidigungslinie gegen Infektionen beruht auf angeborenen Immunzellen wie Makrophagen, die schnell Gefahren erkennen und Warnsignale aussenden. Ein zentrales Steuerzentrum in diesen Zellen, das NLRP3-Inflammasom, reagiert auf eine breite Palette von Bedrohungen und aktiviert ein Enzym, das inaktive Zytokinvorstufen in ihre aktive Form zerschneidet. Diese aktiven Fragmente, insbesondere IL-1β und IL-18, werden anschließend ausgeschüttet, um andere Immunzellen zu mobilisieren. Während diese Reaktion bei der Beseitigung von Infektionen hilft, trägt sie bei Überaktivierung zu lebensbedrohlichen Zuständen wie septischem Schock bei.
Energieverbrauch, Zellansäuerung und ein Immunumschalter
Um dieses schnelle Alarmsystem zu betreiben, verlagern Makrophagen ihren Stoffwechsel hin zur Glykolyse, einem schnellen Weg zur Zuckerzerlegung, der Milchsäure produziert. Die Forscher zeigten, dass bei Auslösung von NLRP3 Immunzellen rasch mehr Milchsäure produzieren und verstärkt in der Zelle zurückhalten. Diese Anreicherung versauert das Zellinnere und verstärkt wiederum deutlich die Assemblierung des Inflammasoms, die Enzymaktivierung und die Freisetzung von IL-1β. Säurehaltige Bedingungen außerhalb der Zelle hindern Milchsäure am Verlassen der Zelle, vertiefen die interne Ansäuerung und verstärken die Reaktion weiter. Eine leicht alkalische Anhebung der umgebenden Flüssigkeit verhinderte diese Versauerung und schaltete die Inflammasomaktivität nahezu vollständig aus, ohne die Milchsäureproduktion selbst zu stoppen.
Im Inneren der Zelle: Eine Kettenreaktion zur Entzündung
Tiefergehende Untersuchungen ergaben, dass die durch Milchsäure bedingte Versauerung die Mitochondrien, die Kraftwerke der Zelle, stört und die Bildung reaktiver Sauerstoffspezies erhöht, eine Form chemischen Stresssignals. Gleichzeitig aktiviert sie ein Stress-sensitives Enzym namens PKR und fördert dessen physische Interaktion mit dem NLRP3-Apparat. Sowohl der mitochondriale Stress als auch die PKR-Aktivierung erwiesen sich als notwendig für die volle Funktion des Inflammasoms. Das Blockieren der Milchsäureproduktion oder eine alkalischere Umgebung verringerte diese Stresssignale, schwächte die PKR–NLRP3-Partnerschaft und bremste die Bildung des Inflammasomkomplexes. 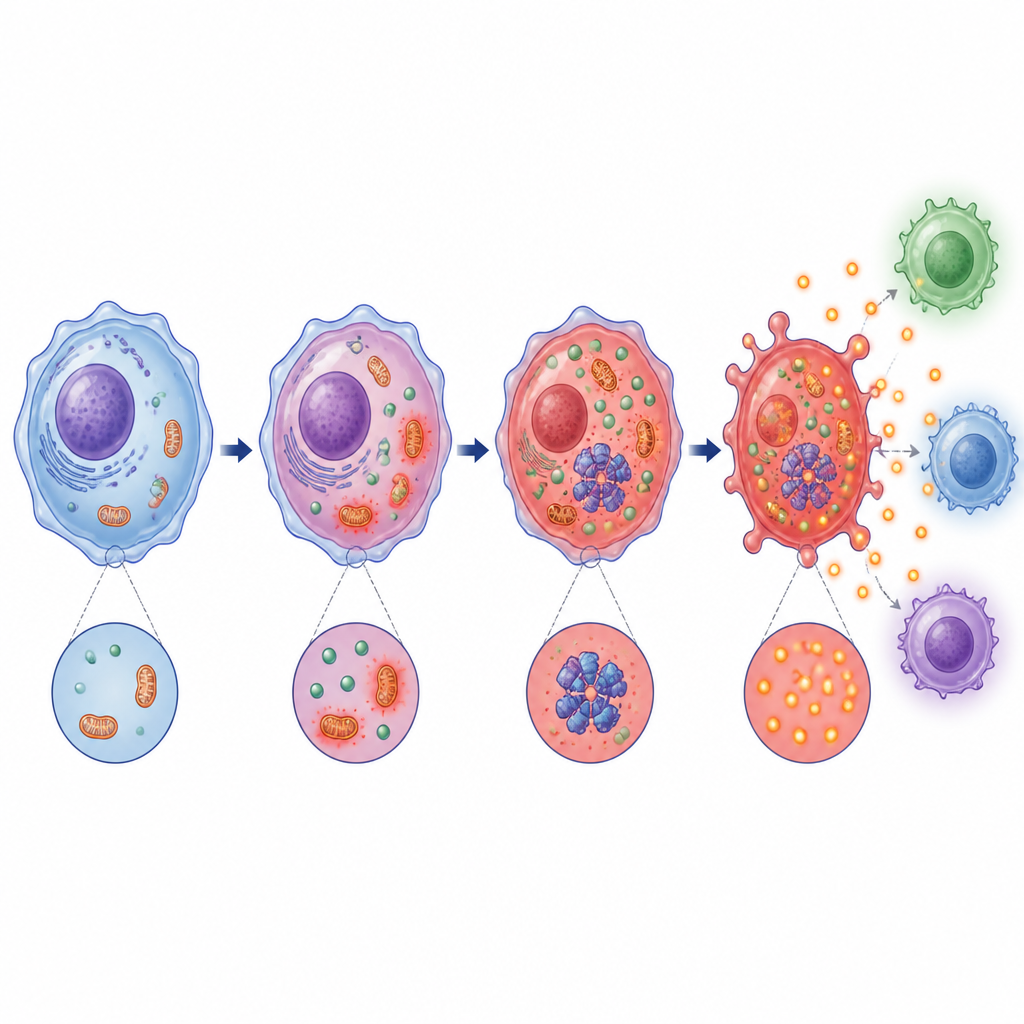
Milchsäure als chemisches „Skalpell"
Überraschenderweise erfüllte Milchsäure auch eine zweite, unabhängige Rolle. In Zellextrakten ohne intakte Inflammasom-Maschinerie war das einfache Hinzufügen von Milchsäure ausreichend, um die Vorstufen von IL-1β und IL-18 in reife, größenpassende Fragmente zu schneiden, die denen des üblichen Enzyms entsprachen. Dieses chemische Schneiden erforderte die saure, undissoziierte Form der Milchsäure und hing von einer bestimmten Stelle innerhalb von IL-1β ab, der gleichen Stelle, die normalerweise vom Enzym genutzt wird. Andere organische Säuren mit ähnlichen chemischen Gruppen konnten dies in geringerem Maße ebenfalls bewirken, während starke Mineralsäure allein deutlich weniger effektiv war. Das deutet darauf hin, dass die spezifische Struktur der Milchsäure diese präzise Spaltungsreaktion unter sehr sauren Bedingungen unterstützt.
Was das für Sepsis und andere Krankheiten bedeutet
Um die Konzepte in einem lebenden System zu testen, verwendeten die Forscher ein Mausmodell für polymikrobielle Sepsis, eine schwere, den ganzen Körper erfassende Infektion. Eine Erhöhung des Blutlaktatspiegels bei septischen Mäusen steigerte IL-1β im Blut und in der Bauchhöhle, zog mehr Neutrophile an den Infektionsort, senkte die Körpertemperatur und verschlechterte das Überleben. Die Behandlung der Mäuse mit einem Wirkstoff, der NLRP3 blockiert, kehrte diese schädlichen Effekte weitgehend um und unterstreicht, dass die Milchsäurewelle die Entzündung hauptsächlich über diesen Weg antreibt. Zusammen deuten die Befunde darauf hin, dass Milchsäure Entzündung auf zweifache Weise fördert: durch Umgestaltung des Zellstoffwechsels zugunsten der Inflammasomaktivierung und durch direkte Verarbeitung wichtiger Zytokine bei extremer Versauerung.
Warum diese Ergebnisse wichtig sind
Für den Laien ist die Kernbotschaft, dass Milchsäure nicht bloß ein harmloses Nebenprodukt von Sport oder Krankheit ist. In gestressten Immunzellen wird sie zu einem Signal, das sagt: "heiz das Feuer an" — sie verstärkt Entzündungen und macht sie schwerer kontrollierbar. In Zuständen wie Sepsis, in denen sowohl Milchsäure als auch Azidität steigen, kann dies das Gleichgewicht von einer hilfreichen Abwehr zu gefährlichem, systemischem Schaden kippen. Indem gezeigt wird, wie Milchsäure Immunzellen in diesen überaktiven Zustand treibt und wie sie direkt entzündliche Botenstoffe formt, weist diese Arbeit auf neue Strategien hin, schädliche Entzündungen durch gezielte Beeinflussung der zellulären Säureverhältnisse und des NLRP3-Systems zu dämpfen.
Zitation: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Schlüsselwörter: Milchsäure, Inflammasom, IL-1β, Sepsis, Immunstoffwechsel